|
x |
x |
|
 |
 |
|
INFECTIOUS
DISEASE |
BAKTERIYOLOJİ |
İMMÜNOLOJİ |
MYCOLOGY |
PARASITOLOGY |
VİROLOJİ |
|
ENGLISH |
VIROLOJİ -
BÖLÜM ONİKİ
VIRUS-KONAK İLİŞKİLERİ
Dr Gene Mayer
Emeritus Professor
Department of Pathology, Microbiology and Immunology
University of South Carolina School of Medicine
Columbia
Çeviren. Prof.
Dr. Selçuk Kaya
İzmir Katip Çelebi Üniversitesi, Tıp Fakültesi
|
|
Español |
|
FRANCAIS |
Let us know what you think
FEEDBACK |
|
SEARCH |
|
|

 |
|
Logo image
© Jeffrey Nelson, Rush University, Chicago, Illinois and
The MicrobeLibrary |
|
|
|
|
|
ÖĞRETİM HEDEFLERİ Virus
infeksiyonlarından kurtulma ve dirence katılan konak spesifik ve
nonspesifik savunma mekanizmalarını tanımlamak
Viral enfeksiyonlarda interferon rolünü tartışmak
Interferonun hangi mekanizmalarla antiviral aktivite sergilediğini
gözden geçirmek
Viral enfeksiyonlarda çeşitli konak savunma mekanizmalarının göreceli
katkılarını tartışmak
|
Viral enfeksiyonların
iyileşmesi ve ona karşı direnç oluşumu, virüs ve konak arasında meydana
gelen etkileşimlere bağlıdır. Konak tarafından yapılan savunmalar:
enfekte hücreyi öldürerek veya değiştirerek virüs replikasyonunda
indirek veya virüs üzerinde direk olarak etki gösterebilir. Spesifik
konak savunmaları sonradan gelişen tepkiler için bağışıklık sağlandıktan
sonra ortaya çıkan enfeksiyonlarda işlev görürken, spesifik olmayan
konak savunmaları enfeksiyonu sınırlama veya virüsle karşılaşmayı
önlemede erken fonksiyon gösterir. Belirli bir viral enfeksiyonda konak
savunması: virüse, doza ve giriş kapısına bağlı olarak değişmesine
rağmen, virüs-konak etkileşimlerinin bazı genel esasları aşağıda
özetlenmiştir.
INFEKSIYON ENGELLEYİCİLER
Kalıtsal Bariyerler
Konak organizmada, kalıtsal olarak belirli sayıda enfeksiyon
bariyerleri bulunur. Bunlar enfeksiyonu sınırlama veya önleme
fonksiyonuna sahip olan ilk savunma hattını temsil eder.
Deri
Deri, çoğu virüslere karşı aşılması zor bir bariyer etkisi
gösterir ve yalnızca bu bariyerin bozulması sonrasında
virüsler konağı enfekte edebilir.
Membran Reseptörlerinin
Eksikliği
Virüsler ilk olarak hücreler üzerindeki spesifik
reseptörlere bağlanarak konak hücrelerin içine giriş
sağlarlar (Tablo 1: Roitt, Immunology, 5th Ed’den adapte
edilmiştir).
|
|
ANAHTAR KELİMELER
Kalıtsal savunmalar
Uyarılan savunmalar
Interferon
2'5' Oligo A sentetaz
IFN-aktive protein kinaz
Intrinsik antiviral aktivite
Dışsal antiviral aktivite
ADCC
Immun bağlılık
NK hücreleri
CTL
|
|
Tablo 1 |
|
Virus |
Reseptör |
Infekte Hücre Tipi |
|
HIV |
CD4 |
TH
hücre |
|
Epstein-Barr virus |
CR2 (kompleman reseptor tip 2) |
B hücre |
|
Influenza A |
Glikoforin A |
Birkaç hücre tipi |
|
Rhino virus |
ICAM-1 |
Birkaç hücre tipi |
Virüsün konağa erişimi bu reseptörlerin
varlığına bağlıdır. Bu nedenle eğer bir virüs için konakta
reseptör eksikse veya bir virüsün replikasyonu için konak
hücrede bazı gerekli komponentler yoksa, konak kalıtsal olarak
virüse dirençlidir. Örneğin, farelerde polio virüsleri için
reseptörler eksiktir ve bu nedenle polio virüse dirençlidir.
Benzer şekilde, insanlar bitki ve çok sayıda hayvansal virüslere
karşı dirençlidir.
Mukus
Mukus, konak hücrelerin enfekte olmasını önlemek için epitel
dokuyu kaplayan bir bariyer görevi görür. Bazı durumlarda mukus
yalnızca bir bariyer olarak görev yapar ancak diğer durumlarda,
hücrelerde virüs reseptörleri ile mücadale ederek enfeksiyonu
önleyebilir. Örneğin, orthomikso-ve paramikso virüs aileleri
sialik asit reseptörlerine bağlanarak konak hücreleri enfekte
etmektedir. Mukustaki sialik asit- içeren glikoproteinler
böylece hücre reseptörleri ile rekabet edebilir ve virüsün
hücrelere bağlanmasını önler ya da bağlanmayı zayıflatır.
Silialı epitel
Mukosiliyer elevatörü hareket ettiren silli epitel bazı
virüslerin enfeksitivitesini azaltmaya yardımcı olur. Bu
sistemin aktivitesi, enfeksiyon veya ilaçlarla inhibe
edildiğinde virüsün belirli inokulumu ile artan bir enfeksiyon
oranı olduğundan bu sistemin solunum yolu enfeksiyonlarında
önemli olduğu gösterilmiştir.
Düşük pH
Mide salgılarının düşük pH’sı çoğu virüsü inaktive eder. Ancak,
Enterovirüsler mide salgılarına dayanıklıdır ve bu nedenle
bağırsakta hayatta kalıp replike olabilir.
Humoral ve hücresel
komponentler
Aşağıya bakınız
|
| |
Uyarılan
Bariyerler
Enfeksiyona tepki olarak konakta meydana gelen
değişiklikler ayrıca virüsün enfektivitesini azaltmaya da yardımcı
olabilir.
Ateş
Ateş diğer immün savunmaları güçlendirerek virüs replikasyonunu
azaltarak virüs replikasyonunu inhibe etmeye yardımcı olabilir.
37 C nin üzerindeki sıcaklıklarda bazı virüslerin replikasyonu
azalır.
Düşük pH
İnflamatuar infiltratların pH’sı da düşüktür ve virüsleri
inaktive ederek viral enfeksiyonların sınırlandırılmasına
yardımcı olabilir.
Humoral ve hücresel
komponentler
Aşağıya bakınız
VIRAL İNFEKSİYONA
KARŞI DİRENÇTE HUMORAL KOMPONENTLER
Nonspesifik
Viral enfeksiyonlara dirençte, non-spesifik immün
sistem fonksiyonunun bir dizi humoral bileşenleri bazıları yapısal
olarak bulunurken, diğerleri enfeksiyonla uyarılır.
Interferon (IFN)
IFN, virüsle enfekte olmuş hücrelerden elde edilen süpernatant
fraksiyonlarında diğer hücrelere enfeksiyona karşı direnç
kazandıran bir protein içerdiğini göstermiş olan Issacs ve
Lindemann tarafından 40 yıl önce keşfedilmiştir. Bu madde, virüs
üzerinde doğrudan etki etmek yerine hücreler üzerinde etki
göstererek onları enfeksiyona karşı dirençli hale getirir (Şekil
1).
|
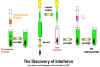 Şekil 1.\ Interferonun keşfi
Şekil 1.\ Interferonun keşfi
 Şekil 2 Akut viral enfeksiyona tipik cevap
Şekil 2 Akut viral enfeksiyona tipik cevap |
IFN, virüslere karşı ilk savunma hattından biridir çünkü
diğer herhangi bir savunma mekanizması ortaya çıkmadan önce
virüs enfeksiyonu sonrası erken uyarılır ( örn: antikor, Tc
hücreleri v.b) (Şekil 2). Bundan sonra hangi IFN’ nin yapılmaya
başlanacağı virüsün dozuna bağlıdır.
a) Interferonların Tip ve Özellikleri
Tablo 2;: Murray, Medical Microbiology, 5th Ed. Tablo
14-3’den adapte edilmiştir)
|
Tablo 2
Interferon Tip ve Özellikleri |
|
|
Interferon |
|
Özellik |
Alfa |
Beta |
Gama |
|
Önceki tanımlamaları |
Lökosit IFN
Tip I |
Fibroblast IFN
Tip I |
Immun IFN
Tip II |
|
Gen |
>20 |
1 |
1 |
|
pH2 duyarlılık |
Stabil |
Stabil |
Labil |
|
Uyarıcılar |
Virus (RNA>DNA)
dsRNA |
Virus (RNA>DNA)
dsRNA |
Antijen, Mitojen |
|
Esas kaynak |
Lökosit, Epitel |
Fibroblast |
Lenfosit |
İnterferonun 3 tipi vardır; IFN-alfa( aynı
zamanda lökosit interferon olarak da bilinir), IFN-beta(
aynı zamanda fibroblast interferon olarak da bilinir) ve
IFN-gama( aynı zamanda immün interferon olarak da bilinir.
IFN-alfa ve IFN-beta aynı zamanda Tip I interferon ve
IFN-gama ise Tip II olarak da adlandırılır. IFN-alfa’ nın
yaklaşık 20 alttipi vardır fakat sadece tek bir IFN-beta ve
IFN-gama bulunur.
IFN’lar arasında ayrım yapmak için
kullanılabilen farklı özellikleri vardır ( örn: pH
stabilitesi ve SDS’ nin varlığında aktive olma) fakat hali
hazırda onlar interferonlara özgü antikorlar kullanılarak
belirlenmiştir.
b) İnterferonların Uyarıcıları - Normal hücreler öncül IFN
de yapısal olarak gizli interferon da içermez. Bunun nedeni,
normal hücrelerde interferon genlerinin transkribe
olmamasıdır. IFN genlerinin transkripsiyonu yalnızca
hücrelerin uygun bir uyarıcıya maruz kalması sonrası oluşur.
IFN-alfa ve IFN-beta’ nın uyarıcıları, virüs enfeksiyonu,
çift zincirli RNA [örn: poli inosinik; poli sitidilik asit;
(poli I: C). Virüsler arasında, poxvirüsler dışındaki DNA
virüsleri zayıf IFN uyarıcılarıyken, RNA virüsleri en iyi
uyarıcıdır. IFN-gama uyarıcıları mitojen ve antijenleri (ör.
aktive lenfositleri) içerir.
|
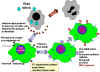 Şekil 3
Şekil 3
Interferon etki mekanizması |
c) İnterferonların Uyarılmasında Hücresel Olaylar
IFN genleri normal hücrelerde ifade olmaz çünkü hücreler
genin promotor bölgesi yakınlarına bağlanan bir değişken
represör protein ve transkripsiyonu inhibe eder. Buna ek
olarak, genlerin transkripsiyonu için promotor bölgeye
bağlanan ve transkripsiyonu etkinleştiren aktivatör
proteinler gerekir. IFN’ nin uyarıcıları ya represör
proteinin sentezini engelleyerek ya da aktivatör
proteinlerin seviyelerini arttırarak etki gösterir
böylelikle IFN genini etkinleştirir. Uyarıcı gittikten sonra,
IFN geni aktivatör proteinlerin eksikliği ve / veya represör
protein tarafından tekrar etkinliğini yitirir. Gen
etkinleştikten sonra transkribe olur, mRNA translate olur ve
hücreden protein salgılanır. IFN, komşu hücreler üzerindeki
IFN-reseptörlerine bağlanır ve 2. Hücrede antiviral bir
duruma neden olur (Şekil 3).
|
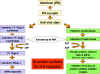 Şekil 4
Şekil 4
Antiviral durumun moleküler temeli |
d) İnterferonların Aktivasyonunda Hücresel Olaylar - IFN’
nin IFN-reseptörüne bağlanması sonucunda hücrede viral
replikasyonu önlemede rol oynayan antiviral proteinleri
kodlayan bir grup genin transkripsiyonu olur. Sonuç olarak
hücre, antiviral proteinler bozulana kadar virüs
enfeksiyonunundan korur, bu birkaç günü alan bir işlemdir.
IFN’ ye maruz kalan hücrelerdeki antiviral durum, protein
sentezinin inhibisyonuna neden olan 2 enzimin
sentezlenmesinin sonucu olarak ortaya çıkar. Bir protein,
viral mRNA’ nın yapısını bozarak protein sentezini dolaylı,
viral mRNA’ nın uzamasını inhibe ederek ise doğrudan etkiler
(Şekil 4).
Bu protein 2'5' Oligo A sentaz adı verilen 2'- 5'
fosfodiester bağları içeren tek bir polimeri (2'5' Oligo A)
ATP’ ye dönüştüren bir enzimdir. Çift sarmallı RNA, bu
enzimin aktivitesi için gereklidir.2'5' Oligo A, viral mRNA’
nın yapısını bozan RNaz L’ yi aktive eder. İkinci protein
olan protein kinaz, çift sarmallı RNA’ nın varlığında,
otofosforile olur ve böylece aktive olur. Aktive edilmiş
protein kinaz, uzama faktörü eIF-2’ yi fosforile eder ve
inaktive eder. Bu iki IFN-kaynaklı enzimler protein
sentezini engelleyen etki gösterir. Enfekte hücre, konağın
protein sentezini inhibe etmesi sonucu ölür, enfeksiyon
durur. Üretilmeyen çift sarmallı RNA yı gerektiren iki
enzimin aktivasyonundan dolayı enfekte olmamış hücreler IFN
muamelesiyle yok edilmez. Bazı virüsler IFN’ nun antiviral
etkisini inhibe eden öneme sahiptir. Örneğin, Adenovirüsler
IFN’nin antiviral etkisini azaltarak çift sarmallı RNA
tarafından protein kinazın aktive olmasını önleyen bir RNA
üretir.
|
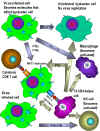 Şekil 5
Şekil 5
İnterferon alfa, beta ve gama'nın etkileri |
e) Interferonların Diğer Biolojik Aktivitileri - IFN,
yalnızca antiviral proteinlerin üretilmesini uyarmakla
kalmaz, aynı zamanda hücreler üzerinde başka etkilere de
sahiptir, viral enfeksiyondan kurtulma veya dolaylı olarak
konağa direnç yeteneği kazandırmaya katkıda bulunur (Şekil
5). IFN, sınıf I ve sınıf II MHC molekülleri üzerinde etki
göstererek immün yanıtları sağlamada yardımcı olabilir.
IFN-alfa, IFN-beta ve IFN-gama tüm hücrelerde MHC I
moleküllerinin ekspresyonunu arttırır böylece virüsle
enfekte hücreleri tahrip eden Tc hücreleri tarafından
tanınma artar. IFN-gama, aynı zamanda antijen sunan hücreler
üzerinde bulunan MHC II moleküllerinin ekspresyonunu
arttırır, viral antijenlerin CD4+ T yardımcı hücrelerine
daha iyi sunulmasını sağlar. Ayrıca, IFN-gama virüsle
enfekte olan hücreleri öldürebilen NK hücrelerini aktive
edebilir İntrinsik antiviral aktivite, virüsle enfeksiyonda
makrofajlara direnç kazandırır ve ekstrinsik antiviral
aktivite, makrofajlara virüsle enfekte olan diğer hücreleri
yok etme yeteneği verir. IFN’ ler aynı zamanda bazı kanser
tedavilerinde, onları yararlı hale getiren anti-proliferatif
etkinliğe sahiptir.
|
| |
f) Interferonların Klinik Kullanımı - IFN’ ler belirli
sayıda viral ve diğer hastalıkların tedavisinde kullanılır (Tablo
3; Mims, Medical Microbiology, Fig 37.5’den adapte
edilmiştir)
|
Tablo 3
Interferonların Klinik Kullanımı |
|
Interferon |
Tedavide kullanım |
|
IFN-alfa, IFN-beta |
Hepatit B (kronik)
Hepatit C
Herpes zoster
Papilloma virus
Rhino virus (sadece profilaktik)
Siğil |
|
IFN-gama |
Lepramatöz lepra
Leishmanyazis
Toksoplasmozis
Kronik granulomatöz hastalık (CGD) |
|
| |
Ek olarak, IFN’ lerin antiprolifratif etkileri nedeniyle
çeşitli kanserlerin tedavisinde de kullanılmaktadır. (Tablo 4;
Zinsser, Microbiology, 20th Ed, Table 58.3’den adapte edilmiştir).
|
Tablo 4
Interferonların Kanser Tedavisinde Kullanımı |
|
Tumor |
Tam veya kısmi remisyon yüzdesi |
|
Hairy cell lösemi |
90 |
|
Kronik miyelositik lösemi |
90 |
|
T hücreli lenfoma |
53 |
|
Kaposi's sarkomu |
42 |
|
Endokrin pankreatik neoplazm |
30 |
|
Non-Hodgkin's lenfoma |
25 - 35 |
|
| |
Ancak, IFN tedavisinin yan etkileri klinik tıpta rutin
kullanımı sınırlandırmaktadır (Table 5; Mims, Medical
Microbiology, Fig. 37.6’dan adapte edilmiştir).
|
Tablo 5
Interferonların Sık Görülen Yan Etkileri |
|
Interferon |
Ateş
Halsizlik
Yorgunluk
Kas ağrısı
Toksik etkileri:
böbrek
karaciğer
kemik iliği
kalp |
|
| |
Kompleman
Çoğu virüs alternatif yollarla kompleman fiksasyonu yapamaz.
Fakat virüsle enfekte olan bir hücreyle ya da zarflı bir virüs
ile kompleman-sabitleyici antikorun etkileşimi virüs veya
hücrenin lizisine yol açabilir. Dolayısıyla kompleman spesifik
immün sistemle ara bağlantı oluşturarak da viral enfeksiyonlara
karşı dirençte önemli rol oynar.
Sitokinler
IFN’ den başka sitokinler de virüs enfeksiyonuna karşı dirençte
önemli rol oynar. Tümör nekroz faktör alfa (TNF- α),
interlökin-1 (IL-1) ve IL-6 ‘nın invitro koşullarda antiviral
etkinliğe sahip olduğu gösterilmiştir. Bu sitokinler, aktive
olan makrofajlarla üretilir fakat invivo ortamda dirence
katkıları tam olarak aydınlatılmamıştır.
|
| |
Spesifik
Spesifik immün sistem tarafından üretilen antikorlar,
öncelikle viral enfeksiyonun iyileşmesini ve virüsle daha sonraki
karşılaşmalarda direnç geliştirmeyi sağlar. IgG, IgM ve IgA
antikorları tüm virüs enfeksiyonlarına karşı bağışıklıkta önemli rol
oynayabilir fakat farklı sınıfların nispi katkıları, virüse ve giriş
kapısına bağlıdır. Örneğin, IgG antikorları belirgin bir özelliği
olan viremi enfeksiyonlarında önemli iken, IgA mukozayı enfekte eden
virüslerde önemlidir. Antikorlar konak için hem yararlı hem de
zararlı etkiye sahiptir.
Yararlı etkiler
(Tablo 6; Roitt, Immunology 5th Ed., Fig 16.5’den adapte
edilmiştir)
Antikor, konak hücreler üzerindeki reseptörlere virüsün
bağlanmasını önleyerek ya da hücre içine virüsün girişini
engelleyerek doğrudan virüsün enfektivitesini nötralize eder.
Antikorlar, kılıfsızlaşmaya yol açan viral proteinlerin
etkileşimine müdahale ederek virüs kılıfının çıkarılmasını
önleyebilir. Kompleman-sabitleyici antikorlar, zarflı virüslerin
veya enfekte olan hücrelerin parçalanmasına yardımcı olabilir.
Antikorlar opsoninler olarak da etki gösterebilir ya Fc veya C3b
reseptörleriyle virüsü tanımayı kolaylaştırarak virüsün
fagositozunu arttırır ya da virüs aglütinasyonu ile onların daha
kolay fagosite olmasını sağlar. Antikor kaplanmış virüsle
enfekte hücreler, enfeksiyonun yayılmasını önleyen K hücreleri
tarafından öldürülebilir.
|
Tablo 6
Antikorların Antiviral Etkileri |
|
Hedef |
Ajan |
Mekanizma |
|
Serbest virus |
Antikor |
Hücreye bağlanmayı engeller Hücreye
girişi engeller Virusun soyulmasını bloklar |
|
Antikor + Kompleman |
Virus zarfını hasarlar
Virusun opsonizasyonu |
|
Virus-infekte hücre |
Antikor + Kompleman |
İnfekte hücrenin lizisi
İnfekte hücrenin opsonizasyonu |
|
Infekte Hücreye Antikor Bağlanması |
K, NK hücreler ve/veya makrofajlarca
ADCC |
Zararlı etkiler
a) Immunopatolojik hasar - Kompleman fiksasyonu, immün
kompleksler tarafından vazoaktif aminlerin salınması,
inflamatuar hücrelerin iyileştirilmesi ve konak dokuya hasar
sonrasında oluşabilir. Lenfositik koryomenenjit virüsü gibi bazı
virüsler, dolaşımda vasküler yataklarda ve doku hasarına yol
açan kompleman fikse ettikleri böbreklerde immün kompleksin
büyük bir kısmını üretir. Bu hasarlara neden olan virüslerin
diğer örnekleri: kızamık, solunum sinsityal virüs, dang ve serum
hepatit virüsü.
b) Immun bağlılık - Antikorlar tarafından
virüslerin opsonizasyonu, fagositik hücrelerle onların
tanınmasını kolaylaştırır. Eğer virüs fagositte yaşarsa, virus
enfeksiyonunun yayılmasına izin verilir. Dang ve HIV
makrofajlarda yaşayabilen virusa örneklerdir.
Seroloji
Virüslerin izolasyonu ve identifikasyonundan beri klinik
laboratuvarlarda kullanımı yaygın olmayan klinik tablo ve
seroloji, viral hastalıkların tanısında daha büyük rol oynar.
Antikorların başlıca tipleri olan; nötralize eden,
hemaglütinasyonu inhibe eden ve kompleman fikse eden antikorlar
için çalışılır. Kompleman fikse eden antikorlar, IgM’ in
hareketlerini takip eden ve şimdiki ya da yeni enfeksiyonu
gösteren en yararlı antikorlardır. Buna karşılık, nötralize eden
ve hemaglütine edici antikorlar IgM’ in hareketlerini takip eder
uzun bir süre devam eden ve bağışıklık değerlendirmede
kullanılan antikorlardır. Virüsün farklı bileşenlerine karşı
antikor gelişimi, hastalık göstergesi olarak kullanılır. Örneğin;
Hepatit B ve HIV enfeksiyonlarında bu yaklaşım kullanılır.
|
| |
HÜCRESEL KOMPONENTLER
Bariyerler ve viral enfeksiyonun iyileşmesiyle virüse karşı direnç
kazanmayı sağlayan humoral bileşenlere ek olarak, bizim antiviral
savunmamızda rol oynayan birkaç farklı hücre vardır.
Nonspesifik
Makrofajlar
Makrofajlar, vücudun çeşitli bölgelerinde yerleşimi sayesinde
virüslerle karşılaşan ilk hücrelerden biridir. Deneysel kanıtlar,
bu hücrelerin viral enfeksiyona karşı dirençte önemli rol
oynadığını ileri sürmüştür. Örneğin; yeni doğan farelerde
virüsün çoğalmasını önleyen makrofajların işlevindeki bir
bozukluk nedeniyle herpes virüs tip 1’ le enfeksiyona karşı
duyarlıdır. Fakat yetişkin farelerdeki makrofajlar, virüsün
çoğalmasını önleyebilir ve bu fareler bu virüsle enfeksiyona
karşı dirençlidir. Aynı zamanda, makrofajları tükenen
hayvanlarda herhangi bir virüsle enfeksiyona daha duyarlıdır.
Makrofajlar bir dizi yolla antiviral savunmaya katkı sağlar.
a) Intrinsik antiviral aktivite - Makrofajlar virüslerle
enfekte olabilir fakat birçok virüs, makrofajlarda verimsiz
olarak çoğalır. Makrofajlar (örn; IFN- γ tarafından) viral
replikasyona karşı dirençte daha verimli dengeli olarak
etkinleşirler. Böylece makrofajlar, virüslerin çoğalmasını
önleyen intrinsik(içsel) yeteneğe sahip olmasıyla viral
enfeksiyonları sınırlamaya yardım eder. Ancak bazı virüsler
replike olabilir ya da en azından makrofajlarda hayatta
kalabilir ve böylece makrofajlar tarafından yayılabilir (Aşağıya
bakınız).
b) Dışsal antiviral aktivite - Makrofajlar ayrıca virüsle
enfekte olan hücreleri tanıyıp onları öldürebilir. Böylece,
makrofajlar sitotoksik işlevleri sayesinde antiviral
savunmaya katkıda bulunur.
c) ADCC - IgG antikorları ile kaplanmış virüsle enfekte
enfekte hücreler ADCC tarafından makrofajlarla öldürülebilir
d) IFN üretimi - IFN’ nin kaynağı makrofajlardır.
NK Hücreler
Deneysel kanıtlar, NK hücrelerinin de viral enfeksiyona karşı
dirençte rol oynadığını düşündürmektedir. NK hücreleri tükenmiş
olan fareler, bazı virüslerle enfeksiyona daha duyarlıdır.
Ayrıca, düşük NK hücre aktivitesine sahip olan hastalar herpes
simplex tip1 virüsü ile tekrar eden durumlara karşı daha
duyarlıdır. NK hücreleri, virüsle enfekte olan hücreleri
tanıyarak ve yok ederek etki gösterir. Virüsle enfekte olan
hücreler, MHC ile sınırlandırılmamış ya da spesifik bir antijen
olamayan hücreler olarak tanınır. Böylece, NK hücreleri birçok
farklı virüsle enfekte olan hücreleri öldürür. NK hücreleri aynı
zamanda ADCC’ ye aracılık edebilir ve bu mekanizma sayesinde
virüsle enfekte olan hücreleri yok edebilir. NK hücrelerinin
aktiviteleri, IFN-γ ve IL-2 ile arttırılabilir (aşağıya bakınız).
|
| |
Spesifik
T Hücreler
Thücreleri, viral enfeksiyonların iyileşmesinde önemli rol oynar.
Enfekte hücreler üzerindeki viral antijenlere yanıt olarak
üretilen sitotoksik T hücreleri(CTL’ ler), enfekte hücreleri
öldürerek enfeksiyonun yayılmasını önler. T helper hücreleri,
CTL’ lerin üretimini sağlar ve antikor yapımı için B hücrelerine
yardım eder. Ek olarak, T hücreleri tarafından salgılanan
lenfokinler bir araya toplanır, makrofajlar ve NK hücreleri
aktive olur böylece virüse karşı saldırıda ortak hareket
sağlanır.
|
| |
SAVUNMANIN ÖZETİ
Tablo 7 (Baron, Medical Microbiology, 2nd Ed., Table
69-2’den adapte edilmiştir) viral enfeksiyonlara karşı konak savunmasını
özetler ve bu savunmanın her biri için hedefleri gösterir.
|
Tablo 7
Viral Infeksiyonlarda Konak Efektör İşlevleri
|
|
Konak Savunma |
Efektör |
Efektin hedefi |
|
Erken nonspesifik cevap |
Ateş
Fagositoz
Inflamasyon
NK hücre aktivitesi
Interferon
|
Virus replikasyonu
Virus
Virus replikasyonu
Virus-infekte hücre
Virus replikasyonu, immunomodulasyon
|
|
Hücrelerle ilişkili immun cevap |
Sitotoksik T lenfosit
Aktive makrofaj
Lenfokin
ADCC
|
Virus infekte hücre
Virus, virus-infekte hücre
Virus-infekte hücre, immunomodulasyon
Virus-infekte hücre
|
|
Humoral immun cevap |
Antikor
Antikor + kompleman
|
Virus, Virus-infekte hücre
Virus, Virus-infekte hücre
|
KONAK SAVUNMA
MEKANİZMASININ RÖLATİF KATKILARI
Çeşitli konak savunma mekanizmalarının göreceli olarak
katkısı; virüsün yapısına ve giriş kapısına bağlıdır. Antikorlar viremi
gibi belirgin bir özelliği olan enfeksiyonlarda daha önemli olacaktır.
Fakat, antikorlar hücre füzyonuyla hücreden hücreye geçebilen virüs olan
herpes veya paramiksovirüslerle enfeksiyonda yararlı olmayabilir. Bu
durumda hücre-aracılı immünite daha önemlidir. Eğer bir virüs yalnızca
mokozal yüzeydeki hücreleri enfekte ediyorsa, IgA antikorlar önemli
olabilir.
Konak savunma mekanizmalarının anlaşılması, aşı gelişimi
ve aşıların tam olarak uygulanması için önemlidir. IgA antikorları
belirli bir virüse karşı korumada önemliyse, uygun mukozal yüzeyde IgA
antikor üretimini stimüle eden herhangi bir aşı mümkün olmalıdır.
Alternatif olarak, eğer CTL’ ler önemliyse o halde CTL üretimini uyaran
aşı gereklidir. Canlı aşılar ölü aşılara göre daha fazla tercih
edilmesinin nedeni, ölü aşılar yapamazken canlı aşılar genellikle CTL’
lerin üretimine öncülük ederler.
|
| |
VIRUS-KAYNAKLI
IMMUNOPATOLOJİ
Konak, viral enfeksiyonlara karşı korumak için çeşitli
savunma mekanizmalarına sahip olmasına rağmen, bazı durumlarda doku
hasarı sebebiyle doğrudan enfeksiyona karşı immün yanıt oluşturur.
Örneğin; sitomegalovirüs ile enfekte olan bebeklerin artrit ve
glomerular nefrit gibi patolojik bir durumla sonuçlanan eklemler ve
böbreklere yerleşmiş sirkülasyon halinde immün kompleksleri vardır. Bir
başka örnek; Dang virüs enfeksiyonu ile ilişkili ölümcül hemorojik şok
sendromu. Bu durum; ani artan vasküler geçirgenliğe, şok ve ölüme yol
açan kompleman kaskatının ürünlerinin serbest kalması sonucu,
dolaşımdaki immün kompleksleriyle komplemanın fiksasyonudur.
IMMUNOSUPRESYON
Birçok virüs, bağışık yanıtları baskılayabilir ve
böylece konak savunmasını atlatır ya da en aza indirir. En iyi örnek:
HIV, CD4+ hücrelerini enfekte eder böylece spesifik immün sistemi yıkıma
uğratır. Diğer virüsler (örneğin; kızamık virüsü) aynı zamanda
lenfositleri enfekte edebilir ve lenfositlerin çoğalma ve
farklılaşmalarını etkileyebilir. Virüs-kaynaklı immünsupresyon, aşı
gelişiminde önemli bir husustur. Tablo 8’ de konak savunmasından
kaçabilen virüslerin bazı mekanizmaları örneklerle açıklanmıştır (Roitt,
Immunology 5th Ed., Fig 16.10’den adapte edilmiştir)
|
Tablo 8
Konak Savunması ile İlişkili Viral Ürünler |
|
Etkilenen Konak Savunması |
Virus |
Virus Ürünü |
Mekanizma |
|
Interferon |
EBV |
EBERS (küçük RNAlar) |
Protein kinaz aktivasyonunu engeller |
|
Vaccinia |
eIF-2alpha homolog |
Protein kinaz tarafından eIF2alfa
fosforilasyonunu önler |
|
Kompleman |
Vaccinia |
Kompleman kontrol proteinlerin homologları |
Kompleman aktivasyonunu bloklar |
|
Antikor |
HSV-1 |
gE/gI |
Fc gama bağlanır ve fonksiyonu bloklar |
|
Sitokin |
Myxoma |
IFN-gama reseptor homolog |
IFN-gama için yarışır ve fonksiyonu bloklar |
|
Shope fibroma virus |
TNF reseptor |
TNF için yarışır ve fonksiyonu bloklar |
|
EBV |
IL-10 homologu |
IFN-gama fonksiyonunu azaltır |
|
MHC Klas I |
CMV |
Early protein |
Peptid-yüklenmiş MHC taşınmasını önler |
|
Adenovirus |
E3 |
MHC'nin yüzeye taşınmasını bloklar |
|
Apoptoz |
Adenovirus |
14.7K |
Inhibits capsases |
|
EBV |
Bcl-2 homologu |
Anti-apoptotik |
|
NK hücre |
HCMV |
UL-18 |
MHC homologu NK hücrelerini inhibe eder |
|
|
|
 Mikrobiyoloji ve İmmünoloji On-line, Viroloji Bölümüne Dönünüz
Mikrobiyoloji ve İmmünoloji On-line, Viroloji Bölümüne Dönünüz
This page last changed on
Saturday, October 29, 2016
Page maintained by
Richard Hunt
|

 Şekil 1.\ Interferonun keşfi
Şekil 1.\ Interferonun keşfi Şekil 3
Şekil 3 Şekil 4
Şekil 4 Şekil 5
Şekil 5
