|
x |
x |
|
 |
 |
|
INFECTIOUS
DISEASE |
BAKTERIYOLOJİ |
İMMÜNOLOJİ |
MYCOLOGY |
PARASITOLOGY |
VİROLOJİ |
|
RNA tümör virüsleri ayrı bir sayfaya taşındı
İzleyin Sonraki aşağıda
|
VIROLOJİ
- BÖLÜM ALTI
KISIM BİR
ONKOJENIK VIRUSLAR
DNA Tümör Virusları
Dr Richard Hunt
Professor
Department of Pathology, Microbiology and Immunology
University of South Carolina School of Medicine
Çeviren. Prof. Dr.
Selçuk Kaya
İzmir Katip Çelebi Üniversitesi, Tıp Fakültesi
|
|
|
|
EN
FRANCAIS |
|
En
Español |
|
NË SHQIPTARE |
|
ENGLISH |
|
Let us know what you think
FEEDBACK |
|
SEARCH |
|

 |
|
|
|
|
|
ÖĞRETİM HEDEFLERİ
İnsanlarda kansere neden olan virusları öğrenmek
Virüs tarafından hücrenin nasıl transforme edildiğini öğrenmek
DNA ve RNA tumor virusleri arsındaki farkları öğrenmek
Hücre transformasyonuna RNA viral onkogenezin nasıl sonuçlandırdğını
anlama
|
Kanserler, hücre proliferasyonunun normal sınırlarının bozulması sonucu
oluşur. Bu tip bozulmaların oluşabileceği yolak sayısının oldukça
sınırlı olduğu açıktır ve mutasyon veya diğer bazı ekspresyon
bozukluklarının sınırsız hücre büyümesine neden olduğu en az kırk tane
hücresel gen bulunabilir.
Değişmiş olan ekspresyonun büyüme kontrolünün
kaybına yol açtığı iki sınıf gen vardır:
- Büyüme için uyarıcı olup hiperaktif
hale geldiğinde kansere sebep olan genlerdir. Bu genlerdeki
mutasyonlar baskın olacaktır. Bu genlere onkogenler denir.
- Hücre büyümesini inhibe edip
durdurulduklarında kansere sebep olan genler. Bu genlerdeki
mutasyonlar çekinik olacaktır. Bunlar anti-onkogenler veya tümör
baskılayıcı genlerdir.
Virüsler kanserde yer alırlar çünkü bu genlerin bir kopyasını
taşıyabilirler ya da hücrede bu gen kopyalarından bir tanesinin
ekspresyonunu değiştirebilirler. Bunlar onkogenik virüslerdir (diğer
bir deyişle onkovirüsler veya tümör virüsleridir).
|
|
Hücresel proto-onkogenlerin keşfini
anlamak
Hücresel onkogenlerin virusun yokluğunda nasıl kanser yapabildiğini
öğrenmek
Anti-onkogenlerin keşfinine yol açan keşiflerin nasıl olduğunu öğrenmek
Anti-onkogenlerin keşfininin nasıl olduğunu anlamak DNA virusları nasıl
kansere neden olur göstermek
|
TÜMÖR VİRÜSLERİNİN SINIFLARI
Tümör virüslerinin iki sınıfı vardır:
- DNA tümör virüsleri
- RNA tümör virüsleri, bu aynı zamanda RETROVİRÜSLER olarak
adlandırılmaktadır
Bu iki sınıfın kendilerini eşlemek için çok farklı yolları olduğunu
görmekteyiz ancak yaşam döngülerinde bir tek ortak noktaları bulunmaktadır:
kendi genomlarını konak hücreye entegre edebilme yeteneğidir. Ancak bu tip bir
entegrasyon tümör oluşumu için bir önkoşul değildir.
TRANSFORMASYON VE ONKOGENLER
Eğer bir virüs bir hücreyi konak olarak seçerse ve o hücrenin özelliklerini
değiştirirse o hücreye transforme hücre denir. Bir virüs tarafından gerçekleşen
transformasyon bir hücrenin biyolojik özelliklerinin değişimidir. Bu, hücrenin
viral genler tarafından kontrol edilmesiyle oluşur ve enfekte hücrelerde
neoplazinin belirli özellikleri görülür.
Transformasyon sıklıkla büyüme kontrolünün kaybını, ankoraj-bağımsız büyümeyi,
ekstraselüler matrikse geçebilme yeteneğini, dediferensiyasyonu ve
ölümsüzleştirilmeyi içerir. Karsinomalarda birçok epitel hücre
epitelyal-mezenkimal transformasyon geçirir. Transforme olan hücreler genellikle
kromozomal anormallikleri ve genelde transformasyonda görülen değişimleri
gösterir. Ancak her zaman olmamakla birlikte viral genomun konak hücre
kromozomuna entegrasyonu sonucu oluşur.
Tümöre sebep olabilen viral genom bölgesi (DNA tümör virüslerinde DNA veya
RNA-tümör virüslerinde RNA) onkogen olarak adlandırılır. Bu yabancı gen hücreye
virüsle taşınabilir ve konak hücrenin yeni özelliklere sahip olmasına neden
olabilir.
Retrovirüslerde viral onkogenlerin keşfi bunların sadece virüslere ait
olmadığını ve homolog genlerin (proto-onkogen denir) bütün hücrelerde
bulunduğunu göstermiştir. Hatta, virüs kendi evrimi esnasında bir hücresel geni
alır ve bunu takiben bu gen değişmiş olur. Normalde, hücresel proto-onkogenler
pasif hücrelerde eksprese edilmez çünkü bunlar büyüme (vücut hücrelerinin
çoğunda oluşmaz) ve gelişimde yer almazlar veya hücrenin sıkı kontrolü altında
eksprese edilirler. Ancak, viral onkogen taşımayan hücre tümör virüsleri
tarafından enfekte hale geldiğinde bu genler anormal bir şekilde eksprese edilir
hale gelebilir. Bunun nasıl gerçekleştiğini daha sonra göreceğiz ancak bir
virüsün iki yolla kansere sebep olabileceği açıktır: bir onkogeni hücreye
taşıyabilir veya hücresel proto-onkogeni aktive edebilir.
Hücresel onkogenlerin keşfi non-viral uyarılmış kanserlere sebep olabilen
mekanizmaların açığa çıkarılmasına yol açmıştır. Enfekte hücrelerde ve hücresel
proto-onkogenlerin eksprese edildiği hücrelerde viral ve hücresel onkogenlerin
protein ürünlerinin ne olduğunu araştırmalıyız. Bunların fonksiyonlarının
hücrelerin neoplastik fenotipe transforme edilebildiği mekanizmaları güçlü bir
şekilde öne sürdüğünü görmeliyiz. Hücresel onkogenlerin keşfi hücresel genlerin
tümör represör (baskılayıcı) genler veya anti-onkogenler adı veirlen farklı bir
sınıfının keşfine sebep olmuştur.
İlk olarak retrovirüsler tarafından oluşmuş viral ve hücresel onkogenlerin
yer alması DNA tümör virüs onkogenlerinin yer almasından çok daha açıktır ancak
tümör represör genlerinin keşfi (retrovirüslerin nasıl kansere yol açtığına
ilişkin bilgimize dayanarak) DNA virüs onkogenlerinin aktivitesinin
aydınlatılmasına sebep olmuştur.
Retrovirüslerin onkogenez mekanizmasının aydınlatılmasında aracı olmasına
rağmen çoğu insan kanserleri, retrovirüsler bazı hayvan kanserlerinde önemli
olmasına rağmen, muhtemelen retroviral enfeksiyondan kaynaklanmamaktadır. Birçok
insan tümörünün DNA tümör virüsleriyle enfeksiyonda kaynaklanabileceği çok daha
açık hale gelmektedir.
|
 Şekil 1
Şekil 1
DNA tümör virüslerinde bilgi akışı ökaryotik hücrelerde benzerdir |
| Şekil 2
Papilloma virus
Copyright 1994 Veterinary Sciences Division, Queens
University Belfast |
DNA TUMOR VIRUSLARI
DNA tümör virüsü RNA’ya transkribe olup sonradan proteine transle
olan bir DNA genomu içerir (Şekil 1). İki türlü yaşam ömürleri vardır:
- Serbest hücrelerde viral genomun bütün kısımları eksprese edilir.
Bu, viral replikasyona, hücre lizisine ve hücre ölümüne sebep olur
- Replikasyon için serbest olmayan hücrelerde viral DNA her zaman
olmamakla birlikte genelde hücre kromozomunun bazı bölgelerine
rastgele olarak entegre olurlar. Viral genomun sadece bir kısmı
eksprese edilir. Bu, virüsün erken kontrol fonksiyonlarıdır (örneğin;
T antijenleri). Viral yapısal proteinler yapılmaz ve çoğalan
virüsler salınmazlar.
|
|

Papilloma virus
Copyright Dr Linda M Stannard, 1995 (used with
permission)
Papilloma virus bilgisayarda renklendirilmiş EM görüntüsü. Tüm72
kapsomerin esas yapısal proteini pentamerlerdir.
Copyright Dr Linda M Stannard, 1995 (used with
permission)
Şekil 3A

Perine anal bölgede zührevi siğiller. Kondiloma acuminata, ya da genital
siğiller, Human Papilloma Virus (HPV)'un neden olduğu cinsel yolla
bulaşan bir hastalıktır
CDC
|
İNSAN KANSERLERİNDE YER ALAN DNA TÜMÖR
VİRÜSLERİ
İlk keşfedilen DNA tümör virüsleri tavşan fibroma virüsü ve Shope
papilloma virüsüdür. Her ikisi de Richard Shope tarafından 1930’da
keşfedilmiştir. Papillomalar siğiller gibi epitelyal hücrelerin benign
büyümesidir. Bunlar vahşi bir tavşandaki tümörden ekstrakte edilip başka
bir tavşana enjekte edilmesi ve bu tavşanda da benign papilloma
büyümesinin gözlenmesiyle keşfedilmiştir. Ancak, bu filtrat evcil
tavşana enjekte edildiğinde sonuç karsinoma oluşmuştur. Bu da malign bir
büyümedir. Bu etkileyici gözlem malign bir büyümeden enfeksiyöz virüs
izole etme olasılığının daha uzun süremeceğini göstermiştir. Çünkü virüs
malign hücrelerin kromozomlarına entegre olmuştur.
KÜÇÜK DNA TUMOR VIRUSLARI
AİLE: PAPILLOMAVIRIDAE
PAPILLOMA VIRUSLAR
Papillomaviridae ailesi önceleri Papovaviridae ailesinde (isimlendirme
şu şekildedir: Pa: papilloma; Po: polyoma; Va: vacuolating) yer
alan Polyomaviridae içerisinde sınıflandırılmaktaydı. Bu terim
artık kullanılmamaktadır. Papilloma ve polyoma günümüzde farklı
aileler olarak kabul edilmektedir.
Papillomaviridae küçük, zarfsız ikozahedral DNA virüsleridir
(şekil 2). Temel kapsid proteini olan L1 72 pentamerden (kapsomer)
oluşur. Bu protein ikozahedral kapsidin oluşması için gerekli
olan herşeydir ve kendi kendine birleşerek oluşur. Her bir
pentamer diğer minör kapsid protein molekülleri olan L2 ve L3
ile ilişkilidir. Papilloma virüsleri yaklaşık 8 kilobazlık genom
büyüklüğüne sahiptirler ve DNA konak hücre tarafından kodlanan
histon proteinleriyle kompleks halindedir.
Bu virüsler siğillere (şekil 3A) ve aynı zamanda insan ve hayvan
kanserlerine sebep olurlar. Siğiller genellikle tehlikeli
değildir ancak tehlikeli karsinomalara dönüşebilirler. Bu,
epidermodisplazi verruciformisli hastalarda görülmektedir (şekil
3B).
Epidermodisplazi verruciformis aynı zamanda Lewandowsky-Lutz
displazisi veya Lutz-Lewandowsky epidermodisplazi verruciformis
olarak da bilinmektedir ve çok nadirdir. Anormal, kontrolsüz
papilloma virüsünün replikasyonuna sebep olan otozomal resesif
bir mutasyondur. Bu, vücudun çeşitli bölgelerinde, özellikle de
ellerde ve ayaklarda pulsu leke ve papüllerin oluşmasına sebep
olur. Yüksek riskli deri karsinoması ile ilişkili olan
Epidermodisplazi verruciformis tipik olarak HPV tip 5 ve 8 ile
ilişkilidir (diğer tipler de yer alabilir). Bunlar çoğu insanı
enfekte eder (popülasyonu %80’i) ve genellikle asemptomatiktir.
Papilloma virüsleri aynı zamanda insan penil, rahim, servikal
ve anal karsinomaları ile de ilişkili bulunmuştur ve bu
hastalıkların sebebi olmaları çok muhtemeldir. Hatta, genital
siğiller karsinomalara dönüşebilirler.
Larinkste, özofagusta ve akciğerde squamöz hücre karsinoması
histolojik açıdan servikal karsinomaya oldukça benzemektedir ve
bunlar da papilloma virüslerini içerebilir. Günümüzde, belirli
oral-faringeal kanserlerle HPV16 arasında güçlü bir sebep
ilişkisi olduğu ortaya konmuştur.
100’den fazla insan papilloma virüs tipi bulunmaktadır ancak
hepsi kanserlerle ilişkili değildir. Ayrıca, papillomalar dünya
çapında kadınlarda görülen kanserlerin %16’sına ve bütün
kanserlerin %10’una sebep olabilirler.
|
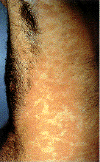 Epidermodysplasia verruciformis. Bu yaygın, belirgin kaşıntılı,
eritematoz döküntülü. İnsan papillomavirus infeksiyonu kaynaklı olduğu
bulundu.
Epidermodysplasia verruciformis. Bu yaygın, belirgin kaşıntılı,
eritematoz döküntülü. İnsan papillomavirus infeksiyonu kaynaklı olduğu
bulundu.
International Association of Physicians in AIDS Care

Epidermodysplasia verruciformis:Elin dorsal tarfında
hiperkeratotik siğil lezyonu
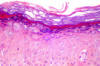
Epidermodysplasia verruciformis: Histopatolojik görüntü:
Epidermiste Koiliosit ve ılımlı displazi (H&E x100)
From: Reza Mahmoud Robati MD, Afsaneh Marefat MD, Marjan
Saeedi MD, Mohammad Rahmati-Roodsari MD, Zahra Asadi-Kani MD
Dermatology Online Journal 15 (4): 8, 2009 (used under Creative Commons
license)
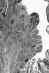 Şekil 3B
Şekil 3B
Verruköz karsinom. Epitel yüzey olgunlaşması, parakeratoz ve
hiperkeratoz gösterir. hücresel atipi az veya hiç yoktur. Stroma hafif
kronik inflamasyon gösterir.
The Johns Hopkins Autopsy Resource (JHAR) Image Archive
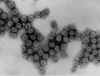 Şekil 4A
Şekil 4A
Polyomavirus SV40’ın Transmisyon elektron mikrografisi
Dr. Erskine Palmer CDC
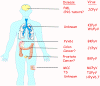 Şekil 4B
Şekil 4B
İnsan polyomaviruslar ve ilişkili hastalıkları.
Her insan polyomavirus doku tropizmi ve hastalıkları.
doi:10.1371/journal.ppat.1003206.g001
From: The Rapidly Expanding Family of Human Polyomaviruses: Recent
Developments in Understanding Their Life Cycle and Role in Human
Pathology. Martyn K. White, Jennifer Gordon and Kamel Khalili. PLOS
Pathogens. Used under Creative Commons License
|
Vulvar, penil ve servikal kanserler tip 16 ve 18 papilloma
virüsleriyle (ve diğerleri) ilişkilidir ancak en yaygın genital insan
papilloma virüsleri (HPV) tip 6 ve 11’dir. Tahmin edilebileceği gibi
belirli kanserlerin sebepleri iseler tip 16 ve 18 insan keratinositlerin
transformasyonuna sebep olur. Almanya’da yapılan bir çalışmada 30 HPV
tip 16 ile enfekte kadından 1 tanesinde malignant hastalık
geliştirecekken 500 enfekte insanda 1 kişide penil veya vulvar kanser
gelişeceği gösterilmiştir. Bütün enfekte kişiler kanser
geliştirmediğinden dolayı büyük olasılıkla hastalığı uyarıcı bazı
kofaktörler mevcuttur. Bu tip kofaktörler sığırda sindirim sistemi
karsinomasında saptanmıştır. Eğrelti otunu içeren beslenmesinin
hastalıkla ilişkili olduğu bulunmuştur. HIV enfeksiyonu ve AIDS olan
bireyler, diğer immün baskılayıcı formlarına sahip hastalar gibi HPV
ilişkili kanserler için yüksek risklidir.
Bir virüsün hastalıkla ilişkili olması (sıklıkla tümörlerde,
neoplastik hücrelerdeki viral genom kopyasının varlığı) o virüsün
kansere sebep olduğunu göstermez. İlişki neden olmaktan çok geçici
olabilir. Bütün bunlara rağmen birçok örnekte epidemiyolojik veriler
oldukça güçlüdür ve insan servikal kanserinde anti-HPV aşının etkinliği
HPV’nin servikal kansere yol açtığı tartışmasını zorlamaktadır.
AILE: POLYOMAVIRIDAE
POLYOMA VIRUSLAR
Polyomaviridae ailesi (şekil 4A) küçük, zarfsız ikozahedral DNA
virüsleridir (şekil 2). Temel kapsid proteini VP1’dir ve 72 pentamerden
oluşur. Her bir pentamer diğer minör kapsid proteini olan VP2 veya VP3
ile ilişkilidir. 5 kilobazlık bir genoma sahiptirler. Her partikül 40-50
nanometredir.
Günümüze kadar, sadece bir cins polyoma virüsü bulunmaktaydı. Ancak,
2010 yılında daha fazlası keşfedilmiştir. Tek cins üçe ayrılmıştır:
- Ortopolyomavirüs. Klasik memeli polyomavirüslerini kapsar (ör;
JCPyV, BKPyV, SV40, fare polyomavirüsü, vb.)
- Wukipolyomavirüs. Günümüzde keşfedilmiş insan
polyomavirüsleridir. Karolinska Enstitüsü polyomavirüsü (KIPyV) ve
Washington Üniversitesi polyomavirüsü (WUPyV)
- Avipolyomavirüs. Kuşlara ait polyomavirüslerini kapsar
Birçok polyoma virüsü insan hastalıklarıyla ilişkilidir (şekil 4b)
Fare (Murin) Polyoma virus
Polyoma virüsü bu şekilde isimlendirilmiştir çünkü birçok hayvan türünde
farklı birçok bölgelerde birçok tümöre sebep olur. İlk olarak AK
faresinden izole edilmiştir ve fare hücrelerinde replikasyon için
tamamen serbesttir. Fare ve hamsterlarda lösemilere sebep olmaktadır.
Simian virus 40
SV40 virüsü ilk olarak al yanaklı maymun karaciğer hücresinde
keşfedilmiş olup inaktif çocuk felci aşısı virüsü elde etmek için
kullanılmıştır. Bu hücrelerde inaktif virüs yapılıp Afrika Yeşil Maymunu
karaciğer hücresine verildiğinde, aşının sitopatik bir etki gösterdiği
bulunmuştur. Bu, aşı virüsünü inaktif hale getirmek için kullanılan
formalinle öldürülmemiş canlı virüsün varlığının göstergesidir. SV40 al
yanaklı maymun karaciğer hücresinde replike olur ancak bunların üzerinde
sitopatik etkiye sahip değildir. Çocuk felci aşısının ilk olarak
yapıldığı kişiler kontamine edici SV40 almışlardır çünkü kanlarında
anti-SV40 antikorları (büyük tümör antijenine (T-antijenine) karşı)
tespit edilebilirdi. Bu kişilerde yüksek kanser insidansı görülmemiştir.
SV40, konak hayvan üzerinde açıkça bir etkisi olmayan bir maymun
virüsü olmasına rağmen, yavru hamsterlara enjekte edildiğinde
sarkomalara sebep olur. Hamster tümör hücreleri enfektif virüs üretmez.
İnsan polyoma viruslar
İlk iki insan polyoma izolatları BK ve JC olarak bilinmekte olup 1971
yılında keşfedilmiştir. Hiçbirisi tümörden elde edilmemiştir. BK böbrek
nakli olmuş bir hastanın idrarından ve JC ilerleyici multifokal
lökoensefalopatiye (PML) giden Hodgkin’s lenfoma hastalarının beyninden
elde edilmiştir. Ancak, bunlar hayvanlara enjekte edildiğinde tümörlere
sebep olmaktadır. İnsan popülasyonunun %70-80’i JC için seropozitiftir.
Bu virüsün immünsüpresyonla ilişkili bir hastalık olan PML etkeni olduğu
bilinmektedir (yavaş viral hastalıklara bakınız). 1979’da bu hastalığın
oluşma oranı 10 milyonda 1.5 idi. AIDS yüzünden çok daha yaygın hale
geldi ve AIDS hastalarının %5’inde görülmektedir. BK virüsü ise
immünsüprese renal transplant alıcılarında nefropati ve graft kaybının
önemli bir sebebidir ve batı ülkelerinde neredeyse herkesin 10
yaşlarında anti-BK virüs antikoru bulunur. Günümüzde, BK viral DNA insan
prostat kanseriyle ilişkilidir.
Günümüzde diğer üç insan polyoma virüsleri de açıklanmıştır: KI, WU
ve Merkel hücre polyoma virüsü. En sondaki virüs nadir bir deri
kanserine sebep olur (Merkel ücre karsinoması, aşağıdaki kutucuğa
bakınız).
|
|
WEB KAYNAKLARI
Cutaneous
manifestations of human papilloma virus
Epidermodysplasia
verruciformis
E-medicine
Human papilloma vaccine
CDC |
|
Şekil
5

Adenovirus
Copyright
Dr Stephen
Fuller, 1998
Adenovirus
CDC
 Adenovirus
Copyright
Dr
Linda
M Stannard, University of Cape Town, South Africa, 1995
(used with permission). Adenovirus
Copyright
Dr
Linda
M Stannard, University of Cape Town, South Africa, 1995
(used with permission).
|
Polyoma virüsleri genellikle litiktir (lizise sebep olurlar) ve
transformasyon oluşması transfrome olan virüsün defektif olmasındandır.
Konak DNA’sına entegrasyondan sonra sadece erken fonksiyonları mRNA’ya
transkribe edilir ve protein ürün olarak eksprese edilir. Bunlar tümör
antijenleridir. Tümör antijenleri genlerinin ekspresyonu hücrelerin
transformasyonu için önemli olduğundan bunlar onkogenler olarak
sınıflandırılabilir.
BİR ONKOGENİN TANIMI: BİR ONKOGEN, NORMAL BİR HÜCREYİ MALİGNANT BİR
HÜCREYE DÖNÜŞTÜREBİLEN PROTEİNİ KODLAYAN GENDİR. BU GEN BİR VİRÜS
TARAFINDAN TAŞINDIĞINDA VİRAL ONKOGEN ADINI ALIR.
AILE: ADENOVIRIDAE
ADENOVIRUSLAR
Bu virüsler (şekil 5) 35 kilobazlık genom büyüklükleriyle bir şekilde
polyoma ve papilloma virüslerinden daha büyüktürler. İlk olarak insan
tonsilleri ve adenoidlerinden izole edilmiş olup insanlarda oldukça
onkogeniktirler ve virüsün sadece bi kısmı konak genomuna entegre olur.
Bu kısım, ilk fonksiyonları gerçekleştiren birçok T-antijeni kodlar.
Tümör taşıyan hayvanlar T antijenlerine karşı antikorlar oluşturur.
Hiçbir insan kanseri Adenoviruslarla tümden ilişkililendirilememiştir.
|
| |
TUMOR ANTIJENLERİ ONKOGENDİR
Papilloma virüsleri, adenovirüs veya polyoma virüsü tarafından oluşan tümörler
viral DNA içerirler ancak enfeksiyöz virüs oluşturmazlar. Ancak virüsün varlığı
tümör antijenlerine karşı antikorların oluşmasına sebep olur. Adenovirüslerin
sebep olduğu durumlarda viral genomun sadece bir kısmı konak hücre kromozomunda
bulunurken SV40 genomunun hepsini veya bir kısmını entegre edebilir. Bütün SV40
genomu entegre olsa da olmasa da genomun sadece ir kısmı mRNA’ya ve proteine
transkribe olur ve bu bölge virüs replikasyon döngüsünün erken fonksiyonlarını
kodlayan bölgedir.
Birçok DNA virüslerinin erken veya geç fonksiyonları bulunur. Erken
fonksiyonalr virüs üretimi için hücreyi hazırlayan proteinlerin ekspresyonu
sonucudur ve viral DNA replikasyonunda yer alırlar. Bu proteinler genom
replikasyonundan önce eksprese edilirler ve genellikle olgun virüs partikülünde
son bulmazlar. Geç fonksiyonlar ise olgun virüsü oluşturmak için bir araya gelen
viral yapısal proteinlerin ekspresyonunun sonucudur. Bunlar DNA replikasyonu
esnasında veya sonrasında eksprese edilirler. Erken fonsiyonlar viral genomun
replikasyonunda yer aldığından dolayı konak hücre DNA’sının replikasyonunu
değiştirebilmeleri süpriz değildir.
SV40 bu tip T antijeni olarak iki protein eksprese eder (büyük T ve küçük T
antijeni). Büyük T antijeni viral DNA replikasyonunda replikasyon orijinine
bağlanarak ve transkripsiyonu uyararak cis-regülatör elementi gibi davranır.
Aynı zamanda konak hücre DNA polimeraz alfasına bağlanabilir ve aktivitesini
düzenleyebilir.
Daha sonra göreceğimiz gibi, hücrede DNA replikasyonu süpresör proteinleri
tarafından kontrol edilir (en iyi çalışılanlar retinoblastoma (Rb) ve p53
süpresör proteinleridir). SV40 büyük T antijeni direkt olarak bu proteinlere
bağlanabilir ve bunları inaktif hale getirebilir. Böylece hücreyi G0 fazından S
fazına geçmesi için uyarır. Polyoma virüslerinin küçük genomları olmasından
dolayı DNA replikasyonu için birçok hücre fonksiyonuna gerek duyarlar ve virüsün
hücreyi S fazına geçirmesi önemlidir çünkü viral DNA replikasyonu için uygun bir
ortam yaratır.
Bu yüzden SV büyük T antijeni:
- bir hücrenin kanseröz duruma dönüşümü için gereklidir
- konak hücreyi DNA’sı replike etmesi için uyarır
- çoğunlukla nukleusta bulunur (nüklear lokalizasyon sinyaliyle hedef alır)
ancak küçük bir kısım hücre yüzeyine gider (bu bir tümör-spesifik
transplantasyon antijenidir)
- hücresel DNA’ya bağlanır
- p53 proteinine bağlanır (aşağıda bakınız)
Fare polyoma virüsünde onkogen olarak rol alan orta T antigeni de
bulunmaktadır.
Benzer şekilde adenovirüsle indüklenmiş tümörlerde viral genomun sadece bir
kısmı entegre olur ve yine bunlar genlerin erken bölgeleridir. Bu bölge E1A ve
E1B proteinlerini kodlar. Papilloma virüsü ile indüklenmiş tümörde de iki erken
gen olan E6 ve E7 eksprese edilir.
Bu yüzden, papilloma, polyoma ve adenovirüsleri hücre trasnformasyonuna
benzer şekilde sebep olmaktadır: erken fonksiyon genlerinin konak kromozomuna
entegrasyonu ve bu DNA sentezini kontrol edici genlerin viral yapısal
proteinlerin üretimi olmaksızın ekspresyonudur. Daha sonra göreceğimiz üzere, bu
üç virüs tipi de tümör süpresör genleriyle etkileşime geçerek hücre
proliferasyonunu uyarırlar.
DNA tümör virüslerinin T antijenleri hakkında onkogenler olarak iki önemli
noktaya dikkat edilmelidir:
- Bunlar gerçek viral genlerdir. Enfekte olmayan hücrede hücresel homolog
yoktur
- Bunlar litik enfeksiyonda gereklidir çünkü viral ve hücresel DNA
transkripsiyonunun kontrolünde yer alırlar.
Bu özellikler daha sonra tartışılacak olan retroviral onkogenleriyle zıt
olmalıdır.
|
|
Şekil 6
 Herpes virus. Negatif boyama
Herpes virus. Negatif boyama
Copyright Dr Linda M Stannard, University of Cape Town,
South Africa, 1995 (used with permsssion).
 Herpes Simplex Virus’da DNA kapsidinin faj-benzeri paketi, Sıvı Kristal
Herpes Simplex Virus’da DNA kapsidinin faj-benzeri paketi, Sıvı Kristal
(F.P.Booy, W.W.Newcomb, B.L.Trus, J.C.Brown, T.S.Baker,
and A.C.Steven, in CELL, Vol 64 pp 1007-1015, March 8, 1991)
 Herpes Simplex Virus (TEM x169,920) © Dennis Kunkel
Microscopy, Inc. Used with permission
Herpes Simplex Virus (TEM x169,920) © Dennis Kunkel
Microscopy, Inc. Used with permission
|
KOMPLEKS TUMOR VIRUSLARI
AILE: HERPESVIRIDAE
HERPESVIRUSLAR
Herpesvirüsleri (şekil 6) yukarıda bahsedilen DNA virüslerinden çok
daha büyüktür ve 100-200 kilobaz büyüklüğünde genoma sahiptir.
Büyüklüklerinden dolayı bu virüslerin hücreleri nasıl transforme
ettiğine yönelik keşfedilmesi gereken çok şey vardır.
Bu büyük zarflı virüslerin insan kanserlerinde gösteren önemli
kanıtlar vardır ve hayvanlarda oldukça tümörijeniktir. Herpes virüs
genomu spesifik bölgelerden konak hücresine entegre olur ve
kromozomal kırılma veya diğer hasara (aşağıda bakınız) sebep
olabilir. Herpes virüsleri sıklıkla ko-karsinojendirler. Onkogenezde
vur-kaç mekanizmasına sahip olabilir. Belki de enfeksiyonda erken
safhalarda proteinleri eksprese ederek kromozomal kırılmaya veya
diğer hasarlara yol açarlar.
Herpes virüsleri 100’den fazla gen içerir. Bu virüsler, virüs
üretimi için serbest olmayan ancak virüsleri transforme eden
hücreleri enfekte ettiğinde sadece bir grup viral DNA (yaklaşık 9)
eksprese edilir. Bu genler nüklear antijenleri veya membran
proteinlerini kodlar. Herpes-transforme hücrelerde bütün dokuz
transformasyon-ilişkili genler ekprese edilmez.
Epstein-Barr virus (İnsan
herpes virus 4)
EBV (şekil 7A) güçlü bir şekilde kanserle ilişkili olan bir herpes
virüsüdür. Primer olarak lenfositleri ve epitel hücrelerini enfekte
eder. Enfekte epitelyal hücrelerden virüs alındığında (üretici
enfeksiyon) lenfositlerde enfkeksiyon genellikle üretici değildir.
EBV nedensel olarak şunlarla ilişkilidir:
- Tropiklerde Burkitt’s lenfoması (şekil 7B) iken malarya –endemik
bölgelerde daha yaygındır
- Özellikle Ç, ve SE Asya’da nazofaringeal kanser, belirli
diyetler ko-karsiojen olarak ol alır.
- İmmün süprese kişilerde B hücre lenfoması (organ nakli veya
HIV gibi)
- Hastaların yüksek bir yüzdesinde görülen Hodgkin’s lenfoma (yaklaşık
%40 etkilenmiş hasta)
- X’e bağlı lenfoproliferatif Hastalık (Duncan sendromu)
EBV marmosetlerde lenfomaya sebep olabilir ve insan B
lenfositlerini in vitroda transorme edebilir.
Aynı zamanda EBV enfeksiyöz mononükleozise sebep olur. Bu diğer
bir deyişle glandular ateş olarak da bilinmektedir (şekil 7D). Bu,
tahlikesiz bir büyüme olan B-lenfosit enfeksiyonunun kendiliğinden
çözülmesidir. Sıklıkla enfeksiyon belirlenmez (sub-klinikal) ve batı
ülkelerinde popülasyonun neredeyse yarsı 20 yaşına geldiklerinde
enfekte hale gelirler. Bu virüsün neden bazı popülasyonlarda benign
hastalığa sebep olurken diğerlerinde malignant hastalık olduğu
bilinmemektedir.
|
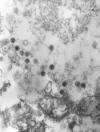 Şekil 7A
Şekil 7A
Epstein- Barr Virus |
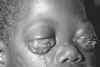 Şekil 7B
Şekil 7B
Epstein-Barr Virus nedenli Burkitt's Lenfoma The Johns Hopkins
Autopsy Resource (JHAR) Image Archive.
 Şekil 7C
Şekil 7C
Burkitt's lenfomanın dağılımı
 A
A
 B
B
Şekil 7D
Sağlıklı kişiden periferik kan örneği (A) ve Epstein-Barr virus
(EBV) ile infekte infectious mononucleosis hastası (B). Heriki
smearda Giemsa ile boyanmıştır
© Gloria J. Delisle and Lewis Tomalty Queens
University Kingston, Ontario, Canada and The MicrobeLibrary
|
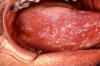 Şekil 7E
Şekil 7E
Erken oral hairy leukoplakia (OHL) dilin yan kenarında. HIV immunolojik
aktiviteyi azaltır, ağıziçi ortam bağışıklık sistemi baskılanmış
koşullar altında, Epstein-Barr virüsü nedenli oral hairy lökoplaki de
dahil olmak üzere inflamatuar süreçler ve kronik sekonder enfeksiyonlar
ana hedeftir
CDC
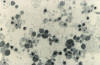 Şekil 7F
Şekil 7F
Sitomegalovirus virionlarının Transmisyon elektron mikrografisi
(x49,200)
CDC
|
İnsan Herpes Virus 8 (HHV-8,
Kaposi Sarkom Herpes Virus)
HHV-8 lenfositleri ve epitelyal/endotelyal hücreleri enfekte eder ve
Kaposi sarkomasının etkenidir. Aynı zamanda primer efüzyon lenfoma,
multisentrik Castleman’s (aynı zamanda Castelman’s) hastalığı (MCD),
MCD-ilişkili immünoblastik/plasmablastik lenfoma ve çeşitli
lenfoproliferatif bozuklukları içeren hematolojik malignansilerle de
ilişkilidir.
EBV ve HHV-8’in HIV ile enfekte hastalarda oral lezyonlar ve
neoplasmlar ile ilişkili oldukları bulunmuştur. Bu hastaların içinde
benign olup bu virüslerin çoğaldığı dil epitelinde beyaz şişliklere
sebep olan oral tüylü lökoplaki (OHL, şekil 7E)’dir.
Human sitomegalovirus (İnsan
Herpes Virus 5)
Bu herpes virüsü (şekil 7F) sıklıkla Kaposi sarkomasıyla ilişkilidir
ancak günümüzde bu hastalığın insan herpes virüsü 8 tarafından oluştuğu
düşünülmektedir.
Herpes virüsleri ve bu hastalıkla ilgili daha fazla bilgi için bölüm
11’deki Viroloji kısmına gidiniz.
|
|
Şekil 8
 Bu kadın hepatit B ve karaciğer kanserli. O Kamboçyalı mülteciydi ve bir
mülteci kampında geldikten sonra 4 ay öldü(karaciğer kanseri tanı
sonrası ortalama yaşam süresi 6 aydır) Immunization Action Coalition
Courtesy of Patricia Walker, MD, Ramsey Clinic
Associates, St. Paul, MN
Bu kadın hepatit B ve karaciğer kanserli. O Kamboçyalı mülteciydi ve bir
mülteci kampında geldikten sonra 4 ay öldü(karaciğer kanseri tanı
sonrası ortalama yaşam süresi 6 aydır) Immunization Action Coalition
Courtesy of Patricia Walker, MD, Ramsey Clinic
Associates, St. Paul, MN
|
AILE: HEPADNAVIRIDAE
HEPATIT B VIRUS
Hepatit B virüsü (şekil 9) diğer DNA tümör virüslerinden oldukça
farklıdır. Hatta bir DNA virüsü olmasına rağmen replikasyonu bakımından
onkornavirüslere (RNA tümör virüsleri) daha çok benzemektedir. DNA RNA’ya
sadece viral proteinlerin üretimi için değil aynı zamanda genom replikasyonu
için de transkribe olur. Genomik RNA tekrar genomik DNA’ya transkribe edilir.
Buna reverse transkripsiyon denir. Bu, çoğu DNA tümör virüsü için tipik
değildir ancak reverse transkripsiyon RNA-tümör virüslerinin yaşam
döngülerinde çok önemli bir faktördür. Aşağıya bakınız.
Hepatit B virüsü ve sebep olduğu hastalık hakkında daha fazla bilgi için
bölüm 18 ve 19, kısım 2’ye gidiniz.
Hepatit B çok yaygın bir haslk sağlığı problemidir ve dünyanın en yaygın
kanserlerinden birisi olan hepatoselüler karsinoma (HCC) (şekil 8) HBV
tarafından oluşur. HBsAg (hepatit B virüsü yüzey antijeni) kronik
taşıyıcıları ile HCC insidansı arasında güçlü bir ilişki vardır. Tayvan’da
HBsAg taşıyıcılarının taşıyıcı olmayanlara göre 217 kat daha fazla HCC riski
olduğu gösterilmiştir. HBsAg taıyıcı ölümlerinin %51’i karaciğer sirozu veya
HCC tarafından oluşur. Genel popülasyonda ise %2’dir.
|
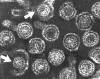 Hepatit B virionları: maruz kalınan iki kor (indicated by arrows)
Hepatit B virionları: maruz kalınan iki kor (indicated by arrows) |
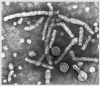 Hepatit B virionları
Hepatit B virionları
 Hepatit B virion ve surface antijen komponentlerinin diagramatik
sunumu
Hepatit B virion ve surface antijen komponentlerinin diagramatik
sunumu
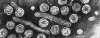 Hepatit
B Virus Hepatit
B VirusŞekil 9
All four images: Copyright Dr Linda M Stannard,
University of Cape Town, South Africa, 1995 (used with
permission).
|
|
|
|
|


|
 Mikrobiyoloji ve İmmünoloji On-line, Viroloji Bölümüne Dönünüz
Mikrobiyoloji ve İmmünoloji On-line, Viroloji Bölümüne Dönünüz
This page last changed on
Sunday, June 05, 2016
Page maintained by
Richard Hunt
|


 Şekil 1
Şekil 1 Epidermodysplasia verruciformis. Bu yaygın, belirgin kaşıntılı,
eritematoz döküntülü. İnsan papillomavirus infeksiyonu kaynaklı olduğu
bulundu.
Epidermodysplasia verruciformis. Bu yaygın, belirgin kaşıntılı,
eritematoz döküntülü. İnsan papillomavirus infeksiyonu kaynaklı olduğu
bulundu.  Şekil 7A
Şekil 7A Şekil 7E
Şekil 7E Hepatit B virionları: maruz kalınan iki kor (indicated by arrows)
Hepatit B virionları: maruz kalınan iki kor (indicated by arrows)





















