|
x |
x |
|
 |
 |
|
INFECTIOUS
DISEASE |
BAKTERIYOLOJİ |
IMMUNOLOGY |
MYCOLOGY |
PARASITOLOGY |
VIROLOGY |
|
ENGLISH |
BAKTERİYOLOJİ – BÖLÜM
YİRMİBİR
RICKETTSIA, ORIENTIA, EHRLICHIA, ANAPLASMA, COXIELLA ve BARTONELLA
Dr. Gene Mayer
Professor Emeritus
University of South Carolina School of Medicine
Çeviren
Prof. Dr. Mustafa Demirci
İzmir Katip Çelebi Üniversitesi, Tıp Fakültesi
|
|
SLOVAK |
|
|
|
|
|
|
Let us know what you think
FEEDBACK |
|
SEARCH |
 |
|
Most images on this page come
from the Centers for Disease Control |
|
ÖĞRETİM HEDEFLERİ
Konak hücresi ile Rickettsia, Ehrlichia, Coxiella ve Bartonella
etkileşimlerini tanımlamak
Rickettsia, Ehrlichia, Coxiella ve Bartonella ile ilişkili patogenezi,
epidemiyoloji ve klinik sendromları tanımlamak
Riketsiyal hastalıkların kontrol, korunma ve tedavi yöntemlerini
tartışmak.
ANAHTAR KELİMELER
Rezervuar
Vektör
Kayalık dağlar benekli ateşi
erlihyozis
Riketsiya çiçeği
Çalılık tifüsü
Epidemik tifüs
Fare tifüsü
Q ateşi
Siper ateşi
Kedi tırmığı hastalığı
Transovaryan geçiş
Weil-Felix testi
Brill-Zinsser hastalığı
Morula
|
Riketsiyal
enfeksiyonlar batı medeniyetinin tarihinde önemli bir rol oynamıştır. Epidemik
tifüs 16. yüzyıldan beri bilinmektedir ve uzun süre kıtlık ve savaş ile ilişkili
olduğu bilinmektedir. Birçok savaşın sonucunu epidemik tifüs etkilemiştir.
Tifüs, iki dünya savaşında, 100.000'den fazla kişinin ölümüne yada büyük acılar
çekmesine neden oldu. Uzun geçmişine rağmen, 20. yüzyılın başlarına kadar bu
hastalığın etkeni tespit edilememiştir. Howard Ricketts Kayalık dağlar benekli
ateşinin etkenini tanımladı ve ajanın laboratuvar hayvanlarında kültürünü
başardı. Diğerleri daha sonra epidemik tifüs etkenininde açıklanan organizma
Ricketts ile ilişkili olduğunu fark ettiler. Tifüsün yayılmasında
eklembacaklı vektörlerin öneminin keşfinden sonra, hastalığın kontrolü için
vektör kontrol önlemleri tesis edilmiştir. Bunlara ragmen, Hans Zinsser'in
işaret ettiği gibi, tifüs ölmedi.
Rickettsia,
Ehrlichia, Anaplasma
ve Coxiella, aynı ailenin bir parçası olduğu düşünülen tümü küçük,
zorunlu hücre içi parazitlerdir. Ancak şimdi, bu bakterilerin farklı, akraba
olmadıkları düşünülmektedir. Klamidya gibi bu bakterilerin önceleri küçük boyutu
ve hücre içi yaşam döngüsü nedeniyle virüs olduğu düşünüldü. Bununla birlikte,
gram negatif bakteriler ile yapısal olarak benzer, gerçek bakteridirler. Küçük
Gram negatif kokobasil yapısında bu bakteriler, Gram boyama ile kötü
boyandıkları için Giemsa ile boyanırlar. Bu bakteriler üremek için gerekli tüm
metabolitleri yapabilme yeteneğinde olmasına rağmen, onlar ev sahibinin
ATP'sinin kullanımına için izin veren bir ATP taşıma sistemine sahiptir. Bundan
dolayı, konaktan ATP sağlayabildikleri sürece, enerji parazitleridirler.
Bu organizmalar;
bir hayvan ve eklembacaklı rezervuarda hayattlarını sürdürürler, Coxiella hariç
olmak üzere, hepsi eklembacaklı vektörler (ör keneler, akarlar, bitler veya
pireler) ile bulaştırılır. Bu organizmalar insanlara rastlantısal olarak
bulaşır. Rezervuarlar, vektörler ve bu organizmaların neden olduğu başlıca
hastalıklar Tablo 1'de özetlenmiştir. (Murray ve ark. Tıbbi Mikrobiyoloji'den:
uyarlanmıştır).
|
Tablo 1 |
|
Hastalık |
Organizma |
Vektör |
Rezervuar |
|
Kayalık dağlar Benekli ateş |
R. rickettsii |
Kene |
Keneler, yabani kemirgenler |
|
Erlihyoz |
E. chaffeensis
E. ewingii
|
Kene |
Geyik
Küçük memeliler |
|
Anaplazoz |
A. phagocytophilum |
Kene |
Geyik
Küçük memeliler |
|
Riketsiya çiçeği |
R. akari |
Akar |
Akarlar, yabani kemirgenler |
|
Çalılık tifüsü |
R. tsutsugamushi |
Akar |
Akarlar, yabani kemirgenler |
|
Epidemik tifüs |
R. prowazekii |
Bit |
İnsanlar, sincaplar, uçan sincaplar, pireler |
|
Fare tifüsü |
R. typhi |
Pire |
Yabani kemirgenler |
|
Q ateşi |
C. burnetii |
Yok |
Sığır, koyun, keçi ve kediler |
|
|
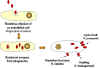 Şekil 1
Şekil 1
Endotel hücresinde Riketsiyal ve Orientia infeksiyonu.
|
RICKETTSIA VE ORIENTIA
Orientia eskiden Rickettsia olarak adlandırılırdı
Çoğalma
Rickettsia tercihen parazitin uyardığı
fagositoz ile küçük kan damarlarını (Şekil 1) döşeyen endotel
hücrelerini enfekte eder. Bakteri konak hücresine girince fosfolipaz ile
fagosom membranını parçalar ve sitoplazma içinde çoğaltmaya başlar.
Konakçı hücreden çıkış şekli türlere bağlı olarak değişiklik gösterir.
R. prowazekii hücreyi parçalayarak hücreden çıkarken, R. rickettsii
yerel çıkıntılar (filopodia) üzerinden hücreden dışarı çıkar, konak
hücresinin F aktini R. rickettsii ile birleşir ve aktin filopodia
aracılığıyla bakterinin hücre dışına "itme" çıkmasına (sekil 2) yardımcı
olur. O. tsutsugamushi hücre membranından tomurcuklanarak çıkar ve konak
hücre membranıyla sarılı olarak diğer hücreleri enfekte eder.
Antijenik yapı
Antijenik bileşimi temelinde, Rickettsia
birkaç gruba ayrılır. Her gruptaki organizmalar, organizmalar neden
olduğu hastalıklar ve bunların jeolojik dağılımı Tablo 2'de
özetlenmiştir. (Murray ve ark. Tıbbi Mikrobiyoloji'den: uyarlanmıştır).
|
Tablo 2 |
|
Benekli ateş grubu |
|
Organizma |
Hastalık |
Dağılım |
|
R. rickettsii |
Kayalık dağlar benekli ateş |
Batı yarım küre |
|
R. akari |
Riketsiya çiçeği |
ABD, eski Sovyetler Birliği |
|
R. conorii |
Sivilceli (akdeniz benekli) ateş |
Akdeniz ülkeleri, Afrika, Hindistan, Güneybatı Asya |
|
R. sibirica |
Sibirya kene tifüsü |
Sibirya, Mogolistan, kuzey Çin |
|
R. australis |
Avusturalya kene tifüsü |
Avusturalya |
|
R. japonica |
Doğu (Japon) benekli ateşi |
Japanya |
|
Tifüs grubu |
|
Organizma |
Hastalık |
Dağılım |
|
R. prowazekii |
Epidemik tifüs
Nükseden tifüs (Brill Zinsser hast.)
Sporadik tifüs
|
Güney Amerika ve Afrika
Dünyada yaygın
ABD
|
|
R. typhi |
Fare tifüsü |
Dünyada yaygın |
|
Çalılık Tifüs grubu |
|
Organizma |
Hastalık |
Dağılım |
|
O. tsutsugamushi |
Çalılık tifüsü |
Asya, kuzey Avusturalya, Pasifik adaları |
Patogenezis ve
immunite
Patogenez öncelikli olarak, çoğalan bakterilerin, enfekte
olmuş hücreleri tahrip etmesine bağlıdır. Endotel hücrelerinin yıkımı
nedeniyle, kan kaybıyla ve doku boşluklarına kan kaçağına bağlı olarak,
organ ve doku hasarıyla sonuçlanır. İmmunopatolojik hasara dair hiçbir kanıt
elde edilmemiştir. Hem humoral ve hemde hücre aracılı bağışıklık
enfeksiyonun iyileşmesinde önemlidir. Antikorla-opsonize edilen (işaretlenen)
Rickettsia fagosite edilir ve makrofajlar tarafından öldürülür ve riketsiyal
enfeksiyonları izleyen gecikmiş tip aşırı duyarlılık gelişir.
|
Şekil 2
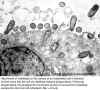 Endotel hücrenin yüzeyine Rickettsia'nın tutunması,
rickettsia-tarafından uyarılan fagositoz yoluyla hücre içine girişini
takip eder. Fagositoz ardından, fagosom membran (ok) kaybolur ve
Rickettsia konak hücre sitoplazması içine kaçar.
Endotel hücrenin yüzeyine Rickettsia'nın tutunması,
rickettsia-tarafından uyarılan fagositoz yoluyla hücre içine girişini
takip eder. Fagositoz ardından, fagosom membran (ok) kaybolur ve
Rickettsia konak hücre sitoplazması içine kaçar.
© Vsevolod Popov and David H. Walker, University of Texas Medical Branch
at Galveston, Galveston, Texas USA and The MicrobeLibrary |
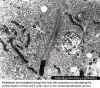
 Fagozomlardan salındıktan sonra, Rickettsia (oklarla görülen) ikye
bölünerek kültüre yapıldığı hücrelerin sitoplazmasında serbest
çoğalır. Ek olarak fotoğrafta riketsiya dış ve iç zarları
vurgulamaktadır.
Fagozomlardan salındıktan sonra, Rickettsia (oklarla görülen) ikye
bölünerek kültüre yapıldığı hücrelerin sitoplazmasında serbest
çoğalır. Ek olarak fotoğrafta riketsiya dış ve iç zarları
vurgulamaktadır.
© Vsevolod Popov and David H. Walker, University of
Texas Medical Branch at Galveston, Galveston, Texas USA and The
MicrobeLibrary
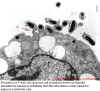
 Rickettsiae, konak hücre F-aktin polimerizasyonunu uyararak,
konak hücre sitoplazması aracılığıyla hareket kazanmıştır, kuyruklu
yıldız gibi 'kuyruk' (ok) görülen.
Rickettsiae, konak hücre F-aktin polimerizasyonunu uyararak,
konak hücre sitoplazması aracılığıyla hareket kazanmıştır, kuyruklu
yıldız gibi 'kuyruk' (ok) görülen.
© Vsevolod Popov and David H. Walker, University of
Texas Medical Branch at Galveston, Galveston, Texas USA and The
MicrobeLibrary
 Komşu endotel hücrelerine yayılım veya hücre yüzeyinden riketsiya
salınımında, filopodia olarak bilinen uzun konak hücre çıkıntıları
içine F-aktin ile itme gücü önce gelir. sds
Komşu endotel hücrelerine yayılım veya hücre yüzeyinden riketsiya
salınımında, filopodia olarak bilinen uzun konak hücre çıkıntıları
içine F-aktin ile itme gücü önce gelir. sds
© Vsevolod Popov and David H. Walker, University of
Texas Medical Branch at Galveston, Galveston, Texas USA and The
MicrobeLibrary
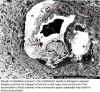 Endotelde Riketsiya üremesi (oklar), damar bütünlüğünün bozulmasına
ve beyin gibi hayati organlar içine sıvı sızmasıyla sonuçlanır.
Perivasküler boşlukta (yıldız) sıvı (ödem) birikmesi, klinik olarak
ensefalite neden olabilir.
Endotelde Riketsiya üremesi (oklar), damar bütünlüğünün bozulmasına
ve beyin gibi hayati organlar içine sıvı sızmasıyla sonuçlanır.
Perivasküler boşlukta (yıldız) sıvı (ödem) birikmesi, klinik olarak
ensefalite neden olabilir.
© Vsevolod Popov and David H. Walker, University of
Texas Medical Branch at Galveston, Galveston, Texas USA and The
MicrobeLibrary
 Konak bağışıklık hücreleri tarafından salgılanan, gama interferon ve
tümör nekroz faktör alfa, enfekte endotel hücreleri otofagozom
oluşumu yoluyla, hücre içi Rickettsia'ları öldürmek için "uyarır".
Daha sonra, lizozomların otofagozomla füzyonu ölecek olan
Rickettsia'ların (ok) sindirilmesiyle sonuçlanır.
Konak bağışıklık hücreleri tarafından salgılanan, gama interferon ve
tümör nekroz faktör alfa, enfekte endotel hücreleri otofagozom
oluşumu yoluyla, hücre içi Rickettsia'ları öldürmek için "uyarır".
Daha sonra, lizozomların otofagozomla füzyonu ölecek olan
Rickettsia'ların (ok) sindirilmesiyle sonuçlanır.
© Vsevolod Popov and David H. Walker, University of
Texas Medical Branch at Galveston, Galveston, Texas USA and The
MicrobeLibrary
|
| |
|
|
Rickettsia
rickettsii (Kayalık dağlar benekli ateşi)
Epidemiyoloji
Amerika Birleşik Devletleri'nde, yılda meydana gelen 400-700
vaka ile kayalık dağlar benekli ateşi en sık görülen riketsiyal
hastalıktır.
Hastalık başlangıçta
Kayalık dağların bulunduğu devletlerde tanımlanırken, şimdi
Güney Carolina (sekil 4) da dahil olmak üzere Güney Merkez
devletler arasında da yaygın olduğu bilinmektedir.
Çoğu enfeksiyonda organizma, kene ile insanların temasının daha
çok olduğu mevsim zamanlarında, Eylül ile Nisan arasında meydana
gelen infekte kenelerin ısırmasıyla bulaştırılır.
Kenelerdeki Rickettsia
dormant (uyuşuk) durumdadır ve sıcak kan ile beslenerek aktive
edilmelidir. Daha sonra kenelerin tükürükleri ile salınır.
Böylece, organizmaların insan konağa bulaşabilmesi için önce
enfekte kenelere uzun süreli maruz kalmanın (24-48 saat)
gerçekleşmesi gerekir. R. rickettsii'nin, transovarial geçişinde
meydana geldiği, başlıca rezervuarı ixodid (sert) keneleridir.
Vahşi kemirgenler enfekte olabilir ve bakteriler için bir
rezervuar görevi yaparlar ancak, ana rezervuar olarak kabul
edilmezler.
|
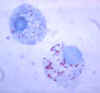 Şekil 3
Şekil 3
Gimenez boyasında Kenelerin enfekte hemolenf hücrelerinde R.
rickettsii
CDC
|
|
Şekil 4
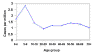
Yaş gruplarına göre ortalama yıllık Kayalık dağlar benekli ateşi
insidansı 1993-1996
CDC |
 ABD’de rapor edilmiş kayalık dağlar benekli ateşi vakaları,
1942-1996
ABD’de rapor edilmiş kayalık dağlar benekli ateşi vakaları,
1942-1996
CDC
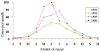 Kayalık dağlar benekli ateşi rapor edilmiş vakaların sezonal
dağılımı, 1993-1996
Kayalık dağlar benekli ateşi rapor edilmiş vakaların sezonal
dağılımı, 1993-1996
CDC
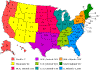 Devlet ve bölgelere göre rapor edilmiş Kayalık dağlar benekli ateşi
olguları sayısı, 1994-1998
Devlet ve bölgelere göre rapor edilmiş Kayalık dağlar benekli ateşi
olguları sayısı, 1994-1998
CDC
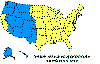 Amerikan köpek kenesinin yaklaşık dağılım
Amerikan köpek kenesinin yaklaşık dağılım
CDC
 Kayalık
dağlar orman kenesi (Dermacentor andersoni) Kayalık
dağlar orman kenesi (Dermacentor andersoni)
CDC
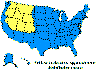 Kayalık dağlar orman kenesinin yaklaşık dağılımı
Kayalık dağlar orman kenesinin yaklaşık dağılımı
CDC
|

Amerikan köpek kenesi (Dermacentor variabilis)
CDC |
 Şekil
5 Şekil
5
Dermacentor variabilis ve Dermacentor andersoni
kenelerinin genel yaşam döngüleri (Aile Ixodidae)
CDC
|
Klinik sendromlar
Kayalık dağlar benekli ateşi, keneısırığından 2-12 gün sonrası ani
başlangıçlı ateş, baş ağrısı, titreme ve genellikle myalji ile
başlar. Hastalar kene tarafından ısırıldığını hatırlamıyabilir.
Döküntü genellikle (vakaların %90) 2-3 gün sonra görünür. Döküntü
ellerde ve ayaklarda başlar ve gövde doğru merkezcil olarak yayılır.
Avuç içi ve ayak tabanında döküntü yaygındır. Başlangıçta,
makülopapüler olan döküntü daha sonraki aşamalarda peteşial ve
hemorajik (Şekil 6) olabilir.
Yaygın vaskülitten kaynaklanan komplikasyonlar; gastrointestinal
semptomlar, solunum yetmezliği, nöbet, koma ve akut böbrek
yetmezliği olarak görülebilir. beri Komplikasyonlaren sık,
döküntünün görülmediği ve genellikle tedavinin geciktiği olgularda
ortaya çıkar. Tedavi edilmeyen olgularda mortalite oranı %20'dir.
|
|
Şekil 6 |
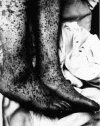 Bir hastanın ayakları üzerinde geç kronik dönem kayalık dağlar
benekli ateşi'nin karakteristik benekli döküntüsü 1946
Bir hastanın ayakları üzerinde geç kronik dönem kayalık dağlar
benekli ateşi'nin karakteristik benekli döküntüsü 1946
CDC
 Ayak tabanında Erken (maküler) döküntü
Ayak tabanında Erken (maküler) döküntü
CDC
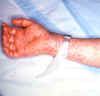 Avuç içi ve önkolda geç (peteşiyal) döküntü
Avuç içi ve önkolda geç (peteşiyal) döküntü
CDC
|
| |
Laboratuvar tanısı
İlk tanı klinik olarak yapılmalı ve laboratuarlarda doğrulanana
kadar tedavi gecikmemelidir. Deri punch biyopsisinde antijeni tespit
edip, tanıyı doğrulamak için en hızlı yol floresan antikor testidir.
Ancak, bu test sadece referans laboratuarlarında bulunur. PCR
tabanlı yöntemler de kullanılabilir ancak, bu testler de referans
laboratuvarlarında sınırlıdır. Bir aglütinasyon testi olan ve
Proteus vulgaris ile çapraz reaksiyona giren antikorları tespit
etmek için kullanılan, Weil-Felix testi artık tavsiye edilmemektedir.
Birincil laboratuvar tanı aracı serolojik yöntemlerdir. İndirekt
floresan antikor testleri (sekil 7) ve lateks aglütinasyon testleri
kayalık dağlar benekli ateşinin serolojik tanısı için kullanılabilir.
|
 Şekil 7
Şekil 7
Tavuk yolk sakında üreyen Rickettsia rickettsii ile insan
serumunun IFA’da pozitif reaksiyonu 400X
CDC
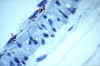 Şekil 8
Şekil 8
Kırmızı yapılar, Rickettsia rickettsii’nin KDBA’den ölen bir
hastanın, kan damarı endotel hücrelerinde immunohistokimyasal olarak
boyandığını gösterir.
CDC
|
Tedavi, korunma ve kontrol
R.rickettsii tetrasiklin ve kloramfenikol karşı hassastır. Tedavi
geciktiğinde morbidite ve mortalite arttığı için, acil tedavi gereklidir.
Aşısı yoktur. Kene ısırıklarından (koruyucu giysi, böcek kovucular, vb)
korunma ve kinelerden hızlıca kurtulmak en iyi önleyici tedbirlerdir. Kene
rezervuarları kontrol etme girişimleri uygulanabilir değildir.
Rickettsia akari
(Riketsiya çiçeği)
Epidemiyoloji
R. akari Amerika Birleşik Devletleri'nde bulunur ve sporadik
enfeksiyonlar şeklinde görülür. Vektör, bir fare akarıdır ve
rezervuarlar akar ve farelerdir. Akarlar, bakteriyi transovarial olarak
aktarabilirler. İnsanlara kazara bulaşmaktadır.
Klinik sendromlar
Riketsiya çiçeği genellikle iki evreden oluşan hafif bir hastalık
tablosudur. Birinci aşamasında; akar ısırık yerinde bir papül gelişir ve
hızla ülserleşerek bir skar dokusu oluşur. Bu ilk aşama kene ısırığından
yaklaşık 1 hafta sonra meydana gelir. 7 ila 24 günlük bir inkübasyon
süresinden sonra, hastalığın ikinci aşaması meydana gelir. Bu aşama ani
başlayan ateş, titreme, baş ağrısı ve miyalji ile karakterizedir ve
yaygın döküntü ile 2 ila 3 gün sonra takip eder. Sonraki aşamalarda
papüloveziküler ve kabuklar ile döküntü gelişir. Çiçek skar yarası
oluşmadan 2 ila 3 hafta içinde iyileşirler. Ölüm nadirdir.
Laboratuvar tanısı
Belirli referans laboratuarları dışında yoktur.
Tedavi and korunma ve kontrol
Tetrasiklin ve kloramfenikol iyileşmeyi hızlandırabilir. Fare nüfusunu
kontrol etme çalışmaları hastalığı önlemeye yardımcı olur.
|
| |
Rickettsia prowazekii (Epidemik
tifüs veya bit kaynaklı tifüs)
Epidemiyoloji
Epidemik tifüs, insan vücud biti (Pediculus humanus corporis) tarafından
bulaştırılan bir hastalıktır. Enfekte bit bir insanı ısırdığında,
bakteri bulunan dışkısını da deriye bırakır. Isırık nedeniyle derisi
tahriş olan kişi derisini kaşıyınca zaten aşınmış deri içine bakteriyi
inoküle eder. Diğer riketsiya hastalıkları aksine, insan R. prowazekii
için primer rezervuardır. Epidemik tifüs, savaşlar, kıtlık ve doğal
afetler gibi ortamlarda sağlıksız koşullarda ve kalabalık yaşayan
insanlar arasında ortaya çıkar. Bitler enfekte olduktan birkaç hafta
sonra öldüklerinden, transovarial aktarım olmamaktadır. ABD'de primer
olarak doğu devletlerinde, hastalık sporadik olarak ortaya çıkar ve
rezervuaralar uçan sincaplar ve onların pireleridir. Pire hastalığı
bulaştıran bir vektördür.
Klinik sendromlar
- Epidemik tifüs ortalama 8 gün bir kuluçka döneminden sonra, ani
başlanğıçlı ateş, titreme, baş ağrısı, miyalji ve eklem ağrısı ile
karakterizedir. Yaklaşık 7 gün sonra, bir döküntü hastaların çoğunda
gelişir. Döküntü makulopapüler ama peteşial veya hemorajik olabilir.
Kayalık dağlar benekli ateşinde görülen döküntü aksine, epidemik
tifüste döküntü ilk gövdede gelişir ve ekstremitelere (merkez kaç
yayılır) yayılır. Komplikasyonlar: miyokardit, uyuşukluk ve deliryum
olarak görülür. Tifüs adı, sıklıkla hastalık komplikasyonu olan
sersemlik ve deliryum gerçeğini vurgulayan yunanca "duman"
anlamından gelmektedir. İyileşme birkaç ay sürebilir. Ölüm oranı
değişir ama bazı epidemilerde (%60-70) oldukça yüksek olabilir.
- Brill-Zinsser hastalığı nükseden epidemik tifüs hastalığıdır. Bu
ilk enfeksiyondan yıllar sonra ortaya çıkabilir. Amerika Birleşik
Devletleri'nde en sık 2. Dünya Savaşında epidemik tifüse maruz kalan
kişilerde görülür. Hastalık klinik seyri epidemik tifüs benzer ama
daha hafif ve iyileşme hızlıdır. Deri döküntüsü nadiren görülür.
Tanı nedeni bilinmiyen bir ateş ve epidemik tifüse önceki maruziyet
öyküsü temelinde yapılır.
Laboratuvar tanısı
Tanı, klinik bulgularla konulmalı ve tedavi, laboratuvar teyidinden önce
başlamalıdır. Weil-Felix antikorları üretilir fakat bu test tavsiye
edilmez. Seroloji R. prowazekii tanısında kullanılan başlıca laboratuvar
alanıdır. İndirekt floresan antikor testleri ve lateks aglütinasyon
testleri mevcuttur. Epidemik tifüs hastalarında başlangıçta bir IgM
antikorları vardır ve takiben bir IgG yanıtı varken, Brill-Zinsser
hastalığında başlangıçta anamnestik bir IgG yanıtı vardır. Organizmanın
izolasyonu mümkündür ama tehlikelidir.
Tedavi, korunma ve kontrol
Tetrasiklinler ve kloramfenikol son derece etkilidir. Fare kontrol
önlemleri enfeksiyonu önleyebilir. Bir ölü bakteriden hazırlanan tifüs
aşısı mevcuttur ve yüksek riskli toplumlarda kullanılmak üzere tavsiye
edilir.
|
| |
Rickettsia typhi
(Fare veya endemik tifüs)
Epidemiyoloji
Fare tifüsü dünyada yaygındır ve ABD'de her yıl yaklaşık
40-60 vaka bildirilmektedir. Fareler primer rezervuardır, hastalık
vektör olan fare piresi tarafından bulaştırılır. Normal döngü fare-pire-fare
şeklindeyken insanlara kazara bulaşmaktadır. Pirede transovarial aktarım
olmadığından, pire hastalık için rezervuar değildir. ABD'de aynı zamanda
kedi piresi hastalık için bir vektör olabilir. Bakteriler pire
dışkısında bulunur ve ısırık ile tahriş olan derinin kaşınmasıyla deri
içine aşılanır.
Klinik sendromlar
Enfeksiyonun bulaşmasından 1-2 hafta sonra aniden ateş, titreme, baş
ağrısı ve kas ağrıları belirtileri ile başlar. Döküntü birçok hastafa
olmakla birlikte hepsinde yoktur. Döküntü gövdeden başlar, kayalık
dağlar benekli ateş'inde görülen döküntü aksine, ekstremitelere yayılır.
Hastalık hafif seyirlidir ve hatta tedavi edilmese bile 3 hafta içinde
düzelir.
Laboratuvar tanısı
R. typhi’ye karşı antikorları saptamak için serolojik olarak
indirekt floresans antikor testi kullanılır.
Tedavi, korunma ve kontrol
Tetrasiklin ve kloramfenikol etkilidirler. Rezervuar kemirgenlerin
kontrolü enfeksiyondan korunmak için yararlıdır. Aşısı yoktur.
|
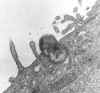 Şekil
9 Şekil
9
Rickettsia tsutsugamushi’nin
fare peritoneal mezotelial hücresinde fagositozu.
CDC/Dr. Edwin P. Ewing, Jr. epe1@cdc.gov
|
Orientia (Rickettsia)
tsutsugamushi (Çalılık tifüs)
Epidemiyoloji
Çalılık tifüsü Asya, Avustralya ve Pasifik Adalarında oluşur. Hastalık
insanları ısırabilen bir akarın (chiggers) larva formu ile bulaşır.
Akarlarda transovaryal bulaşma olduğu için hem vektör hemde rezervuardır.
Kemirgenler da rezervuar olarak rol oynarlar. Normal döngü
akar-kemirgen-akar şeklindedir ve İnsanlara kazara bulaşır.
Klinik sendromlar
Hastalık bakteriyel karşılaştıktan, 1-3 hafta sonra ani başlanğıçlı den
ateş, titreme, baş ağrısı ve kas ağrısıyla ortaya çıkar. 2-3 gün sonra
bir makülopapüler döküntü gelişir. Döküntü önce gövdede görülür sonra
ekstremitelere yayılır (Merkezkaç yayılım). Mortalite oranı salgınlarda
değişkenlik gösterir.
Laboratuvar tanısı
Antikor saptamak için serolojik testler vardır.
Tedavi, korunma ve kontrol
Tetrasiklinler ve kloramfenikol etkilidir. Hastalıktan korunmak için
akar ısırığından kaçının.
|
|
|
EHRLICHIA AND
ANAPLASMA
Çoğalma
Ehrlichia ve Anaplasma tercihen lökositleri enfekte eder. Onlar
fagositoz ile hücreye girip konakçı hücrede fagolisozom birleşmesini
inhibe ederler. Organizmalar zara bağlı fagozomun içinde büyür ve
hücre lizizi (sekil 10) ile serbest bırakılır. Bakterileri içeren
inklüzyon cisimciğine bir morula denir.
Epidemiyoloji
Ehrlichia genetik benzerliğine göre üç gruba ayrılır. Tablo 3
(Murray ve ark. Tıbbi Mikrobiyoloji'den uyarlanmıştır) Ehrlichia ve
Anaplasma'nın neden olduğu insan hastalıkları, vektörler,
rezervuarlar ve coğrafi dağılımlarını özetlemektedir.
|
 Şekil
10 Şekil
10
Lökositlerde Ehrlichia infeksiyonu
|
Şekil 11
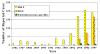 ABD’de rapor edilen Erlihyoz vakaları CDC
ABD’de rapor edilen Erlihyoz vakaları CDC |
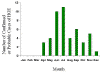 ABD’de HGE’nin yaklaşık seasonal dağılım
ABD’de HGE’nin yaklaşık seasonal dağılım
CDC
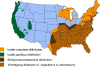 İnsan erlihyozunun bulunduğu alanlarda, vektör kene türünün yaklaşık
dağılım
İnsan erlihyozunun bulunduğu alanlarda, vektör kene türünün yaklaşık
dağılım
CDC
|
| |
|
Tablo 3 |
|
Organizma |
Hastalık |
Vektör |
Rezervuar |
Dağılım |
|
E chaffeensis |
İnsan monositik erlihyozu |
Amerikan kenesi |
Beyaz kuyruklu geyik |
Güneydoğu, orta Atlantik, ve Güney Orta ABD |
|
E. ewingii |
Primer köpek hastalığı, İnsan granülositik erlihyozu |
Amerikan kenesi |
Beyaz kuyruklu geyik |
Güneydoğu, orta Atlantik, ve Güney Orta ABD |
|
A. phagocytophilum |
İnsan granülositik anaplazmoz (insan anaplazmoz) |
Geyik ve köpek keneleri |
Küçük memeliler |
Wisconsin, Minnesota,
Connecticut |
|
E. sennetsu |
Sennetsu (ilerleyen) ateş |
Bilinmiyor |
Bilinmiyor |
Japanya |
|
| |
Ehrlichia chaffeensis
(İnsan monositik erlihyozu)
Klinik sendromlar
Hastalık, döküntünün çoğu (%80) hastada geliştemesi dışında,
kayalık dağlar benekli ateşine benzer. Buna ek olarak,
lökositlerin imha edilmesine bağlı olarak lökopeni görülmektedir.
Mortalite düşüktür (%5).
Laboratuvar tanısı
Kan yaymasında morulanın mikroskobik görüntülenmesi
nadirdir ve kültürü mümkün olmasına rağmen, nadiren girişiminde
bulunulur. Serolojik testi mevcuttur ve en sık kullanılan
testlerdir. DNA probları mevcuttur ve serolojik testler yerini
alabilir.
Tedavi, korunma ve kontrol
Hastalar doksisiklin ile tedavi edilmelidir. Kenelerin enfekte
alanlarından kaçınmak ve koruyucu tedbirlerle (giysi ve böcek
kovucu) hastalık önlenebilir.
|
Figure 12
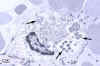 Ehrlichiosis olan bir hastada kemik iliği lökositlerinde morula
elektron-fotomikrografıdır. Oklar bireysel Ehrlichia işaret
ediyor
Ehrlichiosis olan bir hastada kemik iliği lökositlerinde morula
elektron-fotomikrografıdır. Oklar bireysel Ehrlichia işaret
ediyor
CDC |
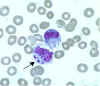 Ehrlichia chaffeensis esas olarak mononükleer lökositler (ağırlıklı
olarak monositler ve makrofajlar) enfekte eder, aynı zamanda ciddi
bir hastalık olan bazı hastalarda granülositlerde de görülebilir. (Morula
monosit sitoplazmasında).
Ehrlichia chaffeensis esas olarak mononükleer lökositler (ağırlıklı
olarak monositler ve makrofajlar) enfekte eder, aynı zamanda ciddi
bir hastalık olan bazı hastalarda granülositlerde de görülebilir. (Morula
monosit sitoplazmasında).
CDC
 Amerikan kenesi (Amblyomma americanum)
Amerikan kenesi (Amblyomma americanum)
CDC
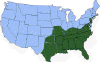 Amerikan kenesinin yaklaşık dağılımı
Amerikan kenesinin yaklaşık dağılımı
CDC
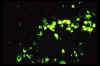 IDH82 hücrelerinde, Ehrlichia chaffeensis IFA görüntüsü 400X
IDH82 hücrelerinde, Ehrlichia chaffeensis IFA görüntüsü 400X
CDC
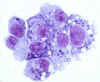 DH82 hücrelerinde, Ehrlichia chaffeensis Diff-Quik boyası, 1000X
DH82 hücrelerinde, Ehrlichia chaffeensis Diff-Quik boyası, 1000X
CDC
 Ehrlichia sp. ilk olarak retikule hücreleri (RC) gibi konak hücre
vakuollerinde (DC) sonra yoğun çekirdekli hücreler içinde gelişir.
Bir Ehrlichial mikrokolonisi içeren bir vakuol morula olarak
adlandırılır. Bir tanesi ölü Ehrlichia'lar ile dolu gibi görünen
dahil olmak üzere, bu konak hücrede birkaç morulla (ok ile
gösterilen) görülüyor.
Ehrlichia sp. ilk olarak retikule hücreleri (RC) gibi konak hücre
vakuollerinde (DC) sonra yoğun çekirdekli hücreler içinde gelişir.
Bir Ehrlichial mikrokolonisi içeren bir vakuol morula olarak
adlandırılır. Bir tanesi ölü Ehrlichia'lar ile dolu gibi görünen
dahil olmak üzere, bu konak hücrede birkaç morulla (ok ile
gösterilen) görülüyor.
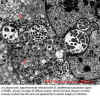 Deneysel E. chaffeensis (HOME etkeni) ile enfekte bir hücre
kültüründe, farklı boyutlarda morula görülüyorr. Küçük morullalar (Beyaz
oklar ile gösterilen) birkaç RC içerirler ve muhtemelen enfeksiyon
erken döneminde görünmektedir.
Deneysel E. chaffeensis (HOME etkeni) ile enfekte bir hücre
kültüründe, farklı boyutlarda morula görülüyorr. Küçük morullalar (Beyaz
oklar ile gösterilen) birkaç RC içerirler ve muhtemelen enfeksiyon
erken döneminde görünmektedir.
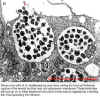 E. chaffeensis yoğun çekirdekli hücreleri, morula ve konak hücre
sitoplazmik membranının rüptürünü takiben konakçı hücreden çıkarken
görülüyor. Bu Ehrlichia'lar şimdi diğer konakçı hücreleri enfekte
etmeye devam edecektir veya bir beslenen kene tarafından
yutulacaktır böylece enfeksiyon yayılacaktır.
E. chaffeensis yoğun çekirdekli hücreleri, morula ve konak hücre
sitoplazmik membranının rüptürünü takiben konakçı hücreden çıkarken
görülüyor. Bu Ehrlichia'lar şimdi diğer konakçı hücreleri enfekte
etmeye devam edecektir veya bir beslenen kene tarafından
yutulacaktır böylece enfeksiyon yayılacaktır.
|
| |
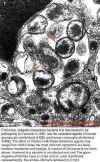 Belirli sayıda bakteri enfekte olmuş bir konak hücresi vakuolünde
toplanır. Gram negatif Ehrlichia'nın bir iç ve oklarla temsil
edilen bir dış zarı var. (Tüm çubuklar 0,5 mm temsil etmektedir)
Belirli sayıda bakteri enfekte olmuş bir konak hücresi vakuolünde
toplanır. Gram negatif Ehrlichia'nın bir iç ve oklarla temsil
edilen bir dış zarı var. (Tüm çubuklar 0,5 mm temsil etmektedir) |
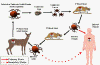 Şekil 13
Şekil 13
İnsan Granüloktik Erlihyozu ajanı için önerilen yaşam döngüsü
CDC
|
Ehrlichia ewingii ve
Anaplasma phagocytophilum (human granulocytic ehrlichiosis)
Klinik sendromlar
Hastalık daha yüksek olabilen ölüm oranı (%10) hariç, insan
monositik erlihyozuna benzer.
Laboratuvar tanısı
E. chaffeensis’ile aynıdır
Tedavi, korunma ve kontrol
E. chaffeensis’ile aynıdır
|
Şekil 14
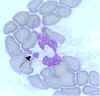 İnsan granülositik ehrlichiosis'e (HGE)
neden olan patojen, öncelikle granülositler (nötrofil ve nadiren
eozinofiller) enfekte eder. Patojen genellikle HGE etkeni veya HGE'nin
etkeni olarak anılır. A. phagocytophilum ve E. equi türler
çok benzer ya da olasılıkla aynıdır. (Morula nötrofil sitoplazmasında)
İnsan granülositik ehrlichiosis'e (HGE)
neden olan patojen, öncelikle granülositler (nötrofil ve nadiren
eozinofiller) enfekte eder. Patojen genellikle HGE etkeni veya HGE'nin
etkeni olarak anılır. A. phagocytophilum ve E. equi türler
çok benzer ya da olasılıkla aynıdır. (Morula nötrofil sitoplazmasında)
CDC |
 Karaayak kenesi (Ixodes scapularis)
Karaayak kenesi (Ixodes scapularis)
CDC
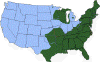 Karaayak kenesinin
yaklaşık
dağılımı
Karaayak kenesinin
yaklaşık
dağılımı
CDC
 Batı karaayak kenesi (Ixodes pacificus)
Batı karaayak kenesi (Ixodes pacificus)
CDC
|
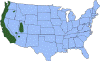 Şekil
15 Şekil
15
Batı karaayak kenesinin yaklaşık Dağılımı
CDC |
Ehrlichia sennetsu
(Sennetsu (ilerleyen) ateş)
Klinik sendromlar
Hastalık; uyuşukluk, servikal lenfadenopati, ateş, periferik kan
mononükleer hücreleri ve atipik lenfositlerin sayısında artış ile
bulaşıcı mononükleoza benzer.
Laboratuvar tanısı
Serolojik testleri vardır
Tedavi
Tetrasiklin kullanılmaktadır ancak, hastalık, hiçbir ölüm ve ciddi
komplikasyonlar görülmez, iyi huyludur.
|
|
|
COXIELLA
Coxiella burnetii (Q ateşi)
[Q, (QUERY:ŞÜPHE, KUŞKU)]
Çoğalma
C. burnetii makrofajları (sekil 16) enfekte eder ve
fagolizozom içinde hayatta kalırlar ve çoğalırlar. Bakteri hücre
ve fagolizozomların parçalanması ile serbest kalır.
Patogenezis ve immunite
Enfeksiyon havadaki partiküllerin solunmasıyla bulaşır.
Organizma akciğerlerde çoğalır ve diğer organlara yayılır.
Pnömoni ve granülomatöz hepatit ağır enfeksiyonu olan hastalarda
görülür. İmmun kompleksler, kronik hastalığın patogenezde rol
oynayabilir. C burnetii'nin LPS'lerinde faz değişimi olabilir.
Akut hastalıkta, antikorlar faz II antijenine karşı üretilir.
Kronik olarak enfekte hastalarda, antikorlar hem faz I hemde faz
II antijenlerine karşı oluşmaktadır. Hücresel bağışıklık
hastalığın iyileşmesinde önemlidir.
Epidemiyoloji
C. burnetii çevre koşullarına son derece kararlı ve "spor
gibi" özelliklere sahiptir. C. burnetii geniş bir yelpazede;
keçi, koyun, sığır ve kediler dahil olmak üzere birçok hayvanda
bulunur. Organizma plasentada ve enfekte hayvanların
dışkılarında bulunur. Organizmalar, enfeksiyon için bir odak
noktası olan, kontamine toprakta uzun süre kalabilirler. C.
burnetii ayrıca süte geçirilir ve pastörize olmayan süt tüketen
insanlara bulaşabilir. Eklembacaklılar, insanlara C burnetii'yi
bulaştırmak için yaygın vektörler değildirler ama, keneler
veterinerlik türler arasında bulaşım için primer bir vektördür.
C. burnetii dünyada
yaygın bulunur ve enfeksiyon küçük çiftçiler, veterinerler,
mezbaha işçileri ve diğer sığır ve hayvancılık uğraşanlarında
yaygındır.
Klinik sendromlar
Hastalık hafif ve asemptomatik olabildiğinden genellikle tanı
konulmayabilir. Hastalık akut ya da kronik olabilir. Akut Q
Ateşi, hasta; baş ağrısı, ateş, titreme ve kas ağrısı ile
başvururlar. Solunum semptomları genellikle hafiftir ("atipik
pnömoni"). Hepatomegali ve splenomegali görülebilir. Granülomlar
Q ateşi geçiren bir çok hastanın histolojik kesitlerinde
görülebilir. Kronik Q ateşi, genellikle hasarlı kalp
kapakçığıyle tipik endokardit olarak görülür. Kronik Q ateşinin
prognozu iyi değildir.
Laboratuvar tanısı
Q ateşi teşhis etmek için en yaygın olarak seroloji kullanılır.
Faz II antijenine karşı gelişen antikorlar akut hastalığı teşhis
etmek, hem faz I hemde faz II antijenlerine karşı gelişen
antikorlar kronik hastalığı teşhis etmek için kullanılır.
Tedavi, korunma ve kontrol
Tetrasiklin, akut Q ateşini tedavi etmek için kullanılır. Kronik
hastalık antibiyotik kombinasyonu ile tedavi edilmektedir.
Avusturalya gibi bazı ülkelerde bir aşı kullanılabilir ancak,
Amerika Birleşik Devletleri'nde kullanılmak üzere
onaylanmamıştır.
|
 Şekil 16
Şekil 16
Makrofajlarda Coxiella enfeksiyonu
|
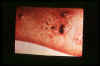 Şekil 17 Bartonellosis - Bartonella bacilliformis'in neden olduğu
ve Güney Amerika'da bulunan bir bakteriyel enfeksiyon. Eenfeksiyon hem
akut ateşli anemi (Oroya ateşi) hemde kronik deri döküntüsü olarak (Verruga
peruana) oluşabilir.
Şekil 17 Bartonellosis - Bartonella bacilliformis'in neden olduğu
ve Güney Amerika'da bulunan bir bakteriyel enfeksiyon. Eenfeksiyon hem
akut ateşli anemi (Oroya ateşi) hemde kronik deri döküntüsü olarak (Verruga
peruana) oluşabilir.
© Dr V. Lloyd, Mount Allison University
|
BARTONELLA
Mikrobiyoloji
Bartonella’lar, kültüründe üremesi zor olan, küçük, Gram-negatif,
aerobik bakterilerdir. Pek çok farklı hayvanlarda bulunur ancak hayvanlarda
hiçbir görülen hastalığa neden olmaz. İnsan hastalığında vektörlerin
böçekler olduğu düşünülmektedir. Bazı türler sadece eritrositleri enfekte
edebilirken diğerleri konak hücrelerini enfekte edebilir. Tablo 4 (Murray ve
ark., Tıbbi Mikrobiyoloji'den uyarlanmıştır) Organizmalar ve onların neden
olduğu hastalıklar özetlemektedir.
|
Tablo 4 |
|
Organizma |
Hastalık |
|
B. quintana
(eskiden Rochalimaea
quintana) |
Siper ateşi (incik kemiği ateşi, 5 gün ateşi), basilli
anjiomatozis, basilli purpuralı endokardit |
|
B. henselae |
Kedi tırmığı hastalığı, basilli anjiomatozis, basilli
purpuralı endokardit |
|
B. bacilliformis |
Oroya ateşi (bartonellosis, Carrion hastalığı) |
|
B. elizabethae |
Endokardit (nadir) |
Bartonella quintana (Siper ateşi)
Epidemiyoloji
Siper ateşi savaş ile ilişkili bir hastalıktır. Vektör, insan
vücut bitidir ve insanlardan başka bilinen rezervuar
bulunmamaktadır. Bitlerde transovarial bulaşma oluşmaz.
Organizma bitin dışkılarında bulunur ve kaşınırken çizilme
aracılıgıyla insanlara aşılanır. Döngü insan-bit-insan
şeklindedir.
Klinik sendromlar
B. quintana ile enfeksiyon asemptomatik ile ciddi
zayıflatıcı hastalığa kadar görülebilir. Semptomlar; ateş,
titreme, baş ağrısı ve tibiadaki şiddetli ağrıdır. Vücutta bir
makülopapüler döküntü görülebilir veya görünmeyebilir.
Semptomlar beş gün aralarla yeniden tekrarlarlar ve bu nedenle
hastalığa ayrıca beş gün ateşi de denir. Ölüm oranları çok
düşüktür.
Laboratuvar tanısı
Serolojik testleri vardır fakat, sadece referans laboratuarlarda
bulunur. PCR tabanlı testler geliştirilmektedir.
Tedavi, korunma ve
kontrol
Siper ateşinin tedavisi için değişik antibiyotikler
kullanılmıştır. İnsan vücut bitinin kontrolü korunma için en iyi
yöntemdir.
|
| |
Bartonella henselae
- (Kedi tırmığı hastalığı)
Epidemiyoloji
Kedi tırmığı hastalığı kedilerle temastan (tırmalama çizikleri,
olası kedi piresi ile ısırıklar) sonra bulaşır.
Klinik sendromlar
Hastalık genellikle, kronik bölgesel lenfadenopati ile
karakterize ve benigndir.
Laboratuvar tanısı
Serolojik testleri vardır Tedavi
Kedi tırmığı hastalığının antimikrobiyal tedaviye cevap
vermediği görülmektedir.
|
|
|
 Mikrobiyoloji ve İmmünoloji On-line, Bakteriyoloji Bölümüne Dönünüz
Mikrobiyoloji ve İmmünoloji On-line, Bakteriyoloji Bölümüne Dönünüz
This page last changed on
Sunday, March 06, 2016
Page maintained by
Richard Hunt
|

 Endotel hücrenin yüzeyine Rickettsia'nın tutunması,
rickettsia-tarafından uyarılan fagositoz yoluyla hücre içine girişini
takip eder. Fagositoz ardından, fagosom membran (ok) kaybolur ve
Rickettsia konak hücre sitoplazması içine kaçar.
Endotel hücrenin yüzeyine Rickettsia'nın tutunması,
rickettsia-tarafından uyarılan fagositoz yoluyla hücre içine girişini
takip eder. Fagositoz ardından, fagosom membran (ok) kaybolur ve
Rickettsia konak hücre sitoplazması içine kaçar. Şekil 3
Şekil 3
 Şekil
5
Şekil
5 Şekil 7
Şekil 7 Şekil
9
Şekil
9 Şekil
10
Şekil
10 ABD’de rapor edilen Erlihyoz vakaları CDC
ABD’de rapor edilen Erlihyoz vakaları CDC Ehrlichiosis olan bir hastada kemik iliği lökositlerinde morula
elektron-fotomikrografıdır. Oklar bireysel Ehrlichia işaret
ediyor
Ehrlichiosis olan bir hastada kemik iliği lökositlerinde morula
elektron-fotomikrografıdır. Oklar bireysel Ehrlichia işaret
ediyor Belirli sayıda bakteri enfekte olmuş bir konak hücresi vakuolünde
toplanır. Gram negatif Ehrlichia'nın bir iç ve oklarla temsil
edilen bir dış zarı var. (Tüm çubuklar 0,5 mm temsil etmektedir)
Belirli sayıda bakteri enfekte olmuş bir konak hücresi vakuolünde
toplanır. Gram negatif Ehrlichia'nın bir iç ve oklarla temsil
edilen bir dış zarı var. (Tüm çubuklar 0,5 mm temsil etmektedir) Şekil 13
Şekil 13 İnsan granülositik ehrlichiosis'e (HGE)
neden olan patojen, öncelikle granülositler (nötrofil ve nadiren
eozinofiller) enfekte eder. Patojen genellikle HGE etkeni veya HGE'nin
etkeni olarak anılır. A. phagocytophilum ve E. equi türler
çok benzer ya da olasılıkla aynıdır. (Morula nötrofil sitoplazmasında)
İnsan granülositik ehrlichiosis'e (HGE)
neden olan patojen, öncelikle granülositler (nötrofil ve nadiren
eozinofiller) enfekte eder. Patojen genellikle HGE etkeni veya HGE'nin
etkeni olarak anılır. A. phagocytophilum ve E. equi türler
çok benzer ya da olasılıkla aynıdır. (Morula nötrofil sitoplazmasında)
 Şekil
15
Şekil
15  Şekil 16
Şekil 16 Şekil 17 Bartonellosis - Bartonella bacilliformis'in neden olduğu
ve Güney Amerika'da bulunan bir bakteriyel enfeksiyon. Eenfeksiyon hem
akut ateşli anemi (Oroya ateşi) hemde kronik deri döküntüsü olarak (Verruga
peruana) oluşabilir.
Şekil 17 Bartonellosis - Bartonella bacilliformis'in neden olduğu
ve Güney Amerika'da bulunan bir bakteriyel enfeksiyon. Eenfeksiyon hem
akut ateşli anemi (Oroya ateşi) hemde kronik deri döküntüsü olarak (Verruga
peruana) oluşabilir. 




























