|
x |
x |
|
 |
 |
|
INFEKČNÉ CHOROBY |
BAKTERIOLÓGIA |
IMUNOLÓGIA |
MYKOLOGIA |
PARAZITOLÓGIA |
VIROLÓGIA |
|
|
 |
UNIVERZITA KOMENSKÉHO V
BRATISLAVE
JESSENIOVA LEKÁRSKA FAKULTA V MARTINE
Ústav mikrobiológie a imunológie
Sklabinská 26 , 036 01 Martin
|
 |
BAKTERIOLÓGIA
– KAPITOLA SEDEMNÁSŤ
ZOONÓZY
LISTERIA, FRANCISELLA, BRUCELLA, BACILLUS A YERSINIA
Dr Abdul Ghaffar
Department of Pathology, Microbiology and Immunology
University of South Carolina School of Medicine
Columbia, South Carolina Překlad: Elena Novakova,
MD, PhD
Institute of Microbiology and Immunology
Jessenius Faculty of Medicine in Martin
Comenius University in Bratislava
|
|
|
|
ALBÁNČINA |
|
ŠPANIELČINA |
|
ANGLIČTINA |
|
|
|
Dajte vedieť, čo si myslíte
SPATNÁ VAZBA |
|
HĽADAJ |
|

 |
|
Logo image © Jeffrey
Nelson, Rush University, Chicago, Illinois and
The MicrobeLibrary |
|
|
|
 Arnold Boecklin: The Plague 1898. Tempera na dreve, Múzeum umenia,
Basel
Arnold Boecklin: The Plague 1898. Tempera na dreve, Múzeum umenia,
Basel |
|
CIEĽ VÝUČBY
Poznať všeobecnú morfológiu a fyziológiu mikroorganizmov
Poznať epidemiológiu a klinické príznaky
Pochopiť mechanizmy patogenézy
Poznať diagnostické, terapeutické a preventívne postupy
|
Zoonózy
označujú ochorenia, ktoré postihujú primárne zvieratá a môžu byť prenesené na
ľudí následkom priameho alebo nepriameho kontaktu s infikovanou zvieracou
populáciou.
BRUCELÓZA
Morfológia
a fyziológia:
Brucella
je gramnegatívny, nepohyblivý, kokobacil. Je to striktný aeróbny
mikroorganizmus a rastie veľmi pomaly (rastovo
náročný)
na krvnom agare. U hostiteľa prežívajú brucely ako fakultatívne intracelulárne
patogény.
Epidemiológia, prenos a príznaky
Brucelóza je primárne ochorenia zvierat a postihuje orgány bohaté na sacharid
erytritol
(mliečna žľaza, maternica, epididymis a iné). Mikroorganizmus sa lokalizuje
v týchto zvieracích orgánoch a spôsobuje neplodnosť, sterilitu,
mastitídu,
potraty alebo vedie k nosičstvu. Ľudia, ktorí sú v úzkom kontakte
s infikovanými zvieratami (pracovníci kafilérií, veterinári, farmári, pracovníci
mliekarní) sú ohrození vývojom febris undulans (undulujúca horúčka).
V USA sa vyskytuje 100 - 200 prípadov brucelózy, hoci na svete sa odhaduje
incidencia 500 000. Známe sú štyri druhy rodu Brucella, ktoré infikujú
ľudí: B. abortus (dobytok), B. suis (ošípané), B. melitensis
(kozy/ ovce) a B. canis (psy). Hoci bola brucelóza eradikovaná vo väčšine
vyspelých krajín prostredníctvom očkovania zvierat, toto ochorenie pretrváva
v niektorých menej vyvinutých a rozvojových krajinách.
|
|
|
 Brucella abortus
- gramnegatívny kokobacil, prokaryotická bunka; spôsobuje spontnánne aborty
hovädzieho dobytka rýchlym rastom v prítomnosti erytritolu (produkovaný
placentov). SEM x 29,650
Brucella abortus
- gramnegatívny kokobacil, prokaryotická bunka; spôsobuje spontnánne aborty
hovädzieho dobytka rýchlym rastom v prítomnosti erytritolu (produkovaný
placentov). SEM x 29,650
©
Dennis Kunkel Microscopy, Inc.
Použitie s dovolením
 Brucella spp.
slabo sa
farbiaci malý gramnegatívny kokobacil (0,5-0,7 x 0,6-1,5 mikrometer),
obvykle ako samostatné bunky a vyzerajúce ako „jemný piesok“.
Brucella spp.
slabo sa
farbiaci malý gramnegatívny kokobacil (0,5-0,7 x 0,6-1,5 mikrometer),
obvykle ako samostatné bunky a vyzerajúce ako „jemný piesok“.
CDC
 Brucella
spp. Charakteristiky kolónií:
Brucella
spp. Charakteristiky kolónií:
A. Náročné, obvykle
neviditeľné po 24h.
B. Rastú pomaly na väčšine štandardných laboratórnych médií (napr.
ovčia krv, čokoládový a tryptózový sójový agar). Ako hrot špendlíka,
hladké, celé priesvitné, nehemolytické po 48h.
CDC
 Brucella ovis
v epididymis.
Brucella ovis
v epididymis.
© Bristol Biomedical Image Archive, University of
Bristol. Použité s dovolením |
B. abortus
a B. canis spôsobujú mierne hnisavé horúčkovité ochorenie. B. suis
spôsobuje závažnejšiu
hnisavú
infekciu, ktorá môže viesť k deštrukcii lymforetikulárnych orgánov a obličiek.
B. melitensis je príčinou najťažšej pretrvávajúcej a opakujúcej sa
choroby. Baktéria vstupuje do ľudského hostiteľa cez sliznice orofaryngu
(ingescia/ inhalácia), cez poškrabanú kožu alebo spojovku. Obvykle sa infekcia
vyskytuje po priamom kontakte s infikovaným materiálom, hoci sa môže vyskytnúť
aj po požití mlieka alebo mliečnych produktov. Baktérie sú pohltené neutrofilmi
a monocytmi a lokalizujú sa v regionálnych lymfatických uzlinách, kde
intracelulárne proliferujú. Ak mikroorganizmus (Brucella) nie je
deštruovaný alebo zachytený v lymfatických uzlinách, baktéria sa uvoľní
s lymfatickej uzliny a spôsobí septikémiu. Mikroorganizmus migruje do ostatných
lymforetikulárnych orgánov (slezina, kostná dreň, pečeň, testes), spôsobí
tvorbu granulómov a/ alebo mikroabscesov. Symptómy zahŕňajú horúčku, triašku,
potenie, únavu, myalgiu, výraznú svalovú slabosť a anorexiu. Často sú postihnuté
kĺby. Brucelóza môže prebiehať ako akútne alebo chronické ochorenie. Fatálne
prípady (0 – 3 %) spôsobuje obvykle endokarditída.
Patogenéza
Symptómy
pri brucelóze sú spôsobené prítomnosťou mikroorganizmu a objavujú sa 2 - 4
týždne po expozícii (niekedy až po 2 mesiacoch). Pokiaľ je vo fagolyzozóme
B.
abortus, uvoľňuje 5'-guanín a adenín monofosfát, ktoré sú schopné inhibovať
degranuláciu granúl obsahujúcich peroxidázu a inhibujú
myeloperoxidáza-halogenidový systém bakteriálneho zabíjania. Intracelulárne
prežívanie baktérie má za následok tvorbu granulómov v RES a tkanivové
poškodenie prostredníctvom hypersenzitívnych reakcií, obvykle IV. typu.
Diagnostika
Diagnostika
je založená na dlhodobo (minimálne týždeň) prítomnej undululúcej horúčke (febris
undulans),
myalgii,
artralgii
a anamnéze expozície (kontakt so zvieraťom alebo konzumácia materiálu
z infikovaných zvierat). Definitívna diagnóza môže byť stanovená kultiváciou
krvných vzoriek na krvou obohatených médiách. Kultivačne náročný mikroorganizmus
rastie veľmi pomaly (4 - 6 týždňov v hemokultúre). B. abortus (ale iné
brucely nie) rastie lepšie v atmosfére obsahujúcej 5 % CO2. Na krvnom
agare produkuje biele lesklé kolónie. Sérologické metódy sa používajú na
potvrdenie suspektných prípadov.
Prevencia a
liečba
Dlhodobá
liečba rifampicínom, ktorý penetruje do bunky v kombinácii so streptomycínom
alebo tetracyklínovými antibiotikami, sa používa na liečbu infekcií spôsobených
brucelami. Kontrolné opatrenia zahŕňajú očkovanie zvierat a vyhýbanie sa
infikovaným materiálom.
|
|
|
|
 Dr. Alexandre Yersin pred Národnou karanténnou stanicou, Shanghai
Station, 1936.
Dr. Alexandre Yersin pred Národnou karanténnou stanicou, Shanghai
Station, 1936.
 Výskyt moru na svete 1998. Výskyt moru na svete 1998.
CDC
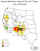 Distribúcia moru v USA podľa štátov.
Distribúcia moru v USA podľa štátov.
CDC
 Yersinia pestis
- palička prokaryotická (deliaca sa); spôsobuje bubonický mor (SEM
x20,800).
Yersinia pestis
- palička prokaryotická (deliaca sa); spôsobuje bubonický mor (SEM
x20,800).
©
Dennis Kunkel Microscopy, Inc.
Použité s dovolením
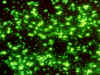 Yersinia pestis.
Identifikácia dôkazom fluorescenčnými protilátkami.
Yersinia pestis.
Identifikácia dôkazom fluorescenčnými protilátkami.
CDC
|
MOR
Mor je
spôsobený baktériou Yersinia pestis a je to ochorenie známe zo
stredoveku ako čierna smrť. Bolo to preto, lebo infekcia často viedla ku
gangréne a sčerneniu rôznych častí tela. Krehkosť kapilár má za následok
krvácanie do kože, čoho výsledkom sú čierne petechie.
Morfológia a fyziológia
Yersinia pestis
je
pleomorfná
gramnegatívna, bipolárne sa farbiaca, fakultatívne aerobná, nepohyblivá
palička. Optimálna teplota pre rast je 28 °C. Je to fakultatívne
intracelulárna baktéria.
Epidemiológia, prenos a príznaky
Tri
dokumentované pandémie moru (čierna smrť) boli zodpovedné za smrť miliónov
ľudí. V súčasnosti sa stále vyskytujú sporadické infekcie. V USA sa
vyskytuje zvierací (lesný)
mor vo viacerých krajinách Západu, obvykle postihuje malé hlodavce
a mäsožravce, ktoré sa živia týmito hlodavcami.
Ľudia
sa infikujú blchami parazitujúcimi na infikovaných hlodavcoch alebo
kontaktom s infikovanými zvieratami. Blcha získa Y. pestis počas
sania krvi infikovaným hlodavcom. Tieto mikroorganizmy strácajú svoje
puzdro, rozmnožujú sa v črevnom trakte a čiastočne blokujú proventrikulus.
Počas sania krvi ľudskému hostiteľovi blcha vracia niektoré mikroorganizmy
do rany. Väčšina neopuzdrených mikroorganizmov je fagocytovaná a zničená
neutrofilmi. Niektoré mikroorganizmy sú ale zachytené histiocytmi, ktoré nie
sú schopné ich usmrtiť a umožnia im znovu nasyntetizovať ich puzdro
a rozmnožiť sa. Opuzdrené mikroorganizmy sú po uvoľnení z histiocytov
rezistentné na fagocytózu a usmrtenie neutrofilmi. Následná infekcia sa šíri
do regionálnych lymfatických uzlín, ktoré sa stávajú horúce, opuchnuté,
citlivé a krvácajúce. Uzliny sa stávajú charakteristickými čiernymi bubo,
z čoho pochádza aj názov choroby bubonický mor. V priebehu hodín sa
mikroorganizmus šíri do sleziny, pečene a pľúc a vzniká pneumónia. Ak sa
dostane do krvi, spôsobí difúznu intravaskulárnu koaguláciu s následnou
tvorbou intravaskulárnych trombov a purpurových lézií po celom tele. Ak sa
nezačne s liečbou, infekcia má vysokú mortalitu (až 90 %). Mikroorganizmus
prítomný vo vydychovaných kvapôčkach infikuje ďalších ľudí v okolí a spôsobí
pneumonický mor, ktorý je epidemiologicky závažnejší a má 100 %
mortalitu.
Patogenéza
Mnoho
faktorov zohráva priamu alebo nepriamu úlohu v patogenéze infekcie Y.
pestis.
Odpoveď
pri nízkom kalciu (lcr)
Plazmidom kódovaný gén umožňuje, aby mikroorganizmus rástol v prostredí
(intracelulárne) s nízkym obsahom Ca++ . Takisto koordinuje
produkciu viacerých ďalších faktorov virulencie, akými sú V, W a yops (Yersinia
outer proteins).
V a W
proteíny
Tieto plazmidom kódované proteíny súvisia s rýchlou proliferáciou a
septikémiou.
Yops
Skupina 11 proteínov, ktoré sú kódované plazmidmi, sú základom patogenézy
u hlodavcov a sú zodpovedné za cytotoxicitu, inhibíciu migrácie fagocytov
a procesu pohltenia, ako aj agregácie doštičiek.
F-1
antigén obalu
Je to proteínovo-polysacharidový komplex, ktorý sa významne prejavuje pri 37
°C v cicavčom hostiteľovi, ale nie v bloche. Má antifagocytárne vlastnosti.
Koaguláza a aktivátor plazminogénu
Obidva sú plazmidom kódované proteíny.
Koagulázy
sú zodpovedné za tvorbu mikrotrombov a aktivátor
plazminogénu
podporuje disemináciu mikroorganizmu. Deštruuje C3b na bakteriálnom povrchu,
čím sa zoslabí fagocytóza.
|
|
|
 Morové oblečenie. Plášť bol naplnený sladko zapáchajúcim olejom a octom, aby
zastreli zápach obetí moru. Hoci lekári v 14. storočí nepoznali príčinu,
oblečenie mohlo byť do určitej miery účinné tým, že bránilo kontaktu
s muchami.
Morové oblečenie. Plášť bol naplnený sladko zapáchajúcim olejom a octom, aby
zastreli zápach obetí moru. Hoci lekári v 14. storočí nepoznali príčinu,
oblečenie mohlo byť do určitej miery účinné tým, že bránilo kontaktu
s muchami.
Vľavo:
Bubonický mor od Ely Janis
Vpravo: © Bristol Biomedical Image Archive, University of Bristol. Použité
s dovolením
|
Diagnóza
Diagnóza je založená na objavení sa bubo. Je potvrdená kultiváciou aspirátu
z lymfatických uzlín. Je nevyhnutná extrémna opatrnosť pri manipulácii so
vzorkou, pretože vzorky sú vysoko infekčné.
Prevencia a liečba
Hospitalizácia a striktná izolácia sú pravidlom. Streptomycín
a tetracyklínové ATB sú vysoko účinné. K dispozícii je účinná vakcína
(obsahuje formaldehydom usmrtenú baktériu), ale odporúčaná je len pre ľudí,
ktorí sú pod vysokým rizikom. Ochorenie podlieha medzinárodným karanténnym
opatreniam a povinné je hlásenie prípadov. Kontrola mestského moru je
založená na likvidácii bĺch a hlodavcov.
|
|
|
 Samička Xenopsylla cheopsis (orientálna krysia blcha) nacicaná krvou. CDC
Samička Xenopsylla cheopsis (orientálna krysia blcha) nacicaná krvou. CDC
 Opuchnuté lymfatické uzliny (bubo) spôsobené baktériou moru – bubonický mor.
CDC
Opuchnuté lymfatické uzliny (bubo) spôsobené baktériou moru – bubonický mor.
CDC
 Waysonovo farbenie
Yersinia pestis. Všimnite si charakteristický
vzhľad baktérie v tvare zatváracieho špendlíka. CDC
Waysonovo farbenie
Yersinia pestis. Všimnite si charakteristický
vzhľad baktérie v tvare zatváracieho špendlíka. CDC
 Symptómy moru u tohto pacienta zahŕňajú ingvinálne bubo. CDC
Symptómy moru u tohto pacienta zahŕňajú ingvinálne bubo. CDC
 Histopatologický obraz sleziny pri ľudskom more – nekróza a
Yersinia
pestis. CDC/Dr. Marshall Fox
Histopatologický obraz sleziny pri ľudskom more – nekróza a
Yersinia
pestis. CDC/Dr. Marshall Fox
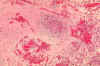 Histopatológia lymfatických uzlín pri smrteľnom ľudskom more – nekróza drene
uzliny s prítomnosťou tekutiny a Yersinia pestis. CDC/Dr. Marshall
Fox
Histopatológia lymfatických uzlín pri smrteľnom ľudskom more – nekróza drene
uzliny s prítomnosťou tekutiny a Yersinia pestis. CDC/Dr. Marshall
Fox
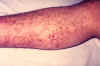 Krehkosť kapilár je jedným z prejavov infekcie morom, viditeľná na nohe
infikovaného pacienta. CDC
Krehkosť kapilár je jedným z prejavov infekcie morom, viditeľná na nohe
infikovaného pacienta. CDC
 Gangréna je jednou z manifestácii moru a je pôvodom názvu „Čierna smrť“,
ktorý sa používal v priebehu vekov. CDC
Gangréna je jednou z manifestácii moru a je pôvodom názvu „Čierna smrť“,
ktorý sa používal v priebehu vekov. CDC
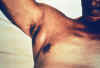 Pacient
s morom so zdurenými lymfatickými uzlinami v axile. CDC
Pacient
s morom so zdurenými lymfatickými uzlinami v axile. CDC
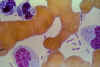 Tmavo zafarbené bipolárne konce baktérieYersinia pestis je jasne
viditeľná pri Wrightovom farbení vzorky krvi u obetí moru.
Tmavo zafarbené bipolárne konce baktérieYersinia pestis je jasne
viditeľná pri Wrightovom farbení vzorky krvi u obetí moru.
 Yersinia pestis
rastie dobre na väčšine obvyklých laboratórnych médií po 48-72 hod.,
šedo-biele až slabo žlté nepriehľadné kolónie, nepravidelného tvaru
„pražených vajec”; alternatívne môžu mať kolónie jasný povrch „vyklepanej
mede”. CDC
Yersinia pestis
rastie dobre na väčšine obvyklých laboratórnych médií po 48-72 hod.,
šedo-biele až slabo žlté nepriehľadné kolónie, nepravidelného tvaru
„pražených vajec”; alternatívne môžu mať kolónie jasný povrch „vyklepanej
mede”. CDC
|
|
|
|
|
 Originálne mikrofotografie Roberta Kocha znázorňujúce bacily antraxu
DOD
Anthrax Program
Originálne mikrofotografie Roberta Kocha znázorňujúce bacily antraxu
DOD
Anthrax Program
 Farbenie podľa Grama - antrax
Farbenie podľa Grama - antrax
DOD Anthrax Program
 Antrax spôsobený Bacillus anthracis (krvný náter).
Antrax spôsobený Bacillus anthracis (krvný náter).
© Bristol
Biomedical Image Archive, University of Bristol. Použité s dovolením |
ANTRAX
Morfológia a fyziológia
Bacillus anthracis
je etiologickým agensom antraxu. Je to grampozitívna, aeróbna, sporulujúca
hrubá palička. Spóry sa vytvárajú v kultúre, v pôde a v tkanivových
vzorkách a exsudátoch uhynutých zvierat, ale nie v krvi alebo
tkanive žijúcich zvierat. Spóry zostávajú životaschopné v pôde aj niekoľko
desiatok rokov.
Epidemiológia, prenos a symptómy
Antrax je najvýznamnejšou chorobou ohrozujúcou bylinožravce (dobytok, ovce
a v menšom rozsahu kone, ošípané a kozy). Ľudia sa infikujú cez kožu (priamy
kontakt s chorými zvieratami, priemyselné spracovanie kože – usní, vlny,
kefy zo štetín alebo z kostnej múčky), inhaláciou (ochorenie
spracovateľov vlny), alebo ingesciou (mäsom chorých zvierat).
|
 Kožný
antrax
Kožný
antrax
DOD Anthrax Program
 Vývoj kožného antraxu.
Vývoj kožného antraxu.
CDC
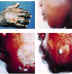 Kožný antrax
Kožný antrax
CDC |
-
Kožný
antrax
predstavuje viac ako 95 % ľudských prípadov. Spóry vstupujú cez malé
poranenia kože, germinujú na vegetatívne bunky, ktoré rýchlo proliferujú
v oblasti brány vstupu. V priebehu niekoľkých dní sa vytvorí malá papula,
ktorá sa postupne mení na vezikulu. Vezikula je naplnená modročiernou
tekutinou. Ruptúra tejto lézie vedie k vytvoreniu čiernej chrasty
príškvar
na spodine s obkolesujúcou zónou
indurácie.
Táto lézia sa nazýva malígna pustula, aj keď sa neprejavuje prítomnosťou
hnisu ani bolesťou. Lézie sa klasicky nachádzajú na rukách, predlaktí alebo
hlave. Invázia do krvného riečiska vedie k systémovej diseminácii baktérie.
-
Pľúcny
antrax
je následkom inhalácie spór B. anthracis, ktoré sú
fagocytované
makrofágmi, kde germinujú a replikujú sa. Postihnuté bunky a mikroorganizmy
sa lokalizujú v lymfatických uzlinách v hiloch, kde sa môže vyskytnúť
hemoragická nekróza. Pacient môže mať horúčku, nevoľnosť, bolesti svalov
a neproduktívny kašeľ. Keď je infekcia prítomná v lymfatických uzlinách
hilu, môže sa šíriť do krvi. Manifestáciou toxémie sú respiračné zlyhanie
a cyanóza. Smrť nastupuje v priebehu 24 hodín. Táto forma antraxu je
významná ako biologická zbraň.
-
Gastrointestinálny antrax
je následkom ingescie mäsa z infikovaných zvierat a vedie k bakteriálnej
proliferácii v GITe, k invázii do epitelu a ulceráciám v sliznici. Šíri sa
inváznym spôsobom do mezenteriálnych lymfatických uzlín a do krvi. Najskôr
dochádza k zvracaniu a hnačke s krvou v stolici. Invázia do krvi súvisí
s celkovou skleslosťou, šokom a smrťou. Vďaka prísnej kontrole sa táto forma
antraxu v USA nevyskytuje.
|
|
|
| |
 Antrax – kožná lézia na tvári muža. CDC
Antrax – kožná lézia na tvári muža. CDC
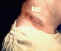 Antrax – kožná lézia na krku muža. CDC
Antrax – kožná lézia na krku muža. CDC
 Ohraničené krvácanie do mukózy a submukózy s degeneráciou arteriol. CDC/Dr.
Marshall Fox
Ohraničené krvácanie do mukózy a submukózy s degeneráciou arteriol. CDC/Dr.
Marshall Fox
 Histopatologický obraz pečene fatálneho ľudského antraxu. Dilatované
sínusoidy, neutrofilný infiltrát. CDC/Dr. Marshall Fox
Histopatologický obraz pečene fatálneho ľudského antraxu. Dilatované
sínusoidy, neutrofilný infiltrát. CDC/Dr. Marshall Fox
 53-ročná žena zamestnaná 10 rokov v oddelení spracovania kozích srstí. Kožný
antrax na pravom líci; 4. deň. CDC
53-ročná žena zamestnaná 10 rokov v oddelení spracovania kozích srstí. Kožný
antrax na pravom líci; 4. deň. CDC
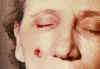 Lézia na 5. deň. CDC
Lézia na 5. deň. CDC
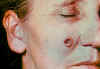 Lézia na 6. deň. CDC
Lézia na 6. deň. CDC
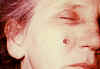 Lézia na 8. deň. CDC
Lézia na 8. deň. CDC
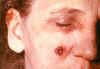 Lézia na 11. deň. CDC
Lézia na 11. deň. CDC
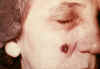 Lézia na 13. deň. CDC
Lézia na 13. deň. CDC
|
| |
| |
|
|
Patogenéza
Faktory
virulencie B. anthracis zahŕňajú viacero exotoxínov a puzdro.
Exotoxín
Plazmidom-kódovaný
termolabilný heterogénny proteínový komplex tvorený 3 súčasťami:
In vivo,
tieto tri faktory účinkujú synergicky (na vyvolanie toxických účinkov).
Protektívny antigén sa viaže na povrchové receptory eukaryotických buniek
a je následne rozložený bunkovými proteázami. Veľká C-terminálna časť PA
zostáva viazaná na receptor a potom sa viaže buď na EF alebo LF a vstúpi do
bunky
endocytózou.
Edematogénny faktor (potom ako vstúpi do bunky) sa viaže a účinkuje ako
adenylcykláza. Letálny faktor účinkuje mechanizmom aktivácie makrofágov
a produkcie cytokínov, ktoré spôsobujú nekrózu, horúčku, šok a smrť.
Individuálne, tri proteíny nemajú známu toxickú aktivitu. Protilátky proti
protektívnym antigénom bránia väzbe PA na bunky, aby sa zastavil vstup EF a
LF.
Puzdro
Puzdro pozostáva z polypeptidu D-glutamovej kyseliny, ktorá je kódovaná
plazmidom a má antifagocytárne vlastnosti. Nie je dobrým
imunogénom.
V prípade ak sa aj nejaké protilátky vytvoria, nie sú protektívne proti
ochoreniu.
Diagnóza
Klinická diagnóza antraxu môže byť potvrdená priamym vyšetrením alebo
kultiváciou. Čerstvé vzorky vezikulárnej tekutiny, tekutina spod chrasty,
krv, slezina alebo aspirát lymfatickej uzliny sa farbia polychrómovou
metylénovou modrou a mikroorganizmus je identifikovaný na základe
charakteristikých tupých zakončení (ako zatvárací špendlík), modro-čiernych
paličiek s ružovým puzdrom. V prípade negatívneho nálezu, je možné vzorku
kultivovať na krvnom agare. Vykultivovaný mikroorganizmus sa farbí pozitívne
farbením podľa Grama a znázorní sa ako tenká palička.
Prevencia a liečba
Antibiotikami voľby sú penicilín a 4-chinolón, ciprofloxacín (Cipro).
Protilátky proti komplexu toxínov sú neutralizujúce a ochranné. Dostupné sú
dve vakcíny. Jedna sa používa na imunizáciu dobytka a ďalších bylinožravcov
a druhá pre ľudí.
|
|
|
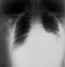 Mediastinálne rozšírenie a pleurálne efúzie na rtg hrudníka pri
inhalačnom antraxe.
Mediastinálne rozšírenie a pleurálne efúzie na rtg hrudníka pri
inhalačnom antraxe.
CDC |
 Antrax, krvná zrazeniny vychádzajúca z konečníka.
Antrax, krvná zrazeniny vychádzajúca z konečníka.
© Bristol Biomedical
Image Archive, University of Bristol. Použité s dovolením |
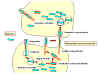 Infekcia
makrofágov alebo parenchýmových buniek baktériou Listeria monocytogenes
Infekcia
makrofágov alebo parenchýmových buniek baktériou Listeria monocytogenes
 Listeria monocytogenes
–
prokaryotická palička, ktorá spôsobuje listeriózu, meningitídu a otravu
z potravín.
Listeria monocytogenes
–
prokaryotická palička, ktorá spôsobuje listeriózu, meningitídu a otravu
z potravín.
©
Dennis Kunkel Microscopy, Inc.
Použité s dovolením
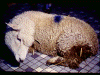 Živá ovca: listerióza.
Živá ovca: listerióza.
© Bristol Biomedical Image Archive, University of
Bristol. Použité s dovolením
 Listeria
monocytogenes
– mikroorganizmy v neutrofiloch (krvný náter).
Listeria
monocytogenes
– mikroorganizmy v neutrofiloch (krvný náter).
© Bristol Biomedical
Image Archive, University of Bristol. Použité s dovolením
 Elektrónová mikroskopia baktérie Listeria monocytogenes s
bičíkmi, zväčšenie 41250X .
Elektrónová mikroskopia baktérie Listeria monocytogenes s
bičíkmi, zväčšenie 41250X .
CDC/Dr. Balasubr Swaminathan; Peggy Hayes; Elizabeth White
 Elektrónová mikrofotografia listerie v tkanive.
Elektrónová mikrofotografia listerie v tkanive.
CDC/Dr. Balasubr Swaminathan; Peggy Hayes; Elizabeth White |
LISTERIÓZA
Morfológia
a fyziológia
L.monocytogenes
je fakultatívne intracelulárny grampozitívny kokobacil, ktorý často rastie
v krátkych retiazkach. Odlišuje sa od ostatných grampozitívnych mikroorganizmov
v tom, že obsahuje molekuly, ktoré sú chemicky a biologicky podobné klasickému
lipopolysacharidu, listeriový LPS. Mikroorganizmus vytvára beta-hemolytické
kolónie na krvnom agare a modrozelené priesvitné kolónie na bezfarebných
médiách. Pri infekcii bunky (makrofágy a parenchýmové bunky), mikroorganizmus
uniká z hostiteľských vakuol (alebo fagozómov) a podstupuje rýchle delenie
v cytoplazme hostiteľských buniek predtým, ako sa opuzdria krátkymi aktínovými
vláknami. Tieto vlákna sa preorganizujú do dlhého vlákna vychádzajúceho len
z jedného konca baktérie. To sprostredkuje pohyb mikroorganizmu v cytoplazme až
na povrch hostiteľskej bunky. Na periférii bunky sa vytvoria výčnelky, ktoré
môžu penetrovať do susedných buniek a umožniť baktérii vstúpiť do nej. Vďaka
tomuto spôsobu intercelulárneho prenosu, mikroorganizmus nie je nikdy exponovaný
extracelulárnemu prostrediu a nie je vystavený humorálnym antibakteriálnym
agensom (napr. komplementu, protilátkam). L. monocytogenes je usmrtená
aktivovanými makrofágmi.
Epidemiológia a príznaky
Listeria
monocytogenes
je všadeprítomný mikroorganizmus nachádzajúci sa v pôde, rastlinách, vode a v
GITe zvierat. Expozícia tomuto mikroorganizmu môže viesť k asymptomatickej
kolonizácii u ľudí. V najväčšom riziku ochorenia sú plody, novorodenci, pacienti
s rakovinou a imunosupresiou. V USA sa zaznamenalo viacero hromadných výskytov
súvisiacich so syrom, nakladanou kapustou, mliekom a mäsom. Mikroorganizmus môže
rásť pri teplote 4 °C, čo znamená, že sa môže replikovať v chladených
potravinách. Laboratórna izolácia je možná technikou chladového
obohatenia.
Listerióza
bola kategorizovaná do 2 foriem: 1) neonatálne ochorenie a 2) ochorenie
dospelých.
Neonatálne
ochorenie
Neonatálne ochorenie sa môže prejaviť v dvoch formách: so skorým nástupom
ochorenia, získaného transplacentárne in utero a s neskorým
nástupom ochorenia získaného pri pôrode alebo v období tesne po pôrode. In utero získaná infekcia (granulomatosis infantiseptica) spôsobuje
abscesy a granulómy vo viacerých orgánoch a veľmi často končí potratom.
Expozícia pri vaginálnom pôrode má za následok ochorenie s neskorým nástupom,
ktoré sa prejaví meningitídou alebo meningoencefalitídou so sepsou v priebehu 2
až 3 týždňov.
Ochorenie
dospelých
Infekcia u normálnych imunokompetentných dospelých má za následok samolimitujúce
chrípkovité ochorenie a/ alebo mierne gastrointestinálne príznaky. Zimnica
a horúčka súvisia s bakteriémiou. U imunosuprimovaných jedincov môže vyvolať
závažné ochorenie vedúce k meningitíde. Je jednou z najčastejších príčin
bakteriálnej meningitídy u pacientov s rakovinou a pacientov po transplantácii
obličky. U starších môžu zostať včasné symptómy nepovšimnuté a infekcia môže
viesť ku akútnej manifestácii sepsy (vysoká horúčka, hypotenzia). Komplikáciou
bakteriémie je endokarditída.
Patogenéza
Listeriolyzín O, β-hemolyzín je podobný streptolyzínu a pneumolyzínu. Je
produkovaný virulentnými kmeňmi. Ničí fagocytujúcu vakuolu a je nástrojom
intercelulárneho prenosu mikroorganizmu. Toxín je oxygén-labilný a imunogénny.
Diagnostika
Listerióza
je suspektná pri monocytóze v krvi a CSF. Mikroorganizmus je možné izolovať na
bežných kultivačných médiách (krvný agar).
Liečba a
kontrola
Účinné sú
penicilín (ampicilín) samostatne alebo v kombinácii s gentamycínom. Imunita je
sprostredkovaná bunkami.
|
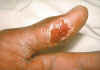 Palec s kožným vredom pri tularémii.
Palec s kožným vredom pri tularémii.
CDC/Emory U./Dr. Seller
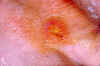 Tularémia – lézia na koži chrbta pravej ruky.
CDC/Dr. Brachman Tularémia – lézia na koži chrbta pravej ruky.
CDC/Dr. Brachman
 Francisella tularensis
- baktéria zafarbená metylénovou modrou.
Francisella tularensis
- baktéria zafarbená metylénovou modrou.
CDC/Dr. P. B. Smith
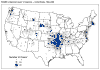 Hlásené prípady tularémie v USA 1990-2000.
CDC
Hlásené prípady tularémie v USA 1990-2000.
CDC
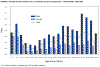 Priemerná ročná incidencia tularémie podľa pohlavia a veku - USA
1990-2000.
CDC
Priemerná ročná incidencia tularémie podľa pohlavia a veku - USA
1990-2000.
CDC
|
TULARÉMIA
Morfológia
a fyziológia
Francisella
tularensis
je malý gramnegatívny, nepohyblivý, opuzdrený, pleomorfný kokobacil (krátka
palička). Je to fakultatívny intracelulárny parazit, ktorý na bežných médiách
rastie slabo alebo vôbec nerastie a vyžaduje špeciálny krvný agar obsahujúci
glukózu a cysteín. Pri manipulácii so vzorkou je potrebná opatrnosť, pretože na
vznik ochorenia je potrebná len nízka infekčná dávka.
Epidemiológia a symptómy
Francisella
tularensis
je etiologickým agensom tularémie (v USA podlieha hláseniu). Na rozdiel od moru
sa tularémia vyskytuje vo všetkých 50 štátoch USA. Jeho primárnym rezervoárom sú
králiky, zajace a kliešte. Človek najčastejšie získa tularémiu prostredníctvom
poštípania hmyzom (primárne kliešte, ale aj rôzne muchy, alebo komáre) alebo
manipuláciou s infikovanými tkanivami zvierat. Ľudské ochorenie (králičia nemoc)
je charakterizovaná fokálnym vredom v mieste vstupu mikroorganizmu a zväčšením
regionálnych lymfatických uzlín.
Na vznik
ochorenia u človeka stačí len 10 - 50 baktérií, ak sú inhalované alebo
aplikované intradermálne. Pri perorálnej infekcii je potrebné väčšie inokulum
(~108 mikroorganizmov). V mieste vstupu sa obvykle vytvoria malé
kožné morfy (papuly). Neskôr sa vytvoria vredy sprevádzané horúčkou, zimnicou,
nevoľnosťou, únavou a obvykle aj lymfadenopatiou. Bežná je bakteriémia. Bacily
rastú intracelulárne v retikuloendotelovom systéme. Diseminácia mikroorganizmu
krvným riečiskom umožní vytvorenie fokálnych lézií vo viacerých orgánoch.
Pacienti majú obvykle viacero klinických syndrómov. Najčastejšou formou
je ulceroglandulárna forma (70 – 85 %). Pri nej sú prítomné v mieste
infekcie bolestivé ulcerózne útvary s nekrotickým stredom. Ďalšími formami sú
glandulárna (lymfadenopatia bez vredu), tyfoidná, pľúcna, okuloglandulárna a
vzácne orofaryngeálna (faryngotonzilitída s lymfadenopatiou).
Patogenéza
Puzdro
mikroorganizmu je dôvodom rezistencie na fagocytózu. Intracelulárne
mikroorganizmy odolávajú usmrteniu fagocytózou a rozmnožujú sa. Väčšina
mikroorganizmov odoláva fagocytóze a rozmnožuje sa. Väčšina symptómov je
spôsobená bunkovou hypersenzitivitou.
Diagnostika
F.
tularensis
je ťažké znázorniť v priamom nátere. Mikroorganizmus môže byť izolovaný zo
vzorky spúta alebo aspirátu lymfatických uzlín po inokulácii na čokoládový agar.
Hemokultiváce sú často negatívne. Mikroorganizmus rastie veľmi pomaly, a preto
je potrebné inkubovať ho viacero dní. Mikroorganizmus je možné potvrdiť
špecifickými antisérami.
Prevencia a
liečba
Liekom
voľby pre všetky formy tularémie je streptomycín. Neliečené prípady majú
úmrtnosť 5 – 15 %. Súčasťou vakcíny je živý oslabený mikroorganizmus, ale
použitie sa obmedzuje na osoby v riziku. Imunita je pravdepodobne bunková. Je
potrebné sa vyhýbať manipulácii s infikovanými zvieratami, vyhnúť sa styku
s kliešťami a používať zásobovanie bezpečnou vodou.
|
|
|
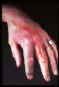 Erysipeloid – je akútna, ale pomaly sa vyvíjajúca kožná infekcia spôsobená
grampozitívnou paličkou (Erysipelothrix rhusiopathiae).
©
Mount Allison Science Image Collection
Erysipeloid – je akútna, ale pomaly sa vyvíjajúca kožná infekcia spôsobená
grampozitívnou paličkou (Erysipelothrix rhusiopathiae).
©
Mount Allison Science Image Collection |
ERYSIPELOID
Je
profesionálnym ochorením mäsiarov, spracovateľov mäsa, farmárov, pracovníkov
hydinární a spracovateľov rýb. Spracovatelia ošípaných a rýb sú obzvlášť
rizikoví. Etiologickým agensom je Erysipelothrix rhusiopathiae,
grampozitívna anaeróbna palička, ktorá infikuje človeka cez kožné abrázie
pri manipulácii s kontaminovanými produktami alebo pôdou. Obvykle spôsobuje
zápalovú léziu kože, prstov alebo ruky, ktorá je
fialovej farby
a má vyvýšené okraje. Šíri sa smerom k periférii postupne ako slabne
odfarbenie stredu. Bolestivá lézia
svrbí
a spôsobuje pálenie alebo pocit trhania. Nehnisá, a tým sa odlišuje
od stafylokokového eryzipelu. Difúzna kožná infekcia a septikémia sú vzácne.
Mikroorganizmus je možné jednoducho kultivovať na väčšine laboratórnych
médií. Je ľahko liečiteľný penicilínom.
|
|
|
 Návrat do sekcie Bakteriológia Microbiology and Immunology On-line
Návrat do sekcie Bakteriológia Microbiology and Immunology On-line
Táto strana bola naposledy zmenená
Stránku spravuje
Richard Hunt
|

 Brucella abortus
- gramnegatívny kokobacil, prokaryotická bunka; spôsobuje spontnánne aborty
hovädzieho dobytka rýchlym rastom v prítomnosti erytritolu (produkovaný
placentov). SEM x 29,650
Brucella abortus
- gramnegatívny kokobacil, prokaryotická bunka; spôsobuje spontnánne aborty
hovädzieho dobytka rýchlym rastom v prítomnosti erytritolu (produkovaný
placentov). SEM x 29,650
 Morové oblečenie. Plášť bol naplnený sladko zapáchajúcim olejom a octom, aby
zastreli zápach obetí moru. Hoci lekári v 14. storočí nepoznali príčinu,
oblečenie mohlo byť do určitej miery účinné tým, že bránilo kontaktu
s muchami.
Morové oblečenie. Plášť bol naplnený sladko zapáchajúcim olejom a octom, aby
zastreli zápach obetí moru. Hoci lekári v 14. storočí nepoznali príčinu,
oblečenie mohlo byť do určitej miery účinné tým, že bránilo kontaktu
s muchami.
 Kožný
antrax
Kožný
antrax  Mediastinálne rozšírenie a pleurálne efúzie na rtg hrudníka pri
inhalačnom antraxe.
Mediastinálne rozšírenie a pleurálne efúzie na rtg hrudníka pri
inhalačnom antraxe. Antrax, krvná zrazeniny vychádzajúca z konečníka.
Antrax, krvná zrazeniny vychádzajúca z konečníka.  Infekcia
makrofágov alebo parenchýmových buniek baktériou Listeria monocytogenes
Infekcia
makrofágov alebo parenchýmových buniek baktériou Listeria monocytogenes
 Palec s kožným vredom pri tularémii.
Palec s kožným vredom pri tularémii.
 Erysipeloid – je akútna, ale pomaly sa vyvíjajúca kožná infekcia spôsobená
grampozitívnou paličkou (Erysipelothrix rhusiopathiae).
©
Mount Allison Science Image Collection
Erysipeloid – je akútna, ale pomaly sa vyvíjajúca kožná infekcia spôsobená
grampozitívnou paličkou (Erysipelothrix rhusiopathiae).
©
Mount Allison Science Image Collection







































