|
x |
x |
|
 |
 |
|
INFECTIOUS
DISEASE |
BACTERIOLOGÍA |
INMUNOLOGÍA
|
MICOLOGÍA |
PARASITOLOGÍA |
VIROLOGÍA |
|
EN INGLÉS |
VIROLOGÍA - CAPÍTULO TRES
ESTRATEGIAS DE REPLICACIÓN DE LOS VIRUS DE ADNDr Margaret Hunt
University of South Carolina School of Medicine
Columbia
SC
USA
Traducido por :
Sarah M. Castillo -
Jorge
Medico Pasante
Clinica Corominas
Santiago
Rep. Dominicana
|
|
BUSCAR |
|
|
|
|
|
|
|
|
|
OBJETIVOS
Análisis descriptivo de las estrategias de replicación usadas por virus
de ADN animal.
Identificación de los prototipos de virus asociados a diversos esquemas
de replicación de ADN.
|
GENERAL
El genoma viral
contiene información que:
·
Asegura la
replicación de los genomas virales
·
Asegura el
ensamblaje de los genomas en viriones
·
Altera la
estructura y/o función de la célula huésped en mayor o menor medida
ESTRATEGIA VIRAL
La estrategia
viral se refiere al modo en que cada virus lleva a cabo las funciones antes
mencionadas. Dado que un virus es un parásito intracelular, tiene que
operar dentro de los límites impuestos por la célula huésped, o sortear
estas limitaciones.
ESTRATEGIA DE
REPLICACIÓN DE LOS VIRUS DE ADN
General
-
El virus
necesita hacer ARNm que pueda ser traducido en proteína por la maquinaria de
traducción de la célula huésped.
-
El virus
necesita replicar su genoma.
-
Las enzimas
de la célula huésped para la síntesis de ARNm y la replicación viral son
nucleares (exceptuando aquellas en mitocondrias) y, por tanto, si un virus va a
aprovechar estas enzimas, necesita penetrar en el núcleo.
|
| |
VIRUS DE ADN NUCLEAR
FAMILIA PARVOVIRUS
Los
parvovirus son virus muy pequeños (18 a 25 nm de diámetro), con ADN de cadena
sencilla (parvum=pequeño). Tienen una cápside icosaédrica, y no están envueltos.
La replicación de AND ocurre en el núcleo. El parvovirus humano B-19 se replica
en células en división – mayormente en progenitores de eritrocitos en la médula
ósea – y causa la quinta enfermedad (eritema infeccioso). Esta es usualmente una
enfermedad de intensidad moderada pero la disminución en la producción de
eritrocitos puede ser un problema en personas con anemia hemolítica severa
|
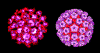 Figura 1 Virus del Papiloma virus
©
Dr. Linda Stannard, Universidad de Cape Town, Sudáfrica. Usado con
autorización.
Figura 1 Virus del Papiloma virus
©
Dr. Linda Stannard, Universidad de Cape Town, Sudáfrica. Usado con
autorización. |
FAMILIA PAPILOMAVIRUS
La familia papillomavirus
antes se agrupaba con los poliomavirus en la familia de los papovavirus (PApiloma,
POlioma, Virus del simio No. 40) porque tienen estructuras similares. Sin
embargo, hoy en día, se ha clarificado que ambos grupos tienen estrategias de
replicación muy diferentes, y por eso se han dividido en sus propios estatus de
familia.
|
PropIEDADES DE LOS POLIOMAVIRYS Y LOS PAPILOMAVIRUS |
|
Son pequeños: 40 - 60nm |
|
Son icosaédricos: proteína de cápside primaria es VP1, y en menor medida
VP2, VP3 |
|
Son virus no envueltos (desnudos) |
|
Tienen un ADN circular, de cadena doble asociados a histonas (nucleosomas) |
Los
Papillomavirus (figura 1) son difíciles de cultivar. No se ampliará este tema en
esta sección (favor referirse a la sección
virus tumorales de ADN)
|
 Figura 2 Virus SV40, un polioma virus
©
Dr. J-Y Sgro, Universidad de Wisconsin. Usado con autorización.
Figura 2 Virus SV40, un polioma virus
©
Dr. J-Y Sgro, Universidad de Wisconsin. Usado con autorización. |
POLIOMAVIRUS
Estos incluyen SV40, BK,
JC y polioma virus. Todos poseen una estrategia de replicación de AND similar.
Son pequeños (~40nm de diámetro), icosaédricos, no-envueltos que se replican en
el núcleo. Dependiendo de la célula huésped, pueden o transformar la célula (referirse
aquí) o replicar el virus y provocar lisis celular.
CICLO LÍTICO
FIJACIÓN,
PENETRACIÓN Y PÉRDIDA DE LA CÁPSULA
Las proteínas de
la cápside vírica interactúan con receptores de la superficie celular y la
penetración se hace posible vía endocitosis. Los viriones son transportados
al núcleo, y pierden su cápsula. El ADN (y las histonas asociadas) entran al
núcleo, probablemente a través de un poro nuclear.
PRODUCCIÓN DE ARNm
Y PROTEÍNAS VÍRICOS
La expresión
genética se divide en fases temprana y tardía.
Genes de fase
temprana
codifican enzimas
y proteínas reguladoras que son necesarias para en inicio del proceso de
replicación vira.
Genes de fase tardía
codifican
proteínas estructurales, proteínas necesarias para el ensamblaje del
virus maduro.
|
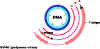 Figura
3 Expresión genética temprana
Figura
3 Expresión genética temprana
Nota: - - - - indica regiones de transcripción primaria que son
removidas en el ARNm procesado alternativamente.
Modificado de Fiers et al.,Nature 273:113

Figura 4 Genes de expresión tardía
Nota: - - - - indica regiones de transcripción primaria que son
removidas en el ARN procesado alternativamente. Las flechas anchas
indican regiones traducidas como proteínas.
Modificado de Fiers et al.,Nature 273:113
|
FASE
TEMPRANA DEL CICLO LÍTICO
Expresión
genética temprana (figura 3)
La
región
promotora temprana es reconocida por la polimerasa II del
ARN del huésped (el SV40 contiene un fuerte
inductor). Las modificaciones postranscripcionales del ARN (metilación,
poliadenilación, splicing o empalmes etc.) se llevan a cabo por
las enzimas del huésped. La transcripción temprana (transcripción
primaria) se realiza y luego tienen lugar los procesamientos
alternativos, resultando en ARNm para los
antígenos T (estas proteínas tienen amino terminales comunes
pero carboxiterminales diferentes).
Los
ARNm son traducidos en el citoplasma.
Nota:
Las transcripciones primarias que pueden ser procesadas y codificar
para más de una proteína se encuentran en diversas familias virales
y en las células huésped.
FASE TARDÍA DEL
CICLO LÍTICO
Por definición
la fase tardía inicia con el comienzo de la replicación del genoma viral.
Replicación del
ADN
La replicación del
ADN del SV40/polioma ocurre en el núcleo.
Los
Antígenos T grandes son necesarios para la replicación del ADN. Se
unen a los orígenes de replicación.
Los Polioma
virus usan la ADN polimerasa de la célula huésped, la misma reconoce los
puntos de origen de la replicación si los antígenos T están presentes.
La replicación
de ADN es bidireccional (hay dos horquillas de replicación por cada
genoma circular de AND y el proceso de replicación conlleva cadenas
líder/retardada, fragmentos de
Okazaki,
ADN ligasa, etc.). Este proceso de replicación de ADN es muy similar
a aquél que ocurre en la célula huésped – lo cual no es sorprendente ya
que el virus usa la maquinaria del huésped exceptuando la implicación de
los antígenos T.
Las histonas
forman complejos con el ADN recién formado.
Expresión genética
de fase tardía
(figura 4)
Los ARNm
tardíos son hechos luego de la replicación del ADN (en esta etapa hay
mucho ADN viral recién sintetizado y disponible como molde o plantilla.
Aún se transcribe ARNm de fase temprana pero a una velocidad mucho menor.
El antígeno T
está involucrado en la regulación de la transcripción aumentada por
promotores tardíos y de la transcripción demorada por promotores de fase
temprana. También interactúa con proteínas de la célula huésped
cambiando las propiedades de la misma, jugando así un papel en la
transformación celular y en la formación tumoral.
VP1, 2, y 3
resultan de la misma transcripción primaria, la cual ha es sometida a
empalmes diferenciales (figura 5). El resultado de esto es que el marco
de lectura para VP1 es diferente a aquel para VP2 y VP3. Por tanto, una
región de ADN puede codificar dos o más secuencias de aminoácidos de
acuerdo al marco de lectura que se utilice. Esta es otra manera en que
los virus (y células) pueden utilizar una corta sección de ADN para
codificar más de una secuencia proteínica.
ENSAMBLAJE
Los ARNm de VP1, 2
y 3 son traducidos en el citoplasma, las proteínas son transportadas al
núcleo, y las
cápsides se ensamblan con el ADN (y las histonas celulares) dentro. Un
gran número de cápsides de acumula en el núcleo formando cuerpos de
inclusión. Los viriones son liberados mediante lisis celular.
|
 Figura 5 VP1, 2, y 3 vienen de la misma transcripción primaria la cual es
sometida a empalmes (splicing) diferenciales. Esto hace que el marco de
lectura para VP1 sea diferente del de VP2 y VP3
Figura 5 VP1, 2, y 3 vienen de la misma transcripción primaria la cual es
sometida a empalmes (splicing) diferenciales. Esto hace que el marco de
lectura para VP1 sea diferente del de VP2 y VP3 |
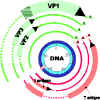 Figura 6
Figura 6
Expresión genética del SV40.
Los genes de fase temprana se ven en rojo, los de fase tardía en verde. Nota:
- - - - indica regiones de transcripción primaria que son removidas
en el ARNm procesado alternativamente. El área marcada con rayitas cruzadas
indica regiones del ARN traducidas en diferentes marcos de lectura de
acuerdo a empalmes alternativas transcritos
Modificado de Fiers et al.,Nature 273:113 |
|
CARACTERÍSTICAS A TOMAR EN CUENTA REFERENTES A LA ESTRATEGIA DEL
POLIOMAVIRUS |
|
Funciones tempranas y tardías |
|
Usos múltiples para la misa secuencia de ADN
(empalmes alternativas; marcos de lectura solapados) |
|
Proteína multifuncional (antígeno T) |
|
Genoma pequeño – no ha de sorprender que el virus codifique un muy
limitado número de proteínas |
|
La célula huésped provee la maquinaria para la síntesis de ARN y su
modificación, también para la síntesis de ADN, y las histonas para
el empacamiento del ADN |
|
 Figura 7a Estructura del Adenovirus
©
Dr. Linda Stannard, Universidad de Cape Town, Sudáfrica. Usado con
autorización
Figura 7a Estructura del Adenovirus
©
Dr. Linda Stannard, Universidad de Cape Town, Sudáfrica. Usado con
autorización
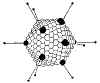 Figura 7b Estructura de un Adenovirus
Figura 7b Estructura de un Adenovirus |
ADENOVIRUS
|
PROPIEDADES DE LOS ADENOVIRUS |
|
Son más grandes que los papovavirus (70nm de diámetro) |
|
No envueltos (desnudos), icosaédricos con fibras en los vértices (figuras
7 y 8) |
Su genoma es 7 veces el tamaño del genoma de los poliomavirus
|
|
Su ADN es linear, de cadena doble, asociado a proteínas básicas
codificadas por al mismo virus (a diferencia de los virus polioma y
papiloma, los adenovirus no utilizan histonas de la célula huésped para
empacar el ADN del virión) |
|
|
CICLO LÍTICO
ADSORSIÓN Y
PENETRACIÓN
Los adenovirus
usualmente infectan células epiteliales. Las fibras se unen con receptores en la
superficie celular y el virus es engullido por endocitosis. El virus aparenta
ser capaz de lisar endosomas. La pérdida de la cápside se da en varios pasos. El
ADN es liberado dentro del núcleo (probablemente por un poro nuclear) (figura
9).
FASE TEMPRANA
Transcripción temprana:
Los adenovirus usan la polimerasa de ARN de la célula huésped y los ARNm de fase
temprana son transcritos de regiones dispersas de ambas hebras del ADN (figura
10). El hecho de que haya promotores múltiples resulta en un control más
flexible. Los ARNm son procesados por la célula huésped para mutilación,
poliadenilación y (a veces) sistemas de enzimas de empalmes, luego son
exportados al citoplasma y traducidos.
|
| |
Las proteínas de
fase temprana incluyen aquellas que:
-
Son necesarias
para la transcripción (la proteína E1A es necesaria para la
transcripción de otros genes de fase temprana; y por eso esos otros
genes a veces son llamados “tempranos retardados” y la E1A es llamada un
gen “temprano inmediato”).
-
Son necesarias
para la síntesis del ADN del adenovirus (incluye la ADN-polimerasa)
-
Alteran la expresión de los genes de la célula huésped. Esto incluye a
los genes cuyos productos interfieren con la respuesta anti-viral del
huésped y/o interfieren con la regulación del ciclo celular
|
| |
A

B
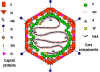 Figura 8
Figura 8
Modelos del virión de adenovirus. A: Una imagen tridimensional de una
partícula intacta de adenovirus vista junto a un eje
icosaédrico de tres dobleces (© EMBL Virus Structure Resource). B:
Una sección estilizada de una partícula de adenovirus en base a los
conocimientos actuales de su ADN y sus componentes polipeptídicos. Ninguna
sección real del virión icosaédrico contendría todos los componentes Los
constituyentes del virión son designados por el número de polipéptidos con
excepción de la proteína terminal (PT). Adaptado de Fields et al.,
Fundamental Virology (1996).
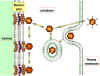 Figura
9 Figura
9
Representación diagramática del engullimiento y pérdida de la cápside de los
adenovirus.
Adaptado de Zinsser Microbiology 20ava Ed.
 Figura 10
Figura 10
Mapa de transcripción del adenovirus. Los genes de fase temprana se señalan
en rojo. En negro se indican los genes de fase tardía. Las líneas azules
indican ADN. Los corchetes indican la posición de los promotores. Las
transcripciones primarias se realizan a partir de cada promotor y luego
pasan por empalmes alternativas, el diagrama arriba no muestra las
transcripciones primarias. Únicamente enseña aquellas regiones presentes en
los productos empalmados alternativamente. Las regiones faltantes indican la
remoción de los intrones. Adaptado
de Broker, T.R. In Processing of RNA. (Apirion, D ed) 181-212, 1984
|
 Figura 11
Mecanismo de dislocación para la replicación del ADN del adenovirus
Figura 11
Mecanismo de dislocación para la replicación del ADN del adenovirus |
FASE TARDÍA
Replicación del ADN:
Los adenovirus
codifican su propia ADN-polimerasa (que es una de las proteínas de fase
temprana). El ADN se replica por un mecanismo de dislocación de las hebras (figura
11). No hay
Fragmentos de Okazaki, ambas hebras se sintetizan en modo continuo.
La ADN –
polimerasa no puede iniciar la síntesis de novo, necesitan un primer
o imprimador o proteína iniciadora. En el caso de los adenovirus, la
proteína Terminal (TP), la cual es codificada por el virus mismo, actúa como
imprimador. Se encuentra, por tanto, unida covalentemente al terminal 5’ de
todas las hebras de ADN de los adenovirus.
|
 Figura 12
Figura 12
Mapa de transcripción del adenovirus. Los genes de fase temprana se muestran
en rojo. El verde señala los genes de fase tardía. El azul indica ADN. Los
corchetes indican los promotores. Las regiones faltantes indican la remoción
de los intrones.
Adaptado
de Broker, T.R. In Processing of RNA. (Apirion, D ed) 181-212, 1984
 Figura
13
Procesamiento de la transcripción viral primaria. Figura
13
Procesamiento de la transcripción viral primaria. |
Transcripción tardía:
La manera en que
la transcripción tardía se inicia todavía no se conoce bien. Los ARNm
tardíos codifican predominantemente para proteínas estructurales y existe UN
promotor tardío principal (figura 12). La transcripción primaria es
procesada para generar varios ARNm
monocistrónicos (figuras 12 y 13):
Hay dos tipos de
división en la transcripción primaria:
i. para
generar diversos terminales 3’ que posteriormente son poliadenilados
ii. para
remoción de los
intrones
Todavía se
desconoce cómo se controla este proceso para que la cantidad correcta de
cada ARNm sea creada. Parece que el virus hace más ARNm y proteínas que las
necesarias para el ensamblaje del virión, por tanto un control preciso puede
no ser necesario.
|
| |
ENSAMBLAJE
El ensamblaje de
las partículas de adenovirus tiene lugar en el núcleo. El ADN entra a las
partículas luego de que una cápside inmadura es formada. Las cápsides
posteriormente sufren un proceso de maduración, a partir del cual las
células son lisadas y los viriones escapan hacia fuera.
Se hacen más
proteínas estructurales de las necesarias y el exceso se acumula en el
núcleo formando cuerpos de inclusión.
|
| |
|
CARACTERÍSTICAS A TOMAR EN CUENTA REFERENTES A LA ESTRATEGIA DEL
ADENOVIRUS |
|
Los adenovirus son más grandes y complejos que los papovavirus. |
|
Los adenovirus codifican su propia ADN-polimerasa y sus proteínas de
empaque del ADN. |
|
Sin embargo, aunque algunos adenovirus codifican su propia
ADN-polimerasa, utilizan también factores del huésped para la
replicación del AND, y usan ARN-polimerasa del huésped y también los
sistemas de modificación del ARN, por ellos la síntesis de ácido
nucleido necesita llevarse a cabo en el núcleo. |
|
|
 Figura 14a
Estructura del Herpes virus
Figura 14a
Estructura del Herpes virus
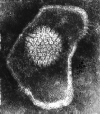 Figura 14b
Virus Herpes simplex
©
Dr. Linda M Stannard, Universidad de Cape Town, Sudáfrica, 1995 (usado con
autorización).
Figura 14b
Virus Herpes simplex
©
Dr. Linda M Stannard, Universidad de Cape Town, Sudáfrica, 1995 (usado con
autorización).
|
HERPESVIRUS
|
PROPIEDADES DE LOS HERPESVIRUS |
|
Son viriones grandes (180 - 200nm), más que los adenovirus |
|
Tienen genomas más grandes (3 a 5 veces) más que los adenovirus |
|
ADN linear, de cadena doble |
|
Son virus icosaédricos (esto significa que los solventes lipídicos
inactivan estos virus) (figura 14) |
|
 Figura 15a Virus Herpes simplex fijándose a la membrana plasmática
©
Dennis Kunkel Microscopy, Inc.
Usado con autorización
Figura 15a Virus Herpes simplex fijándose a la membrana plasmática
©
Dennis Kunkel Microscopy, Inc.
Usado con autorización
 Figura 15b Fusión de un virus asociado-a-membrana con la membrana
plasmática
Figura 15b Fusión de un virus asociado-a-membrana con la membrana
plasmática |
FIJACIÓN Y PENETRACIÓN
Muchos herpesvirus,
incluyendo el virus herpes simples, pueden fundirse directamente con la
membrana celular plasmática (resultado en pérdida parcial de su envoltura) (figura
15). Dicha fusión con la membrana plasmática tiene implicaciones tanto para
el virus como para la célula huésped. Dentro de dichas implicaciones tenemos:
i) Como la
proteína de fusión está activa a un pH fisiológico, si se inserta en la
membrana celular plasmática durante el ciclo de crecimiento viral, la
célula infectada puede potencialmente fundirse con otras células y
formar
sincitios.
ii) La
envoltura viral deja “huellas” en la membrana celular plasmática y estas
son señales de infección en la célula (figura 15b)
Las cápside son
transportadas hacia el núcleo y el ADN pasa al mismo (probablemente a través
de poros nucleares).
|
 Figura
16 Expresión de los genes temprano – inmediatos, tempranos y tardíos de los
herpesvirus Figura
16 Expresión de los genes temprano – inmediatos, tempranos y tardíos de los
herpesvirus |
FASE TEMPRANA
Transcripción temprana (los
ARNm hechos durante esta fase son los ARN alfa y beta) (figura 16)
Los herpesvirus
usan ARN – polimerasa del huésped. Sin embargo, una proteína del tegumento
del virión (VP16) entra en el núcleo durante la infección como parte del
complejo de factores de transcripción reconocidos por la ARN – polimerasa
del huésped. El virus usa enzimas del huésped para la modificación del ARNm.
Inicialmente, los
ARNm – alfa son transcritos. Estos son los ARNm inmediatos tempranos y son
exportados al citoplasma y traducidos en proteínas alfa. Las α-proteínas
traducidas en el citoplasma son transportadas al núcleo en donde activan
promotores beta que serán utilizados por la ARN polimerasa del huésped (figura
16).
Los ARN-betas son
transcritos por la ARN – polimerasa del huésped. (Los genes-beta comoquiera
son “de fase temprana” puesto que son transcritos previo a la síntesis de
ADN. Algunas veces, por ello, los genes – alfa son llamados “tempranos
inmediatos” y los beta “tempranos”). Las proteínas beta participan en la
regulación de la expresión genética. Disminuyen la expresión de los genes
alfa y son necesarias para la expresión de los genes gamma. También
participan en varios aspectos de la síntesis de ADN; por ejemplo, los genes
– beta herpéticos codifican varias proteínas entre las cuales tenemos:
PUESTO QUE ESTAS
PROTEÍNAS BETA SON CODIFICADAS POR EL VIRUS Y NO POR LA CÉLULA HUÉSPED, SON
ESLABONES POTENCIALMENTE DÉBILES EN EL CICLO DE VIDA VIRAL Y POR TANTO, SON
OBJETIVOS PARA QUIMIOTERAPIA VIRAL
|
|
 Figura 18 Posibles estructuras genómicas de los herpesvirus
Figura 18 Posibles estructuras genómicas de los herpesvirus |
FASE TARDÍA
Replicación de ADN
Los
herpesvirus codifican varias proteínas, además de la ADN polimerasa, que son
necesarias para la replicación del ADN. Se desconoce el mecanismo preciso de la
replicación del ADN. La replicación del ADN se acompaña de mucha recombinación.
El ADN replicado se encuentra como moléculas concatámeros (repeticiones en
tándem del genoma unidas cabeza – con – cola). Estas son separadas para que
tengan medidas de genoma cuando el ADN es empacado dentro del virión (figura
18).
Algunos herpesvirus (i.e. el virus herpes simples) tienen una estructura
genómica en la que dos partes del genoma pueden ser inversas con relación la una
con la otra (figura 18), otras no. El significado de esto se desconoce.
Transcripción tardía:
Por definición, la
transcripción tardía ocurre después de la replicación del ADN. Los ARNm
gamma se hacen y se traducen en el citoplasma. Las proteínas gamma son
predominantemente estructurales. Hay una disminución de la expresión de los
genes beta en la etapa tardía. Esto es probablemente debido a una regulación
a la baja de la transcripción de los genes beta por una de las proteínas
gamma.
En los herpesvirus
no hay una organización aparente en bloques del genoma durante las
transcripciones temprana y tardía.
|
 Figura 19A
Figura 19A
Virus
del herpes simples en vacuolas celulares y citoplasma de un linfocito de
sangre periférica ©
Dennis Kunkel Microscopy, Inc.
Usado con autorización
 Figura
19B
Figura
19B
Virus
herpes simplex en un linfocito de sangre periférica ©
Dennis Kunkel Microscopy, Inc.
Usado con autorización
|
ENSAMBLAJE
El ensamblaje ocurre
en el núcleo. La cápside se forma y el ADN entra en ella. Las cápsides adquieren
una envoltura mediante yemación a través de la membrana nuclear interna, la cual
posee insertadas en ella proteínas de membrana virales (figura 19). También hay
proteínas de tegumento asociadas con la cara interna de la membrana nuclear
interna. La envoltura vírica entonces se funde con la membrana nuclear externa y
la nucleocápside desenvuelta es llevada al citoplasma, en donde adquiere un
tegumento más maduro. Luego se hace envuelta de nuevo al yemar como vesículas de
Golgi, y es posteriormente liberado.
La proteína de fase
tardía requerida para la transcripción inmediata de ARNm de fase temprana en la
próxima vuelta de infección es empacada en el virión.
Proteínas
estructurales excedentes se acumulan en el núcleo, muchas veces forman cuerpos
de inclusión (parte del efecto citopático).
|
CARACTERÍSTICAS A NOTAR SOBRE LOS HERPESVIRUS |
| No hay bloqueo evidente
de los genes de fase temprana ni tardía |
| Son más independientes
que algunos de los virus más pequeños |
| Como son más
independientes, son “eslabones más débiles” para ser atacados por drogas |
|
Figura 19C (derecha)
Etapas de la exocitosis hacia la membrana plasmática y desde el núcleo del
herpesvirus, en el núcleo se ensambla el núcleo vírico |
 |
 |
 |
 |
|
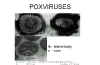 Figura 20 Tinción negativa de poxvirus
© F. Fenner
Figura 20 Tinción negativa de poxvirus
© F. Fenner |
VIRUS CITOPLÁSMICOS DE ADN
POXVIRUS
|
 Figura 21 Niño con varicela
CDC/Cheryl Tryon ctt1@cdc.gov
Figura 21 Niño con varicela
CDC/Cheryl Tryon ctt1@cdc.gov |
Hay muchas razones por
las que los poxvirus (figura 20) son de importancia:
- Algunos poxvirus
son una nota histórica, como el virus de la viruela (figura 21) y el virus
vaccinia (viruela bovina, la cual fue utilizada en la vacuna de la viruela)
(referirse
aquí))
- Los poxvirus
pueden ser posibles agentes de bioterrorismo
- Los poxvirus son
usados en nuevas técnicas de vacunación (tales como la vaccinia
genéticamente manipulada)
-
Algunos miembros de esta familia infectan humanos (molluscum contagium (figura
22), orf virus de los pequeños rumiantes, pox de los simios, pox bovino).
|
 Figura 22 Micrografía de transmisión de electrones del
poxvirus molluscum contagiosum
CDC
Figura 22 Micrografía de transmisión de electrones del
poxvirus molluscum contagiosum
CDC |
|
PROPIEDADES DE LOS POXVIRUS |
|
Viriones grandes |
|
Genomas largos, ADN de doble cadena variado en tamaño pero tanto o más
grandes que los herpesvirus |
|
Morfología compleja |
|
Envueltos |
|
| |
Los poxvirus se replican
en el citoplasma. Esto significa que ellos deben aportar su propio ARNm y su
propia maquinaria de síntesis de ADN.
El virus vaccinia es, de
los miembros de la familia poxvirus, el más estudiado.
FIJACIÓN Y
PENETRACIÓN
El virus se fija a
receptores de la superficie celular. Entra a la célula mediante endocitosis
o por fusión directa del mismo con la membrana plasmática. Posteriormente el
virus es liberado al citoplasma sin su envoltura.
FASE TEMPRANA
Transcripción temprana
Luego de la etapa
inicial de pérdida de la envoltura, el virus puede crear un limitado número
de ARNm (los ARNm tempranos inmediatos). Para lograr esto, el poxvirus
necesita una ARN – polimerasa dependiente de ADN. La ARN polimerasa del
huésped se encuentra en el núcleo de la célula y esto explica porqué los
poxvirus codifican su propia ARN – polimerasa dependiente de ADN para hacer
su propio ARN. Como esta enzima es necesaria inmediatamente luego de la
infección, debe de ser traída a la célula infectada junto al ADN viral, está
por tanto presente en el virión. El ADN viral “desnudo” que ha sido
desprovisto de toda proteína es por tanto no infeccioso, ya que no tendrá
ARN – polimerasa asociada a él, y el ciclo de vida del virus no podrá
llevarse a cabo sin la presencia de ARN ni de proteínas.
Los poxvirus son
metilados y poliadenilados al igual que los ARNm eucarióticos, pero los ARNm
celulares son modificados en el núcleo y los del virus en el citoplasma.
Como el poxvirus es citoplásmico, estas modificaciones deben de llevarse a
cabo por enzimas codificadas por el virus mismo. Las enzimas modificadoras
son empacadas dentro del virión y por ello, aquellos ARNm creados
inmediatamente luego de la infección pueden ser modificados. Hasta ahora, no
ha sido reportado ningún ARN empalmado de los virus vaccinia (esto no ha de
sorprender puesto que se replica en el citoplasma y las enzimas empalmadotas
del huésped se hallan dentro del núcleo).
Uno de los
productos de los ARNm tempranos inmediatos es la enzima que ayuda a quitar
la envoltura del virus. Esto permite mayor pérdida de las membranas del ADN
de la vaccinia y así más genes pueden ser transcritos – los genes de fase
temprana ahora se expresan todos. Los poxvirus son excepcionales en que
codifican una proteína para desenvolver la cual debe de ser creada en la
célula recién infectada antes de que la pérdida de su envoltura sea completa.
En el citoplasma
se pueden apreciar “factorías” de producción viral – sitios de replicación
del virus vaccinia.
Las proteínas de
fase temprana son parte de la replicación del ADN, transcripción del ARN,
modificación del ARN y pérdida de su envoltura. También algunas son
estructurales.
|
| |
FASE TARDÍA
Síntesis de ADN
La síntesis del
ADN ocurre en “factorías” y utilizan un mecanismo inusual que no va a ser
discutido en este texto.
Transcripción tardía y
traducción
Este es un proceso
complejo. Algunas proteínas de fase tardía son creadas durante dicha fase,
pero otras se crean únicamente al principio de la misma. Algunas proteínas
de fase temprana no se sintetizan una vez que ha comenzado la replicación
del ADN, mientras que algunas otras proteínas de fase temprana se sintetizan
tanto durante la fase temprana como durante la tardía. Por tanto, hay un
control complicado sobre cuales proteínas son hechas por el virus vaccinia y
en qué momento. Esto significa que hay controles diferentes a los de fase
temprana y a los de fase tardía. (Este es un virus muy grande, por eso su
complejidad no es rara).
|
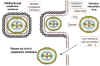 Figura 23
Posibles esquemas de formación de los viriones pox infecciosos. El núcleo vírico
se envuelve en la membrana citoplásmica y es liberado cuando la célula huésped
es lisada. Otros viriones asociados-a-membrana pueden yemar a través de otras
membranas, en cuyo caso tendrían dos envolturas. En cualquier caso, el virión es
infeccioso.
Adaptado de Baron, S. Ed. Medical Microbiology 4a Edición. 1996.
Figura 23
Posibles esquemas de formación de los viriones pox infecciosos. El núcleo vírico
se envuelve en la membrana citoplásmica y es liberado cuando la célula huésped
es lisada. Otros viriones asociados-a-membrana pueden yemar a través de otras
membranas, en cuyo caso tendrían dos envolturas. En cualquier caso, el virión es
infeccioso.
Adaptado de Baron, S. Ed. Medical Microbiology 4a Edición. 1996. |
ENSAMBLAJE
El ensamblaje
ocurre en las “factorías” en el citoplasma. Las nuevas partículas
víricas inmaduras adquieren una membrana mientas están en el
citoplasma – este mecanismo no está completamente esclarecido pero
al parecer el virus es “envuelto” por membranas celulares (figura
23). Las ideas anteriores de que esta envoltura se forma
directamente a partir de lípidos son incorrectas. Hay una maduración
gradual de las partículas envueltas. El virus generalmente es
liberado con la desintegración de la célula huésped, pero algunos
pueden liberarse yemando a través de la membrana (en estos casos
tienen una envoltura extra). Ambas formas son infecciosas. La manera
en la que el virus es liberado puede depender del tipo de célula
huésped.
|
CARACTERÍSTICAS A TOMAR
EN CUENTA SOBRE LOS POXVIRUS |
| Citoplásmicos |
| Genoma largo |
| El virus hace muchas
cosas por su propia cuenta |
| El virus tiene
habilidades inusuales comparado a otros virus |
|
|
|
 Regreso a la sección de
Virologia
Microbiología e Inmunología on line
Regreso a la sección de
Virologia
Microbiología e Inmunología on line
Esta página se modificó
recientemente en
Saturday, February 07, 2015
Mantenimiento de la pagina por
Richard Hunt
|

 Figura 1 Virus del Papiloma virus
©
Dr. Linda Stannard, Universidad de Cape Town, Sudáfrica. Usado con
autorización.
Figura 1 Virus del Papiloma virus
©
Dr. Linda Stannard, Universidad de Cape Town, Sudáfrica. Usado con
autorización.  Figura 2 Virus SV40, un polioma virus
©
Dr. J-Y Sgro, Universidad de Wisconsin. Usado con autorización.
Figura 2 Virus SV40, un polioma virus
©
Dr. J-Y Sgro, Universidad de Wisconsin. Usado con autorización.  Figura 5 VP1, 2, y 3 vienen de la misma transcripción primaria la cual es
sometida a empalmes (splicing) diferenciales. Esto hace que el marco de
lectura para VP1 sea diferente del de VP2 y VP3
Figura 5 VP1, 2, y 3 vienen de la misma transcripción primaria la cual es
sometida a empalmes (splicing) diferenciales. Esto hace que el marco de
lectura para VP1 sea diferente del de VP2 y VP3  Figura 6
Figura 6 Figura 7a Estructura del Adenovirus
©
Dr. Linda Stannard, Universidad de Cape Town, Sudáfrica. Usado con
autorización
Figura 7a Estructura del Adenovirus
©
Dr. Linda Stannard, Universidad de Cape Town, Sudáfrica. Usado con
autorización
 Figura 8
Figura 8
 Figura 11
Mecanismo de dislocación para la replicación del ADN del adenovirus
Figura 11
Mecanismo de dislocación para la replicación del ADN del adenovirus Figura 12
Figura 12 Figura 15a Virus Herpes simplex fijándose a la membrana plasmática
©
Dennis Kunkel Microscopy, Inc.
Usado con autorización
Figura 15a Virus Herpes simplex fijándose a la membrana plasmática
©
Dennis Kunkel Microscopy, Inc.
Usado con autorización
 Figura
16 Expresión de los genes temprano – inmediatos, tempranos y tardíos de los
herpesvirus
Figura
16 Expresión de los genes temprano – inmediatos, tempranos y tardíos de los
herpesvirus Figura 19A
Figura 19A 



 Figura 20 Tinción negativa de poxvirus
© F. Fenner
Figura 20 Tinción negativa de poxvirus
© F. Fenner Figura 21 Niño con varicela
CDC/Cheryl Tryon ctt1@cdc.gov
Figura 21 Niño con varicela
CDC/Cheryl Tryon ctt1@cdc.gov Figura 22 Micrografía de transmisión de electrones del
poxvirus molluscum contagiosum
CDC
Figura 22 Micrografía de transmisión de electrones del
poxvirus molluscum contagiosum
CDC  Figura 23
Posibles esquemas de formación de los viriones pox infecciosos. El núcleo vírico
se envuelve en la membrana citoplásmica y es liberado cuando la célula huésped
es lisada. Otros viriones asociados-a-membrana pueden yemar a través de otras
membranas, en cuyo caso tendrían dos envolturas. En cualquier caso, el virión es
infeccioso.
Adaptado de Baron, S. Ed. Medical Microbiology 4a Edición. 1996.
Figura 23
Posibles esquemas de formación de los viriones pox infecciosos. El núcleo vírico
se envuelve en la membrana citoplásmica y es liberado cuando la célula huésped
es lisada. Otros viriones asociados-a-membrana pueden yemar a través de otras
membranas, en cuyo caso tendrían dos envolturas. En cualquier caso, el virión es
infeccioso.
Adaptado de Baron, S. Ed. Medical Microbiology 4a Edición. 1996. 







