|
|
 |
||||
|
Dr Alvin Fox |
BACTERIOLOGÍA | INMUNOLOGÍA | MICOLOGÍA | PARASITOLOGÍA | VIROLOGÍA |
|
|||||
|
|
|||||
|
E-MAIL |
|||||
|
|
ESTERILIZATION El término esterilización se refiere a la muerte (o eliminación) de TODAS las bacterias de manera no selectiva. Por ejemplo, esterilizar en autoclave involucra el calentamiento de líquidos (por ejemplo medios de cultivo) o sólidos a 121oC bajo presión de vapor. Los materiales en este caso obviamente deben ser resistentes al calor. El óxido de etileno se usa con frecuencia en los hospitales para esterilizar equipo que no puede ser calentado. Los filtros de membrana poseen poros que atrapan a las bacterias, no obstante permiten que algunos fármacos y sustancias químicas pequeñas los atraviesen, así que es posible utilizar filtros pre-esterilizados para la esterilización de soluciones delicadas. La luz ultravioleta se usa para disminuir los niveles bacterianos en las superficies como en las salas de operaciones, sin embargo, no es completamente efectiva. La radiación ionizante es más eficiente y puede ser utilizada para esterilizar instrumental y alimentos. Los desinfectantes (por ejemplo los basados en fenol) pueden ser útiles para eliminar bacterias en algunos instrumentos, pero no pueden ser utilizadas para consumo de ingesta o sobre la piel. Los antisépticos (por ejemplo el yodo o el alcohol al 70%) se usan vía tópica (por ejemplo en la superficie de la piel) para reducir la carga bacteriana.
ANTIBIOTICOS En contraste, los antibióticos son agentes que son “selectivamente” tóxicos para las bacterias (ya sea porque las matan [bactericida] o porque inhiben su crecimiento [bacteriostático] sin dañar al paciente. De esta forma pueden ser ingeridos. Estos compuestos por definición, deben actuar sobre estructuras que se encuentran en las bacterias, pero no en el huésped. Los antibióticos trabajan mas eficientemente en colaboración con el sistema inmune activo, para matar las bacterias infecciosas eliminándolas del huésped. Después del aislamiento de colonias puras (ver la Conferencia 2 de Bacteriología, Bacteriology lecture 2), la susceptibilidad de los aislamientos bacterianos se puede ensayar en una amplia variedad de antibióticos. La concentración inhibitoria mínima (MIC) se refiere a la concentración más baja de antibiótico que detiene visiblemente el crecimiento bacteriano. La forma más simple, la zona de inhibición del crecimiento bacteriano alrededor de un disco impregnada con el antibiótico (método de Kirby-Bauer) es otra medida de la actividad del antibiótico.
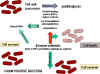
INHIBIDORES DE LA SINTESIS DE PARED CELULAR Una clase principal de antibióticos, es aquella de los que inhiben la síntesis de peptidoglicanos (Figura 1). Una vez que se inhibe la síntesis de la pared celular (lo que involucra proteínas de unión a penicilina, PBPs), puede ocurrir autolisis enzimática de la pared celular. Sin la influencia restrictiva de la pared celular, la elevada presión osmótica dentro de la célula hace estallar a la membrana interna y/o externa de la bacteria. Por lo tanto estos antibióticos son generalmente bactericidas. Varios mecanismos están involucrados en la inhibición de la síntesis de peptidoglicanos:
|
||||
|
|
|||||
|
PALABRAS CLAVE |
|||||
|
TUTORIAL |
|||||
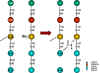 Figura 1 Unión cruzada de peptidoglicanos.
Figura 1 Unión cruzada de peptidoglicanos.
|
|
||||
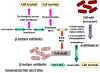 Figura 3 Resistancia a beta-lactamasas – Bacterias Gram negativas
Figura 3 Resistancia a beta-lactamasas – Bacterias Gram negativas
|
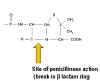
PENICILINA La penicilina la sintetiza el hongo Penicillium chrysogenum. Durante la fermentación el hongo forma el ácido-6-aminopenicilánico el cual consta de la fusión de un anillo tiazólico y un anillo beta lactámico (Figura 2). Sin embargo, este anillo es lábil a pH ácido y está sujeto a la degradación por enzimas bacterianas. Sus derivados más estables se elaboran bioquímicamente de manera que adicionalmente incrementen su estabilidad, se absorban mejor por el tracto gastrointestinal y tengan un más amplio espectro de efectos bactericidas. Varias cadenas laterales procedentes de síntesis química, se han unido a las estructuras de anillos lactámicos de forma sintética, produciendo un número de antibióticos con diferentes propiedades en el huésped. Muchas penicilinas (Figura 2) muestran poca actividad contra las bacterias Gram negativas, debido a que no penetran la membrana externa. Las cefalosporinas y otras penicilinas mas recientes son activas contra las bacterias gram negativas ya que pueden penetrar la membrana externa. Otras penicilinas químicamente modificadas presentan una menor tasa de eliminación por parte del paciente, disminuyendo así la frecuencia de administración de estos fármacos. Las penicilinas pueden ser destruídas por las beta-lactamasas (o penicilinasas) que producen las cepas bacterianas resistentes (Figura 3). El ácido clavulínico también posee un componente beta lactámico, mediante el cual se une fuertemente a las beta-lactamasas, impidiendo su disociación como sustrato e inhibiendo por lo tanto la actividad de las beta-lactamasas. Este compuesto se utiliza en combinación con otras penicilinas, permitiendo su uso contra bacterias que de otra manera presentarían resistencia. Otra forma de resistencia involucra un cambio en la estructura de las proteínas de unión a penicilina (PBPs, penicillin binding proteins), de tal manera que el antibiótico no se una eficientemente con ellas (Figura 4). En el caso de las bacterias gram negativas, las penicilinas atraviesan la membrana externa por medio de porinas. Los mecanismos de resistencia se pueden desarrollar a través de mutación, dando lugar a la aparición de porinas modificadas.
|
||||
 Figura 5 Estructura de polimixina
Figura 5 Estructura de polimixina |
POLYMYXIN B La polimixina B (Figura 5) se une a la porción Lípido A del lipopolisacárido y también se une a fosfolípidos. Sin embargo, se une preferencialmente al Lípido A. Esto desestabiliza la membrana externa de las bacterias gram negativas. Debido a que la membrana celular no se encuentra expuesta en las bacterias gram positivas, la polimixina tiene poca efectividad contra ellas. Esta droga es tóxica a las células humanas, debido a que también puede lisar a las membranas eucarióticas, esto explica que su uso clínico sea limitado.
|
||||
|
|
|
||||