|
x |
x |
|
 |
 |
|
INFECTIOUS
DISEASE |
BAKTERIYOLOJİ |
İMMÜNOLOJİ |
MYCOLOGY |
PARASITOLOGY |
VIROLOGY |
|
|
İMMÜNOLOJİ – BÖLÜM ONBEŞ
MHC: GENETİĞİ VE
TRANSPLANTASYONDAKİ ROLÜ
Abdul Ghaffar, Ph.D.
Emertius Professor of Pathology, Microbiology and Immunology
University of South Carolina
Çeviri:
Doç. Dr. Erkan Yula
İzmir, Katip Çelebi Üniversitesi, Tıp Fakültesi, Tıbbi Mikrobiyoloji
Anabilim Dalı
|
|
ENGLISH |
|
FRANCAIS |
|
SHQIP |
|
PORTUGUES |
|
Let us know what you think
FEEDBACK |
|
SEARCH |
|
|
|

 |
|
Logo image © Jeffrey
Nelson, Rush University, Chicago, Illinois and
The MicrobeLibrary |
|
|
|
|
|
ÖĞRENME HEDEFLERİ
MHC lokuslarını ve ürünlerini öğrenilmesi
MHC heterojenitesini ve genetik temellerini anlaşılması
Farklı hücrelerdeki MHC moleküllerinin dağılımını
MHC antijenlerinin saptanmasını( doku tiplendirmesi) öğrenilmesi
MHC’nin transplantasyondaki, immün fonksiyonlardaki ve hastalıklardaki
rolünün anlaşılması
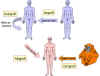 Şekil 1
Şekil 1
Greft çeşitleri |
TANIMLAR
-
Doku uyum (transplantasyon) antijenleri
Genetik olarak farklı iki birey arasında nakil yapıldığında ret
olup olmayacağını belirleyen doku ve hücreler üzerindeki
antijenler
-
Majör doku uyum (MHC) antijenleri
Çok güçlü immün yanıta yol açan ve doku reddinde en önemli
olanlar Doku-uyumluluk antijenleridir.
-
MHC kompleksi
MHC antijenlerini kodlayan tek bir kromozom üzerindeki gen grubu
-
HLA (insan lökosit antijenleri)
insan MHC antijenleri (ilk olarak lökosit üzerinde tespit
edilmişlerdir)
-
H-2 antijenleri
Fare MHC antijenleri
Greft tipleri (Şekil 1)
-
Ksenogreft
Farklı türlerin üyeleri arasında nakil (ayrıca heterolog,
ksenojenik ya da heterogreft olarak da bilinir)
-
Allogreft
Aynı türün iki üyesi arasında nakil (ayrıca allojenik ya da
homogreft olarak da bilinir)
-
İzogreft
Aynı türün özdeş genetik yapıdaki üyeleri arasında nakil (tek
yumurta ikizleri veya aynı soydan çiftleştirilmiş hayvanlar
(inbred) arası)
Haplotip
Tek bir kromozom üzerindeki bir grup gen
|
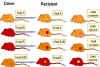 Şekil 2
Şekil 2
Transplantasyon kuralları |
TRANSPLANTASYON
İLKELERİ (Şekil 2)
İmmünkompetan konak nakledilen dokulardaki (ya da
hücrelerdeki ) yabancı antijenleri tanır ve ret ile sonuçlanan bir immun
yanıt başlatır. Diğer yandan, immun yetmezliği olan konağa yabancı
immunkompetan lenfoid hücreler nakil edildiğinde greftteki immünoreaktif
T hücreleri konak dokuyu yabancı antijen olarak tanır doku hasarına yol
açar.
Host-versus-graft-reaksiyonu
Greft sağkalım süreleri kseno <allo <izo- = oto-greft şeklinde
sıralanır. Rejeksiyon süresi ayrıca donör ve alıcı arasındaki
antijenik uyumsuzluğa bağlıdır. MHC antijenleri redde majör
etkiliyken, minör doku uygunluk antijenleri de ayrıca rol oynar.
Birçok minör doku uygunluk antijenlerinin uyumsuzluğuna bağlı
rejeksiyon MHC antijeni aracılı ret kadar ya da daha hızlı olabilir.
Diğer bağışıklık yanıtlarında olduğu gibi, immünolojik hafıza ve
sekonder yanıt greft rejeksiyonunda da vardır. Böylece, bir greft
alıcı tarafından reddedildiğinde, aynı donörden ikinci nakil ve ya
donörle aynı doku uyum antijenlerine sahip bir greft çok daha kısa
bir süre içinde reddedilecektir.
|
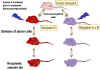 Şekil 3
Şekil 3
Graft versus host hastalığı |
Graft-versus-host (GVH)
Reaksiyonu
İmmun yetmezliği olan konakçıya
doku-uyumlu lenfoid hücreler enjekte edildiğinde kolayca kabul
edilirler. Ancak, nakil yapılan hücreler arasında imünokompetan T
lenfositler alloantijenleri tanır, cevap olarak prolifere olurlar ve
giderek artan konak doku ve hücre hasarına neden olurlar. Bu durum
graft-versus-host (GVH) hastalığı olarak (Şekil 3) bilinir ve
sıklıkla ölümcüldür. GVH reaksiyonunun (Şekil 4) yaygın bilinen
belirtileri ishal, eritem, kilo kaybı, halsizlik, ateş, eklem
ağrıları, vb ve sonuçta ölümdür.
|
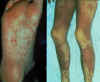 Şekil 4
Şekil 4
Graft versus host hastalığı |
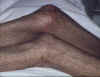 Yaygın, neredeyse birleşen hiperpigmente likenoid papüller ve diz
üzerinde toksik epidermal nekroz benzeri görünüm ile erken kronik
graft-versus-host reaksiyonu
Yaygın, neredeyse birleşen hiperpigmente likenoid papüller ve diz
üzerinde toksik epidermal nekroz benzeri görünüm ile erken kronik
graft-versus-host reaksiyonu
© Bristol Biyomedikal Görüntü Arşivi. Izin alınarak
kullanıldı.
 Sırtta hiperpigmente sklerotik plaklar ile geç kronik
graft-versus-host reaksiyonu.
Sırtta hiperpigmente sklerotik plaklar ile geç kronik
graft-versus-host reaksiyonu.
© Bristol Biyomedikal Görüntü Arşivi. Izin alınarak
kullanıldı
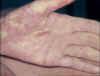 Parlak palmar eritem ile akut graft-versus-host reaksiyonu
Parlak palmar eritem ile akut graft-versus-host reaksiyonu
© Bristol Biyomedikal Görüntü Arşivi. Izin alınarak
kullanıldı
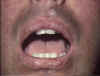 Dudakların erken, kronik, diffüz, yaygın likenoid değişiklikleri ile
graft-versus-host reaksiyonu
Dudakların erken, kronik, diffüz, yaygın likenoid değişiklikleri ile
graft-versus-host reaksiyonu
© Bristol Biyomedikal Görüntü Arşivi. Izin alınarak
kullanıldı
 Graft-versus-host reaksiyonu; interepidermal nekrotik keratinositler
ile akut bazal hücre hidropik dejenerasyonu
Graft-versus-host reaksiyonu; interepidermal nekrotik keratinositler
ile akut bazal hücre hidropik dejenerasyonu
© Bristol Biyomedikal Görüntü Arşivi. Izin alınarak
kullanıldı
 Graft-versus-host reaksiyonu; erken kronik hiperkeratoz ve
hipergranüloz, düzensiz akantoz, sitoid cisimcik ve liken planusu
anımsatan bazal hücre hidropik dejenerasyonu
Graft-versus-host reaksiyonu; erken kronik hiperkeratoz ve
hipergranüloz, düzensiz akantoz, sitoid cisimcik ve liken planusu
anımsatan bazal hücre hidropik dejenerasyonu
© Bristol Biyomedikal Görüntü Arşivi. Izin alınarak
kullanıldı
|
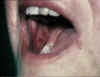 Graft versus-host-reaksiyonunda ağız mukozada akut erezyon
Graft versus-host-reaksiyonunda ağız mukozada akut erezyon
© Bristol Biyomedikal Görüntü Arşivi. Izin alınarak
kullanıldı. |
 Şekil 5
Şekil 5
Insan MHC gen kompleksi |
MHC GEN KOMPLEKSİ
MHC kompleksi çoğu allograft reddini etkileyen çeşitli
antijenleri kontrol eden bir dizi gen içerir. Bu antijenler (ve bunların
genleri): Sınıf I, Sınıf II ve Sınıf III şeklinde üç ana sınıfa
ayrılabilir. Sınıf I ve sınıf II antijenleri hücre ve dokularda ifade
edilirken, sınıf III antijenleri serumdaki ve diğer vücut sıvılarındaki
proteinler (C4, C2, faktör B, TNF vb.) üzerinde eksprese edilmektedir.
Sınıf III gen ürünlerinin antijenleri greft reddinde herhangi bir rolü
yoktur.
İnsan MHC
MHC kromozom 6 üzerine yerleşmiştir.
Sınıf I MHC
Sınıf I gen kompleksi B, C ve A olarak üç majör
lokus ve tanımlanmamış başka bir minör lokus (Şekil 5) içerir.
Her majör lokus bir polipeptidi kodlar; antijenik
determinantları içeren alfa zinciri polimorfiktir (birçok alleli
vardır). Beta-2 mikroglobulin (beta zinciri) ile ilişkilidir,
MHC kompleksi dışındaki bir gen tarafından kodlanır ve hücre
yüzeyi üzerinde eksprese edilir. Beta-2 mikroglobulin olmadan,
sınıf I antijen, hücre yüzeyi üzerinde eksprese edilmez.
Defektif beta-2-mikroglobulin geni olan bireyler hiçbir sınıf I
antijeni eksprese edemez ve bu nedenle, sitotoksik T hücre
kusuru mevcuttur.
Sınıf II MHC
Sınıf II gen kompleksi de DP, DQ ve DR olmak
üzere en az üç lokus içerir; bu lokusların her biri sınıf II
antijenleri oluşturmak için birbiri ile ilişkili kuran bir alfa-
ve bir beta-zincir polipeptid kodlar. Sınıf I antijenleri gibi,
sınıf II antijenleri de polimorfiktir. lokusu birden fazla,
muhtemelen dört işlevsel beta zinciri geni içerir.
|
 Şekil 6A
Şekil 6A
Fare MHC kompleksi |
Fare MHC Fare MHC’si
kromozom 17 üzerinde yer almaktadır.
Sınıf I MHC K ve D olarak iki
majör lokustan oluşur. Bu insan MHC aksine, fare sınıf I gen kompleksi
lokusları birlikte değildir ve sınıf II ve sınıf III genleri tarafından
ayrılmışlardır (Şekil 6A). Sınıf II MHC
Sınıf II gen kompleksi, her biri sınıf II molekülünü oluşturmak üzere
bir alfa ve bir beta zinciri polipeptit için kodlanan A ve E olmak üzere
iki locus içerir. Fare sınıf II gen kompleksi, bölge I olarak da bilinir
ve belirli antijenlere karşı farklı fare türlerinde bağışıklık yanıtın
büyüklüğünü belirlediği için bu kompleks içindeki genler Ir (bağışıklık
yanıtı) genleri olarak adlandırılır. A ve E locusu ürünleri IA ve IE
antijenleri olarak da isimlendirilirler, topluca Ia antijenleri olarak
bilinirler.
|
 Şekil 6B
Şekil 6B
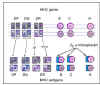
MHC antijenlerinin kodominant ekspresyonu |
MHC ANTİJENLERİ
Terminoloji HLA
grupları lokusu bir harf ve bir numara (A1, B5, vs.) ile tanımlanır ve
haplotipler her bir gruba göre belirlenir (örneğin, A1, B7 Cw4, DP5,
DQ10, DR8). Genomik analiz (PCR) ile tanımlanan gruplar, lokus için bir
harf ve dört haneli bir sayı ile isimlendirilir (örneğin A0101, B0701,
C0401 vs).
Fare MHC grubu (H-2) numarayla tanımlanır. Laboratuar fareleri soy içi
ürediğinden, her bir tür homozigottur ve tek bir haplotipe sahiptir. Bu
türlerde MHC haplotipi 'küçük' bir harf (a, b, d, k, q, s, vs.) ile
belirtilir; örneğin, Balb/c farelerinin MHC haplotipi H2d’dir.
Kalıtım Her ebeveynden
birer tane gelen MHC genleri grup olarak (haplotip) kalıtılır. Böylece,
heterozigot insan kalıtımında her biri üç sınıf I (B, C ve A) ve üç
sınıf II (DP, DQ ve DR) lokus içeren bir babadan ve bir anneden haplotip
aktarılır. Bir heterozigot bireyde en fazla 6 sınıf I kalıtımla
alabilecektir (Şekil 6). Benzer şekilde, birey DP ve DQ genlerini de
aktarır ve her iki ebeveyn antijenlerini eksprese eder. Sınıf II MHC
molekülü her bir zincir üzerinde bazı antijenik determinantlar (gruplar)
mevcut iki zincirden (alfa ve beta) oluştuğu ve DR alfa ve beta
zincirleri hem cis (her ikisi de aynı ebeveynden) hem de trans (her
ebeveynden birer tane) kombinasyonda bağ kurabildiği için bir birey ek
DR gruplarına sahip olabilir (Şekil 6B). Aynı zamanda, birden fazla
işlevsel DR beta zinciri genleri bulunmaktadır (şekilde gösterilmemiştir).
Bu nedenle, birçok DR grupları herhangi bir kişide bulunabilir.
|
| |
Çapraz geçiş
(Crossover)
Haplotipler, normalde, tümden
kalıtımla aktarılır ve dolayısıyla farklı lokuslar tarafından kodlanan
antijenler birlikte kalıtılır (örneğin, A2, B27, Cw2, DPw6, DQw9, DRw2).
Ancak, bazen iki ebeveyn kromozomları arasında çapraz geçiş olur, bu da yeni
rekombinant haplotip oluşumuyla sonuçlanır. Böylece, bir lokus tarafından
kodlanan herhangi bir özellik diğer lokustan gelen bir özellikle
birleşebilir. Bu belirli bir popülasyonun MHC görünümünde çok geniş bir
heterojenite ile sonuçlanır.
Hücreler üzerindeki
MHC antijen ekspresyonu
MHC antijenleri, ko-dominant bir
şekilde hücre yüzeyinde eksprese edilir: her iki ebeveyne ait gen ürünleri
aynı hücreler üzerinde bulunur. Ancak, her hücre hem sınıf I hem de sınıf II
antijenleri birlikte eksprese etmez. Sınıf I antijenler tüm çekirdekli
hücreler ve plateletlerde (ve farede, kırmızı kan hücreleri) eksprese
edilirken sınıf II antijenlerin ekspresyonu daha selektiftir. B
lenfositlerde, makrofajlar ve monositlerin bir kısmında, deri ilişkili (Langerhans)
hücrelerde, dendritik hücrelerde ve bazen de diğer hücrelerde eksprese
edilir.
Serolojik testlerle
MHC saptanması
MHC sınıf I antijenleri serolojik
yöntemlerle (Ab ve C) tespit edilir. Daha önce, HLA doku tiplendirmesi için
serum, doğumda çocuğun paternal antijenlerine maruz kalmış ve daha sonra bu
antijenlere karşı antikor geliştirmiş multipar kadınlardan elde ediliyordu.
Yakın zamanda, bunlar monoklonal antikor teknolojisi ile üretilmeye başlandı.
Laboratuarların çoğunun doku tiplemesi için PCR’a geçişiyle, Serolojik
yöntemlerin kullanımı hızla azalmaktadır.
Karma lökosit
reaksiyonu (MLR) ile MHC saptanması
Bir donörden alınan lenfositler
ilişkisiz başka bir donör lenfositleri ile kültüre edildiğinde
proliferasyonlarının uyarıldığı gözlenmiştir. Bu proliferasyonun temel
olarak sınıf II MHC (DR) uyumsuzluğuna bağlı olduğu ve bir bireyin T-hücrelerinin
allojenik sınıf II MHC antijen taşıyan hücrelerle (B hücreleri, dendritik
hücreler, langerhans hücreleri vb. ) etkileşim içinde olduğu tespit
edilmişdir. Bu reaktivite karma lökosit reaksiyonu (MLR) olarak
adlandırılmıştır ve doku uyumu derecesinin incelenmesi için kullanılmıştır.
Bu testte, test lenfositleri (tepki hücreleri), alıcının ışınlanmış veya
mitomisin C ile işlenmiş B-lenfositleri ve monositleri (stimülatör hücreler)
ile karıştırılır. Hücreler 4- 6 gün süre ile kültüre edilir. Tepkici T
hücreler donörde bulunan yabancı sınıf II antijenleri tanıyarak
transformasyon (DNA sentezini ve büyüme: blastogenezis) ve proliferasyona (mitogenez)
uğrar. Yabancı sınıf II antijenlere yanıt veren T hücreleri sıklıkla CD4 +
TH-1 tipi hücrelerdir. Bu değişiklikler kültüre radyoaktif (trityumlu, 3H)
timidin ilave edilerek kaydedilir ve DNA’ya katılımı görüntülenir.
|
 Şekil 7
Şekil 7
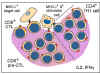
MLR süresince CTL aktivasyonu |
Sitotoksik T lenfosit
Üretimi
MHC antijeni ve T hücresi etkileşiminin diğer bir sonucu,
sitotoksik T-lenfositlerin uyarılmasıdır. T-lenfositler allojenik
lenfositler ile kültürü yapıldığında, mitoz uğramaya (MLR) ek olarak,
stimüle edilmiş MLR tipindeki hücrelere için de sitotoksik hale gelirler (Şekil
7). Böylece, 'x' haplotip T-lenfositler, 5-7 gün boyunca 'y' haplotip B
lenfositleri ile kültüre edildiğinde mitoza uğrarlar ve hayatta kalan T-lenfositler
'y' haplotip hücrelerine sitotoksik olur. MLR'deki mitoz indüksiyonu yalnız
sınıf II antijenleri arasında uyumsuzluk gerektirirken, sitotoksik T
lenfositlerin (STL) indüksiyonu hem sınıf I hem de sınıf II uyumsuzluğu
gerektirir. Ancak, sitotoksik hücreler bir kez uyarılınca, efektör
sitotoksik hücreler yalnız sınıf I antijenleri tanıyarak sitoksisiteye neden
olurlar.
|
 Şekil
8 Şekil
8
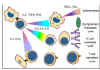
Allogreft destrüksiyon mekanizmaları |
ALLOGRAFT REDDİ
MHC’nin klinik önemi, organ naklinde anlaşılmıştır.
Hücreler ve dokular bir dizi hastalığın tedavisinde rutin olarak
transplante edilir. Ancak, konağın greftin allo-antijenlere karşı
reaksiyonu (HVG) redle sonuçlanır ve bu organ naklinde büyük engel
oluşturur. Greftin red süresi, greftin antijenik doğasına ve konağın
bağışıklık durumuna göre değişir ve çeşitli immün mekanizmalar ile
tespit edilir (Şekil 8 ve Tablo 1).
Hiper-akut
rejeksiyon
Alıcının yüksek titrede, önceden oluşturulmuş
antikorlara sahip olduğu durumlarda ortaya çıkar. Greft dakikalardan
saatlere kadar olan süre içinde hızlı antikor ve kompleman
reaksiyonuna bağlı rejeksiyon bulgularını gösterebilir.
|
| |
Akselere (ikincil;
sekonder) rejeksiyon
İlk greftle anlamlı miktarda antijenik determinant paylaşan
ikinci bir greft nakledilmesi hızlı bir ret ile (2-5 gün) sonuçlanır. Bu ilk
greft reddi sırasında sensitize olanT-lenfositlerin varlığına bağlıdır..
Akselere rejeksiyon hızlı lenfokin üretimi, monosit ve makrofaj aktivasyonu
ve sitotoksik lenfositlerin indüksiyonuyla gerçekleşir.
|
Tablo 1. Greft reddinin farklı
paternleri |
|
Red Türü |
Aldığı süre |
Nedeni |
|
Hiper-akut |
Dakikalar-saatler |
Önceden
oluşmuş anti-donör antikorlar ve kompleman |
|
Akselere |
Günler |
Sensitize T
hücrelerin reaktivasyonu |
|
Akut |
Günler - haftalar |
T hücrelerin
primer aktivasyonu |
|
Kronik |
Aylar-yıllar |
Nedeni belirsiz: antikorları, immun kompleksler, yavaş hücresel
reaksiyonlar, hastalığın rekürrensi. |
Akut (İlk; primer)
rejeksiyon
Yabancı transplantın ilk greftlenmesini takip eden normal
reaksiyon 1-3 hafta alır. Bu akut ret olarak bilinir ve allogreftin sınıf I
ve sınıf II antijenlerine karşı sensitize olmuş T lenfositler, lenfokinlerin
oluşumu ile monosit ve makrofajların aktivasyonu aracılık eder.
|
 Şekil
9A Şekil
9A
Böbrek naklinde greft rejeksiyonu
© Bristol Biyomedikal Görüntü Arşivi. Izin alınarak
kullanıldı. |
Kronik rejeksiyon
Bazı greftler aylarca hatta yıllarca canlı kaldıktan sonra aniden red
belirtileri gösterebilir. Mekanizması tam olarak net olmayan bu durum kronik
rejeksiyon olarak anılır. Hipotezler, ilk organ yetmezliğine yol açan
enfeksiyona, greft ile indüklenen tolerans kaybına vb. bağlı olabileceği
yönündedir.
Bir allogreft olarak fetus
Fetüs, anne ve babanın her ikisinden gelen antijenleri taşıyan kalıtsal
olarak farklı memeli türleridir. Bu yüzden, fetusun gerçekten bir
allogrefttir ve anne normalde fetusu yabancı olarak tanımalı ve fetus
reddetmelidir. Bununla birlikte, bu tür bir rejeksiyon nadiren görülür.
Çünkü memeliler anne karnındaki embriyoların implantasyonunu ve sonrasında
hayatta kalmasını sağlayan bir şekilde adapte olmuştur. Bunda rol oynayan,
en önemlisi plasentanın eşsiz yapısı ve fonksiyonu olmak üzere birçok
mekanizma vardır.
İmmünolojik olarak ayrıcalıklı
bölgeler ve dokular
Vücutta allogreftin kolayca reddedilmeyeceği bazı yerler vardır. Bunlar
beyin, gözün ön kamarası, testis, böbrek tübülü, rahim vb içerir. Bu durum
böyle bölgelerin iyi lenfatik drenajlarının olmamasından kaynaklanır. Ayrıca,
bu tür dokular Fas ligandı gibi, bu dokularla ilişkiye geçebilen herhangi
bir immün hücreyi öldüren molekülleri eksprese edebilir. Ek olarak, bu tür
dokular, diğer bağışıklık baskılayıcı mekanizmalara da sahip olabilir.
Benzer şekilde, uygunluk olmadan ve reddedilmeden nakledilebilen bazı
dokular vardır. Bu tür dokular, immünolojik olarak ayrıcalıklı dokular
olarak adlandırılır. Korneal greft, her türlü organ transplantasyonları
içinde en yüksek başarı oranına sahip, mükemmel bir örnektir. Donör ve alıcı
HLA antijenlerinin normalde uyumlu olmaması gerçeğine rağmen greft reddi
insidansının düşük olması etkileyicidir. Bu tür greftlerin neden kabul
edildiğiyle ilgili pekçok açıklama vardır. Greft yatağının avaskülaritesi
kornea alloantijenlerin bölgesel lenfoid dokulara ulaşmasını önler. Ayrıca,
kornea antijenler maskelenebilir. Bu tür mekanizmaların hepsi birlikte,
alıcının bağışıklık sistemini aktive etmektesinde başarısızlığa neden olur.
|
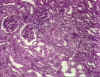 Şekil
9B Şekil
9B
Böbrek naklinde kronik greft rejeksiyonu
© Bristol Biyomedikal Görüntü Arşivi. Izin alınarak
kullanıldı. |
GREFT SAĞKALIMINI
ARTIRMAK İÇİN PROSEDÜRLER
Klinik pratikte, en başarılı transplantasyon programları böbrekler ve
kornealar ile olmuştur. Bununla birlikte, diğer organlar artan sıklıkta
transplante edilmektedir. Bu programlarda başarı, immünolojik mekanizmaların
daha iyi anlaşılmasına, MHC antijenlerinin tanımlanmasına ve daha etkili
immünsupresif ajanların geliştirilmesine bağlı sağlanmıştır.
Donör seçimi
Böbrek nakli ile geniş deneyimlere
dayanarak, pek çok organ nakli için donör seçimi ve alıcı hazırlanmasında
belirli rehberler takip edilebilir. Donör seçiminde en önemlisi alıcı ile
MHC uyumudur; tek yumurta ikizleri ideal donördür. HLA-uyumlu kardeşten
greftlerin % 95-100 başarı şansı vardır. Bir haplotip-uyumlu ebeveyn veya
kardeşin HLA D bölgesinde uyumluluk olmalıdır. D bölgesi antijeni için makul
bir uyum ile iki haplotip olarak farklı verici de kullanılabilir. İki veya
tek DR uyumlu kadavradan organlar da bazen başarıyla kullanılmaktadır. Her
durumda, ABO uyumluluğu gereklidir.
Alıcı hazırlığı
Alıcı enfeksiyonlu ve hipertansif
olmamalıdır. 1-2 hafta aralıklarla donörden bir ila beş kez 100-200 ml’lik
tam kan transfüzyonu greft sağkalımını arttırır ve mümkün olduğunda
uygulanmaktadır.
İmmünosüpresyon
Immunosupresif tedavi
allo-transplantasyonun en önemli parçasıdır. Bu etkenlerin en yenileri ve en
etkililerin olduğu ailede Siklosporin A, FK-506 (takrolimus) ve rapamisin
bulunmaktadır. Siklosporin A ve FK506 Ag-reseptör bağlanmasını takip eden
IL-2 sentezini inhibe ederken, rapamisin IL2-IL2 reseptörü etkileşimi
sonrası sinyal transdüksiyonunu engeller. Böylece, bu üç ilaç da antijene
yanıt olarak gerçekleşenT hücresi proliferasyonunu önlemektedir. Greft
reddini önlemek için kullanılan diğer kimyasal maddeler ve etki yolları
Tablo 2’de listelenmiştir. Lösemili hastalarda kemik iliği nakli öncesinde
tüm vücut ışınlaması kullanılır. Ayrıca T hücrelere karşı antiserum (anti-timosit
globulin: ATG) ya da yaktive T hücrelerin yüzey antijenleri de (aktiveT-hücrelerde
CD3, CD4, CD45, CD25: IL-2 reseptörleri) immünosupresyon elde etmek için
kullanılmaktadır (Tablo 2).
|
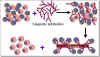 Şekil 10
Şekil 10
İlik greftinden T hücrelerin uzaklaştırılması |
Kemik iliği nakli için
stratejiler
Kemik iliği transplantasyonu için donör seçiminde en önemli
faktör sınıf II MHC uyumluluğudur. tek yumurta ikizleri ideal donördür. Kötü
uyumlu greftlerden monoklonal antikorları kullanılarak T lenfositler
uzaklaştırılabilir (Şekil 10). Alıcının immunsüprese olması gerekir. Malign
hücreler (kan kökenli malignite durumunda) alıcı kanından temizlenmeli.
Metotreksat, siklosporin ve prednizon GVH hastalığı kontrol etme amaçlı
sıklıkla kullanılır.
|
| |
Diğer greftler
Kornea greftler D bölge antijenleri içermezler ve
dolayısıyla sıklıkla sağkalırlar. Küçük greftler daha iyidir ve
kortikosteroidler yararlıdır.
Cilt allogreftlerin başarı oranı çok düşüktür ve
immünsupresif tedavi nispeten etkisizdir. Bununla birlikte, çoğu zaman ciddi
cilt hasarının iyileşmesini desteklemek için geçici bir koruma sağlamada
kullanılır. Sonuç olarak, alıcı ve donör mükemmel uyumlu (tek yumurta
ikizleri) veya alıcı verici MHC antijenlerine (kemik iliği Chimerleri)
toleran olduğunda hiçbir ret olmayacaktır.
|
Tablo 2. Seçilmiş
immunsupresif ajan örnekleri |
|
Ajan |
Muhtemel etki yolu |
Uygulama(lar) |
|
Kortikosteroid, prednizon |
anti-enflamatuar, T-hücresi ve PMN hareketinin değişimi |
organ nakli, aşırı duyarlılık, otoimmun hastalıklar |
|
Siklosporin, FK-506 |
IL-2 sentezinin inhibisyonu |
organ nakli |
|
Rapamisin |
IL-2-IL-2R sinyal blokajı |
organ nakli |
|
Azatioprin, 6-MP |
pürin metabolizması |
organ nakli, otoimmunite |
|
Metotreksat |
folat metabolizması |
organ nakli, otoimmunite |
|
Siklosporin, melfalan |
DNA,RNA ve proteinlerin alkilasyonu |
organ nakli, otoimmunite |
MHC’nin hastalıklarla ilişkisi
Bazı hastalıkların, belirli MHC
haplotipleri olan kişilerde daha yüksek sıklıkta oluştuğu tespit edilmiştir.
Bunların arasında en belirgin olanları ankilozan spondilit (B27), çölyak
hastalığı (DR3) ve Reiter’s sendromu (B27)’dur. Farklı MHC grupları ile
ilişkili diğer hastalıklar Tablo 3'te sıralanmıştır. Bu ilişki için bilinen
kesin bir neden yoktur. Bununla birlikte, birçok hipotezler önerilmiştir:
patojenler ve MHC arasındaki antijenik benzerlik, sınıf II genler tarafından
kontrol edilen antijenik hipo- ve hiper- yanıt bunlar arasındadır.
|
Tablo 3. Önemli HLA örnekleri
ve hastalıkla ilişkileri |
|
Hastalık |
İlişkili Alleller |
Sıklık |
Rölatif Risk |
|
Hastalar |
Kontrol |
|
Ankilozan spondilit
|
B27
|
90
|
9
|
87.4
|
| Reiter’s hastalığı (sendromu) |
B27 |
79 |
9 |
37.0 |
| Akut anterior üveit (Şekil
11) |
B27 |
52 |
9 |
10.4 |
| Psöriazis vulgaris (Şekil
11) |
Cw6 |
87
|
33 |
13.3 |
| Dermatitis herpetiformis
(Şekil 11) |
DR3 |
85 |
26
|
15.4 |
| Çölyak Hastalığı |
DR3 |
79 |
26
|
10.8 |
| İnsülin bağımlı diyabetes
mellitus |
DR3/4 |
91 |
57 |
7.9 |
|
 Şekil 11 Elde psöriazis
Şekil 11 Elde psöriazis
© Bristol Biyomedikal Görüntü Arşivi. Izin alınarak kullanıldı. |
 Psöriazis
Psöriazis
© Bristol Biyomedikal Görüntü Arşivi. Izin alınarak
kullanıldı.
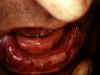 Dermatitis Herpetiformis: Ağız Mukozası
Dermatitis Herpetiformis: Ağız Mukozası
© Bristol Biyomedikal Görüntü Arşivi. Izin alınarak
kullanıldı.
 Üveit
Üveit
© Bristol Biyomedikal Görüntü Arşivi. Izin alınarak kullanıldı.
|
| |
Bunlar
öğrendiniz
Host-versus-graft (HGV)’ta MHC’nin rolü ve
graft-versus-host (GVH) hastalığı.
İki MHC moleküllünün genetiği.
Popülasyondaki MHC antijenlerinin
heterojenitesinde polimorfizmin ve çapraz geçişin rolü.
MHC antijenlerinin tespit yöntemleri (doku
tiplemesi).
Transplant reddinde immün mekanizmalar.
Başarılı transplantasyon için stratejiler.
|
|
|
 Mikrobiyoloji ve İmmünoloji On-line, İMMÜNOLOJİ Bölümüne Dönünüz
Mikrobiyoloji ve İmmünoloji On-line, İMMÜNOLOJİ Bölümüne Dönünüz
This page last changed on
Thursday, March 31, 2016
Page maintained by
Richard Hunt
|

 Şekil 2
Şekil 2 Şekil 3
Şekil 3 Şekil 4
Şekil 4 Graft versus-host-reaksiyonunda ağız mukozada akut erezyon
Graft versus-host-reaksiyonunda ağız mukozada akut erezyon Şekil 5
Şekil 5 Şekil 6A
Şekil 6A Şekil 6B
Şekil 6B  Şekil 7
Şekil 7  Şekil
8
Şekil
8 Şekil
9A
Şekil
9A Şekil
9B
Şekil
9B Şekil 10
Şekil 10  Şekil 11 Elde psöriazis
Şekil 11 Elde psöriazis 









