|
ÖĞRENİM HEDEFLERİ
Tolerans kavramı ve öneminin kavranması
Toleransı indükleyen ve belirleyen faktörlerin bilinmesi
Toleran indüksiyon mekanizmaları
Otoimmünite kavramının anlaşılması
Major otoimmün hastalıkların özellikleri
Otoimmün hastalık etyolojilerinde çeşitli teorilerin öğrenilmesi
|
TOLERANS
GİRİŞ
Tolerans aynı antijene bir antijene karşı spesifik bağışıklık
tepkimesizliğini anlamına gelir. Tolerans en önemli şekli, kendi
antijenlerine tepkime vermemsi iken, öz olmayan antijenlere karşı
tolerans görülmesi de mümkündür. Bir antijen toleransı indüklüyorsa bu
antijen tolerojenik olarak adlandırılır.
ÖZ (SELF)
ANTİJENLERE KARŞI TOLERANS
Normalde, öz (self)
antijenlere karşı kuvvetli bir immün cevap oluşmamaktadır, bu fenomen
“self-tolerans” olarak adlandırılır. İimmün sistem öz antijenleri
tanıdığı ve kuvvetli bir immün cevap oluşturduğu durumlarda otoimmün
hastalıklar gelişmektedir. Yine de, immün sistem, yabancı antijene
cevabı düzenlemek için self-MHC’leri tanımak zorundadır. Böylece, immün
sistem sürekli olarak self, non-self ayırımı yapmakta ve doğru cevabı
düzenlemektedir.
YAPISAL OLMAYAN (NON-SELF)
ANTİJENLERE KARŞI TOLERANSIN UYARILMASI
Antijenin değişmesiyle,
antijenin ağız gibi özel bir yoldan verilmesiyle, antijenin immün sistem
gelişirken alınması gibi yollarla non-self (yabancı) antijenlere karşı
tolerans tetiklenebilir. Birtakım bakteri ve virüsler toleransı
tetikleyen yollar geliştirmiştir böylece konak bu mikroorganizmaları
öldürmemektedir. Örneğin lepramatöz tip lepra hastaları, Mycobacterium
leprae’ya karşı immün cevap oluşturmamaktadır.
DOKU VE HÜCRELER KARŞI
TOLERANS
Doku ve hücreler karşı
tolerans yeni doğanda hemopoetik (kök) hücrelerin enjeksiyonu veya
şiddetli immün yetmezlikli (letal radyasyon veya ilaç ile muameli
edilmiş) hayvanlarda sağlanabilmektedir. Aynı zamanda allojenik kemik
iliği veya timusun yaşamın erken dönemlerinsde nakli ile verici hücre ve
dokularınatoleransla sonuçlanır. Bu tip hayvanlar kimera olarak
bilinirler. Bu bilgiler, kemik iliği nakli uygulamalarında pratik öneme
sahiptir.
|
| |
ÇÖZÜNEBİLEN ANTİJENLERE
KARŞI TOLERANS
Birçok T bağımlı ve T bağımsız antijene karşı tolerans durumu,
çeşitli deneysel modellerle gerçekleştirilmiştir. Bu çalışmalar ile bir
antijenin immün sistemi uyaracağı veya toleransı uyaracağı ile ilgili bir çok
faktörün rol oynadığı bulunmuştur (Tablo 1).
|
Tablo 1
Antijene maruziyet sonrası tolerans veya immün sistemin uyarılmasını
belirleyen faktörler
|
|
Antijene cavabı etkileyen
faktörler |
İmmün cevap lehine |
Tolerans lehine |
|
Antijenin şekli |
Büyük, agrage olmuş, kompleks moleküller |
Soluble, aggregatsız, görece küçük,daha az kompleks
moleküller, ASH tarafından işlenmeyen antijenler veya sınıf II MHC
dışında işlenen antijenler |
|
Antijenin verilme yolu |
Deri altı veya kas içi |
Oral veya bazen damar içi |
|
Antijen dozu |
Optimal doz |
Çok büyük (veya bazen çok küçük) doz |
|
Hayvanın yaşı |
Yaşlı ve immünolojik olarak olgun |
Yeni doğan (fare), immünolojik olarak immature |
|
Hücrelerin farklılaşma düzeyi |
Tam farklılaşmış hücreler, hafıza T ve B hücreleri |
Görece farklılaşmamış: sadece IgM taşıyan B hücreler (IgD
yok), T hücreler (örneğin timik korteksteki hücreler) |
TOLERANSIN İMMÜNOLOJİK
ÖZELLİKLERİ
Tolerans, immünsüpresyon ve immünyetmezlikten farklı bir
durumdur. Antijene cevapta, aktif bir antijen-bağımlı bir prosesdir. İmmün cevap
gibi tolerans spesifiktir ve immünolojik hafıza gibi T hücreler, B hücreler veya
her ikisi bulunmaktadır ve T hücre düzeyinde tolerans B hücre düzeyinden daha
uzun süre devam eder.
T hücrelerde toleransın uyarılması kolaydır ve B hücre
toleransından görece olarak daha az tolerojene ihtiyaç duyar. İmmünolojik
toleransın devamı, antijenin uzun süre varlığına ihtiyaç duyar. Tolerans doğal
olarak bozulabilir (otoimmün hastalık gibi) ve edinilmiş olarak bozulabilir (deney
hayvanlarında gösterildiği gibi, x ışınları ile, bazı ilaç tedavileri ile ve
çapraz reaktif antijenlere maruziyet ile)
Tolerans bir antijen üzerindeki tüm epitoplara olabileceği gibi
bazı epitoplara karşı da olabilir ve tek bir antijene karşı tolerans B hücre, T
hücre veya her iki seviyede de olabilir.
|
| |
TOLERANS
İNDÜKSİYON MEKANİZMALARI
Toleransın uyarılmasının ve
devam ettirilmesinin tam mekanizmaları anlaşılmamıştır. Bununla birlikte
deneysel veriler birçok olasılık olduğunu işaret etmektedir.
Klonal
delesyon
Gelişim sırasında self
antijenlerle karşı karşıya gelen T ve B lenfositler apoptozis veya
programlanmış hücre ölümü olarak bilinen bir süreçle klonal
delesyona uğratılırlar. Örneğin, ilk olarak timusta gelişen T
hücreler CD4 ve CD8 ekprese etmemektedirler. Bu hücreler daha sonra
hem CD4 hem CD8 edinirler ve çift pozitif hücre olarak
adlandırlırlar ve düşük düzeyde αβ TCR eksprese ederler. Bu hücreler
cortikal epitelyum üzerinde eksprese edilen sınıf I veya sınıf II
moleküller ile etkileşim sonrası pozitif seleksiyona uğrarlar. Bu
işlem süresince, düşük aifiniteli MHC’ye sahip hücreler pozitif
olarak seçilirler. Seçilmeyen hücreler apoptozis ile öldürülürler.
Sonra hücreler CD8 veya CD4’lerini kaybederler. Bu T hücrelere
dentritik gürceler üzerindeki self MHC molekülleri ile self
peptitler sunulurlar. Yüksek afiniteli MHC+ resptörlü T hücreler
klonal delesyona uğrar ve bu durum negatif seleksiyon olarak da
bilinmektedir. Bu işlemlerdeki herhangi bir bozukluk otoreaktif T
hücrelerin kaçmasına yol açabilir ve otoimmün hastalıkları
başlatabilir. Benzer şekilde, erken B hücrelerinin farklışamasında
self antijenlerle karşılaşanlar delesyona uğrarlar. Böylece klonal
delesyon self antijenlere toleransta anahtar roloynamayı
sağlamaktadır.
Periferal tolerans
Klonal delesyon tam
anlamaıyla çalışan bir sistem değildir ve sıklıkla T ve B hücreler
delesyondankurtulurlar ve bu hücreler periferal lenfoid organlara
bir kez ulaştı mı potansiyel olarak otoimmün hastalıklara neden
olabilirler. Bu nedenle, immün sistem, toleransın devamı için ek
kontrol noktaları tasarlanmıştır.
Aktivasyonun
indüklediği hücre ölümü
Aktive T hücreler sadece
sitokin üretmez yada efektör fonksiyonlarını uygulamaz aynı zamanda
programlanmış hücre ölümü ile ölürler. Bu süreçte, ölüm resptörü (Fas)
ve onun ligangı (FasL) kritik rol oynar. Böylece, normal T hücreler
Fas ekprese ederler fakat FasL eksprese etmezler. Aktivasyon ile,
Thücreler Fas ile bağlanacak FasL eksprese ederler ve kaspaz-8’in
aktivasyonu ile apoptozisi başlatırlar. Fas (lpr mutasyonu) veya
FasL (gld mutasyonu) olan fareler üzerinde yapılan çalışmalarla Fas
ve FasL’nin önemleri açıkca gösterilmiştir. Bu farelerde ciddi
lenfoproliferatif ve otoimmün hastalık gelişirken ve 6 ay içerisinde
ölürlerken normal fareler 2 yıla kadar yaşamışlardır. İnsanlardaki
apoptotik genlerdeki benzer mutasyonlar otoimmün lenfoproliferatif
sendrom (APLS) olarak adlandırılan lenfoproliferatif hastalığa yol
açmaktadır.
Klonal anerji
Oto-reaktif T hücreleri,
antijen sunan hücre üzerindeki antijenik peptitlere yardımcı uyarıcı
CD80 (B7-1) veya CD86 (B7-2) olmadan maruz kaldığında antijene karşı
anerjik (cevapsız) olurlar. Aynı zamanda, CD28 yoluyla T hücrelerin
aktivasyonu IL-2 üretimini başlatırken, CTLA4’ün aktivasyonu
IL-2’nin üretilmesini ve anerjiyi inhibe eder. Aynı zamanda B
hücreleri çok miktarda soluble antijenle karşı karşıya kaldıklarında
yüzey IgM molekülünü down-regüle ederler ve anerjik olurlar. Bu
hücreler aynı zamanda yüzeylerindeki Fas moleküllerini upregüle
ederler. Bu B hücrelerinin Las ligand taşıyan T hücreleri ile
etkileşimi apoptozis ile hücdre ölümüne yol açar.
Klonal
habersizlik
Timusta sunulmayan self
antijenlere karşı aktif T hücreler olgunlaşak ve perifere göç
edecektir fakat asla uygun antijenle karşılaşmayacaklardır çünkü
ulaşılamayan dokularda tecrit edilmişlerdir. Bu tür hücreler uyarı
eksikliği nedeniyle ölebilirler. Delesyondan kaç otoaktif B hücreler
antijeni bulamayabilir veya özgül T hücreler yardımı olmayabilir ve
böylece aktive olamazlar ve ölürler.
Anti-idiotip
antikorlar
Bu antikorlar diğer
antikorların spesifik idiotiplerine karşı oluşmuşlardır. Anti-idiotip
antikorlar tolerizasyon süresince üretilirler ve tolerant
hayvanlarda demonstre edilmişlerdir. Bu antikorlar B hücre
reseptörünün antijenle etkileşime girmeşini önleyebilirler.
Regülatör T hücreleri (suppresör
hücreler)
Son zamanlarda, T
hücrelerinin belli bir popülasyonu regülatör T hücreleri olarak
adlandırılmaya başlanmıştır. Regülatör T hücrelerinin çok çeşitleri
bulunmaktadır fakat en iyi karakterize edileneleri CD4+ ve CD25+
olanlardır. Çünkü aktive olmuş CD4 T hücreleri aynı zamanda CD25
eksprese ederler, bu nedenle aktive Thücreler ile regülatör T
hücreleri ayırmak kolay değildir. Son çalışmalar regülatör T
hücrelerin transkripsiyon faktör Foxp3 expresyonu ile tanımlandığını
bildirmektedirler. Foxp3 ekspresyonu T hücre gelişimi ve fonksiyonu
için gereklidir. Hangi regülatör T hücrenin diğer T hücrelerin
fonksiyonlarını baskıladığı ile ilgili kesin mekanizma açık değildir.
Bu mekanizmalardan bir tanesi TGF-β ve IL-10 gibi immünosüpresif
sitokinlerin üretimidir. İnsanlarda Foxp3’de genetik mutasyonlar
immün disregülasyon, Poliendokrinopati, enteropati, X’e bağlı
sendrom (IPEX) olarak bilinen ciddi ve hızlı fatal otoimmün
bozukluklara yol açmaktadır. Bu hastalık, regülatör T hücrelerin
otoimmün hastalıklardan korunmada kritik bir rolünün olduğuna dair
en çarpıcı delili oluşturmaktadır.
Toleransın
sonlandırılması
Deneysel olarak
indüklenmiş tolerans, tolerajene uzun süre maruziyetin yokluğu ile,
immün sistemin ciddi zedelenmesi ile (x ışınları) veya çapraz
reaktif antijenlerle immünizasyon ile sonlandırılabilir. Bu
gözlemler otoimmün hastalıkların kavramsallaştırılmasında anlamlıdır.
|
| |
OTOİMMİNİTE
TANIM
Otoimmünite, self tolerans ile ilgili mekanizmaların
bozulması ve kendi komponentlerine karşı immün cevabın uyarılması olarak
tariflenebilir. Böyle bir immün cevap her zaman zararlı olmayanilir (örn,
anti-idiotip antikorlar). Fakat organizmanın kendisine zarar veren
birçok otoimmün hastalık tanımlanmıştır.
OTOİMMÜN
HASTALIKLARDA EFEKTÖR MEKANİZMALAR
Otoimmün hastalıklarda zedelenmede hem antikorlar hem de
efektör T hücreler rol oynamaktadır.
GENEL SINIFLAMA
Otoimmün hastalıklar genellikle kapsadıkları organ ve
doku temelinde sınıflandırılmaktadır. Bu hastalıklar immün sistemin
cevap verdiği antijenlerin bir organı hedef aldığı organ-spesifik
kataogoride olabileceği gibi antikorların bir organı hedef almayan organ
dışı otoimmün hastalık katragorisinde de olabilir (Tablo 2). Çoğu
otoimmün hastalıkta antijen hastalığın adından gelmektedir.
OTOİMMÜNİTEDE
GENETİK YATKINLIK
Fare çalışmaları ve insanlardaki gözlemler otoimmünite
için genetik yatkınlığın olduğunu düşündürmektedir. Belli HLA tipleri
ile otoimmün hastalıkların ilişkileri belirlenmiştir (HLA: B8, B27, DR2,
DR3, DR4, DR5 vb.).
|
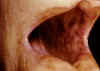 Şekil 1
Şekil 1
Addison's hastalığında oral mukazada hiperpigmentadyon
© Bristol Biomedical Archive. Used with permission
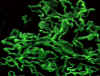 Şekil 2
Şekil 2
Goodpasture sendromunda IgG nin lineer immünofloresans boyanması
© Bristol Biomedical Archive. Used with permission
 Şekil 3
Şekil 3
Pemphigus vulgaris - immünofloresans
© Bristol Biomedical Archive. Used with permission
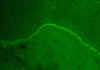 Şekil 4
Şekil 4
Mukoz membran pemphigoid - immünofloresens
© Bristol Biomedical Archive. Used with permission
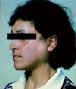 Şekil 5
Şekil 5
Sjogren's sendromunda parotid büyümesi
© Bristol Biomedical Archive. Used with permission
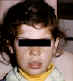
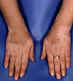 Şekil 6
Şekil 6
Vitiligoda depigmentasyon
© Bristol Biomedical Archive. Used with permission
|
OTOİMMÜN HASTALIKLARI
ETYOLOJİSİ
Otoimmün hastalıkların tam etyolojisi bilinmemektedir. Fakat,
çeşitli teroriler önerilmiştir. Bunlar, tecrit edilmiş antijenler, oto-reaktif
klonların kaçışı, süpresör hücrelerin kaybı, ekzojen antijenleri (patojenleri)
ve değişmiş öz antijenleri kapsayan çapraz reaktif antijenleri kapsamaktadır.
Tecrit edilmiş antijen
Lenfoid hücreler gelişimleri süresince bazı self antijenlere
maruz kalamamış olabilirler çünkü geç gelişen antijenler olabilir veya
özelleşmiş organlarda saklı tutulabilirler (örn: testisler, beyin, göz vb.).
Bu antijenlerin bu organlardan travmatik zedelenme veya cerrahi müdahale
sonrası dışarıya çıkışı immün cevabı uyarabilir ve otoimmün hastalığı
başlatabilir.
Oto-reaktif klonların kaçışı
Timustaki negatif seleksiyon self reaktif hücreleri tam
olarak elemine edemeyebilir. Tüm self antijenler timusta sunulamayabilir
veya belirli antijenler uygun işlenmeiş ve sunulmamış olabilir.
Regulatör T hücre
eksikliği
Bir çok otoimmün hastalıkta daha az regülatör T hücre
bulunmaktadır.
|
Tablo 2
Otoimmün hastalıkların spektrumu, hedef organlar ve tanısal testler
|
|
|
Haslaık |
Organ |
Antikor |
Tanısal test |
|
Organ-Spesifik

Organ spesifik değil
|
Hashimoto's thyroiditi
|
Tiroid |
Tiyroglobulin,
tiroid peroksidaz (mikrozomal) |
RIA, CF, hemaglutinasyon
|
|
Primer miksödem |
Tiroid |
Sitoplasmik TSH reseptör
|
İmmünofloresens
(IF) |
| Graves' hast. |
Tiroid |
|
Bioassay, TSH reseptör yarışı
|
| Pernisiöz anemi |
Eritrosit |
Intrinsik faktor
(IF), Gastrik parietal hüc |
B-12 bağlanması
IF immünofloresens
|
Addison's hast.
(Şekil 1)
|
Adrenal |
Adrenal hüc |
İmmünofloresens |
|
Prematu menopoz cgelişmi
|
Ovaryum |
Steroid üreten
hüc |
İmmünofloresens |
|
Erkek infertilitesi |
Sperm |
Spermatozoa |
Aglutinasyon
İmmünofloresens
|
|
İnsulin bağımlı juvenil diabet
|
Pankreas |
Pankreatic islet
beta hüc |
|
|
İnsülin dirençli diyabet
|
Sistemik |
Insulin reseptör |
Reseptör yarışı |
| Atopik allerji |
Sistemik |
Beta-adrenerjik reseptör
|
Reseptör yarışı |
| Myasthenia graves |
Kas |
Kas, asetil kolin reseptörü
|
İmmünofloresens, reseptör yarışı
|
|
Goodpasture's sendromu
|
Böbrek, akciğer
|
Böbrek ve akciğer
bazal membranı |
İmmünofloresens
(linear boyanma) (Şek. 2) |
| Pemfigus |
Deri |
Desmosom |
İmmünofloresens (şek.
3) |
| Pemfigoid |
Deri |
Deri bazal membranı
|
İmmünofloresens (şek.
4) |
| Fakogenik uveit |
Lens |
Lens protein |
|
| Hemolitik anemi |
Eritrosit
Platelet |
Eritrosit |
Pasif
hemagglutination
Direct Coomb's test |
|
İdiopatik trombositopeni
|
|
Platelet |
İmmünofloresens |
|
Primer bilier siroz
|
Karaciğer |
Mitokondri |
İmmünofloresens |
|
İdiopatik nötropeni
|
Nötrofil |
Nötrofil |
İmmünofloresens |
| Ülseratif kolit |
kolon |
Kolon lipopolisakkarit
|
İmmünofloresens |
| Sjogren's
sendromu |
Sekratuar bezler
(Şekil 5)
|
Mitokondri |
İmmünofloresens |
| Vitiligo |
Deri
|
Melanosit (fig 6) |
İmmünofloresens |
| Romatoid artrit |
Deri, böbrek,
eklem vb. |
IgG |
IgG-latex
aglutinasyon |
|
Sistemik lupuseritematosus
|
Eklem
|
DNA, RNA, nükleoproteinleri
|
RNA-, DNA-latex aglutinasyon, IF(böbrekte granular)
|
|
|
|
|
|
|
Hastalıklar organ
spesifikten (yukarı) daha az spesifiğe doğru (aşağı) sıralanmıştır. |
Çapreaz reaktif
antijenler
Bazı patojenlerin üzerindeki antijenler konak antijenleri
ile çapraz reaksiyon verebilen determinantlara sahip olabilir ve bu
determinantlaraı karşı oluşan immün cevap efektör hücrelerin veya
antikorları doku antijenleriyle etkileşime girmesine yol açabilir.
Streptekokal enfeksiyon sonrası nefrit ve kardit, sifiliz süresince görülen
antikardiolipin antikorları ve Klebsiella ile ankilozan spondilit arasındaki
ilişki bu tür çapraz reaksiyonlara örnektir.
TANI
Otoimmün hastalıkların tanısı, semptomlara ve doku ve
hücrelerdeki antijenlere karşı antikorların (ve/veya çok erken T hücreleri)
tespiti ile yapılmaktadır. Doku/hücre antijenlerine karşı oluşan antikorlar
immünofloresans yöntemi ile tespit edilebilmektedir. Soluble antijenlere karşı
oluşan antikorlar ELISA veya radyoimmünoassya ile tespit edilebilir. Bazı
durumlarda, biyolojik/biyokimyasal testler kullanılabilir (graves hast,
pernisiyöz anermi vb.)
TEDAVİ
Otoimmün hastalıkların tedavi amacı,vücudun enfeksiyonlara karşı
savaş kabiliyetinin devamını sağlabilecek bir şekilde semptomların azaltılmasını
ve otoimmün cevabın kontrol altına alınmasını kapsamaktadır: antienflamatuat (kortikosteroid)
ve immünosüpresif ilaç tedavisi (siklofosfamit, azotioprin, siklosporin)v şuanki
tedavi yöntemleridir. Çeşitli yeni tedavi yöntemleri ileri araştırmalarla
uygulanmaktadır: anti-TNF alfa tedavisi artritlerde, toleransın indüklenmesi
için oral yolla antijen verilmesi, anti-idiotip antikorlar, antijen peptitler,
anti-IL-2 reseptör antikorları, anti-CD4 antikorları ve anti-TCR antikorları
örnek olarak verilebilir.
OTOİMMÜN HASTALIK
MODELLERİ
Otoimmün hastalık çalışm aları için birçok deneysel ve doğal
hayvan modelleri bulunmaktadır. Deneysel modeller, deneysel atoalleriji
ensefalitler, deneysel troiditler, adjuvan indüksiyonlu artrit ve benzerleri
kapsamaktadır. Doğal oluşan modeller arasında ise NZB farelerinde hemolitik
anemi, NZB/NZW (BW), BXSB ve MRL farelerde sistemik lupus eritematosus ve obez
farelerde diabet modelleri yer almaktadır.
|

 Şekil 1
Şekil 1






