| x | x | |||||||
 |
||||||||
| BAKTERIYOLOJİ | İMMÜNOLOJİ | MYCOLOGY | PARASITOLOGY | VİROLOJİ | ||||
|
||||||||
| En Español | ||||||||
| SHQIP - ALBANIAN | ||||||||
|
Let us know what you think FEEDBACK |
||||||||
| SEARCH | ||||||||
|
|
||||||||
|
BU BÖLÜM ÇEŞİTLİ KISIMLARINDA SONRAKİ BÖLÜME GİTMEK İÇİN YUKARIDAKİ NEXT >>
düğmesini kullanın |
||||||||
|
DİĞER HIV VE AIDS BÖLÜMLERİ İÇİN LİNKLER BU sayfanın alt kısmında |
||||||||
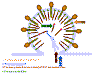
 Şekil 15
Şekil 15HIV’in infekte hücreden tomurcuklanması CDC
|
HIV İLE ENFEKTE OLMUŞ HÜCRELER
HIV AIDS'in işareti olan derin immün baskılanmasına neden olan özellikle CD4 + T4 hücreleri yok eder. Diğer bazı hücreler dendritik hücrelerde olduğu gibi, lizis yapmadan virusu çoğaltır ve barındırır veya onlar virüsu az veya hiç çoğaltmadan hücre yüzeyinde virüsü konsantre edebilir. HIV ile enfekte olmuş hücre tipleri Şekil 15c'de gösterilmektedir.
|
|||||||
 Şekil 15b
Şekil 15bBir lenfosit (solda) ile bir dendritik hücre (sağda) etkileşimi. dendritik hücre yüzeyine bağlı HIV böylece lenfositin enfeksiyonu kolaylaştıran iki hücre arasındaki etkileşimin (ok) yerinde kümelenmiştir. T4 hücreleri üzerinde, HIV reseptörleri de burada konsantre Steve Haley - William Bowers - Richard Hunt
|
||||||||
|
İnsan hücresi içine HIV girişi için CD4 antijeni ekspresyonu gerekliliği. HeLa hücrelerinde CD4 antijeni yoktur ve bulaşmaz. CD4 geni ile transfekte edilmiş HeLa hücreleri enfekte edilir |
T4 hücreleri hastalıkta tükenindiği gözlem ile birlikte, HIV ve
AIDS'in erken tarihinde görülen CD4 + hücre enfeksiyonu belirgin özgünlüğü (aslında,
bir hastada hastalığın seyri, CD4 + T hücre seviyeleri ile takip edilebilir),
CD4 antijenini virus reseptörü olabileceğini öne sürdürmüştür. Bu, (örneğin
servikal karsinom, HeLa hücreleri gibi) CD4-insan hücrelerine CD4 antijeni geni
transfekte edilmesi ve HIV ile enfekte olmasının mümkün olma özelliği ile ortaya
çıkartılmıştır (Şekil 16). CD4 antijeni HIV ile enfekte olmuş, T4 hücrelerinde
ve çoğu diğer hücrelerde hem HIV-1 hem de HIV-2 için önemli bir reseptördür.
|
|||||||
|
||||||||
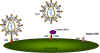 Şekil 17A
Şekil 17AKemokin reseptörleri HIV ile enfeksiyonda CD4 antijen ile birliktedir (sol). Kemokin, reseptörlerine virüsün bağlanmasını engelleyebilir (orta). Kemokin reseptöründe mutasyonlar HIV enfeksiyonuna dirence yol açabilir (sağ)
|
Başlangıçta yalnızca CD4 antijeni sahip hücreler HIV tarafından enfekte olabileceği düşünüldü. CD4 proteininin bazı infekte olabilen hücreler üzerinde gösterilememiş olmasına rağmen, düşük miktarlarda mevcut olduğu düşünüldü ve çoğu infekte olabilen hücrede CD4 antijen mRNA tespit edilebildi. CD4 pozitif hücrelere spesifikliği CD4 gp120 spesifik bağlanmasını gösterir. Artık, beyin ve bağırsak da dahil olmak üzere bazı non-CD4 hücreler, bir galactocerebroside reseptörü aracılığı ile enfekte edilebileceği biliniyor. Diğer hücreler farklı bir şekilde enfekte olabilir; örneğin, makrofajlar bir Fc (aşağı bakınız) ya da kompleman reseptörü kullanılabilir. Bu gibi durumlarda, HIV, hücre yüzeyi üzerindeki reseptörler ile etkileşen anti-HIV antikorları ile bağlı olmalıdır. Böylece makrofajlar üzerinde Fc reseptörlerini düzenlenmesi enfeksiyonu artıracaktır. HÜCREYE GİRİŞ: PH BAĞIMSIZ PLAZMA MEMBRANI İLE FÜZYON Viral zar proteininde pH değerine bağımlı olmayan
uyum değişikliği hücrenin enfekte olması için, viral membran ve hücre zarı
arasında füzyon gereklidir. Böylece, endozom veya lizozomlar içine giriş gerekli
değildir. TERS TRANSKRİPSİYON VE İNTEGRASYON Bu diğer retrovirüslere benzer. HIV, virüsü parçası olarak enfeksiyon esnasında ters transkriptaz kullanır. Nükleokapsid sitoplazmaya girer ve ters transkripsiyon nükleokapsit içinde gerçekleşir. Naif dinlenen T4 hücrelerinde, provirüs (DNA formu) olasılıkla çekirdek içine ön-uyum kompleksinin enerji bağımlı içeri alınması için gerekli ATP eksikliğinden sitoplazma içinde kalır. Çoğu virüs sadece bölünen hücrelerin çekirdeğin içinde replike olur ancak, hücre bölünmesi HIV replikasyonu için esas teşkil etmemektedir. Bunun nedeni: İki virüs proteininin (vpr GAG proteinlerden biri) nükleer lokalizasyon sinyalleri vardır ve böylece kromozomlarına viral DNA'nın nüfuz edebilmesi mitoz sırasında nükleer membran parçalanması gerekli değildir. İNTEGRASYON Soyulma ve çekirdeğe girdikten sonra, viral
DNA'nın hem doğrusal ve dairesel formları bulunur. Doğrusal çift iplikli viral
DNA, viral integraz proteini (pol geninden dönüştürülen) kullanılarak konak
hücre kromozomu içine yerleştirilir. İntegrasyondan sonra, viral RNA konak RNA
polimeraz II tarafından transkripte edilir.
|
|||||||
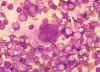 Şekil 18
Şekil 18HIV-1 enfeksiyonlu hastadan lenf düğümü kesitinden dokunun hazırlanmasında çok çekirdekli hücre (sinsityum). Büyük, çok çekirdekli hücre üreten hücre füzyonu, viral sitopatik etki HIV-1 ile enfeksiyonun karekteristiktir, ancak tanısal değil. Giemsa boyama. Lenfadenopati smear. CDC/Dr. Edwin P. Ewing, Jr. epe1@cdc.gov |
||||||||
|
Şekil
19
|
POLİPROTEİNLERİN OLUŞUMU VE BUNLARIN PARÇALANMASI Yeni bir virüsun birleşmesi konak hücre membranında gerçekleşir (Şekil 19). Proteinin üç tipi virionu oluşturur. Bu membran proteini kompleksi (gp120 ve gp41 - ilk olarak gp160'den türetilmiş) ve iki iç ön-madde proteini, Gag poliprotein ve gag/pol poliprotein (ikincisi gag geninden pol genin içine ribozoma gelen çeviri sürdürmesine izin veren bir çerçeve kayması sonucu oluşur) Proteinler hücre zarında bir araya gelir ve membranı çimdikler (şekil 19 ve 20). Daha büyük iç öncüsü (Gag-Pol) oluşmakta olan virionun içine pozitif iplikli RNA'nın iki ipliğini çeker ve proteaz (Gag-Pol proteinin parçası) serbest olan kendisini keser. Proteaz diğer enzimleri (ters transkriptaz, integraz ve daha proteaz) serbest bırakmak için Gag-Pol bölünmesini tamamlar. Ayrıca proteaz Gag-Pol kalan kısmını yapısal küçük Gag proteinlere parçalar. p24 zarın altında iken p24, p7 ve p6 mermi biçimli çekirdek oluşturur. Gag ve gag/pol füzyon proteinleri yaklaşık 20/1 oranında yapılmaktadır. Ayrılmış olmadıkça viral proteinler işlevsel bulunmadığından bu spesifik viral proteaz hayati önem taşımaktadır. Bu özellik, proteazı anti-HIV ilaçlarının inhibisyonu için iyi bir aday yapar (ek 3 ve anti-viral kemoterapiye bakınız). Gag/pol ve gag, kovalent olarak bağlanmış olan bir yağ asidi ile viral zara bağlıdır. Bölünmeler zara bağlı kalan p17 ile sonuçlanır. Gp160, endoplazmik retikulum ile birlikte bir tek iki ucu bağlı
mRNA'dan çevrilmiş olan ve bir kez membranı kapsayan bir entegral zar
proteinidir. Endoplazmik retikulumda, konak enzimi tarafından gp120 ve gp41'e
ayrıldığı ve farklı glikosile edildiği golgi cisimciğine nakledilmeden önce
glikosile edilir. Bu ekzositik yol üzerinden hücre membranına hareket eder. Gag
ve gag-pol proteinlerin aksine, gp 160 viral proteaz tarafından bölünemez.
|
|||||||
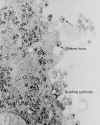 Şekil 20
Şekil 20Transmisyon elektron mikrografisi ile HIV-1’in tomucuklanması ve ayrılması CDC |
||||||||
|
||||||||
|
||||||||