|
x |
x |
|
 |
 |
|
BỆNH NHIỄM TRÙNG |
VI KHUẨN HỌC |
MIỄN DỊCH HỌC |
NẤM HỌC |
KÝ SINH TRÙNG HỌC |
VIRÚT HỌC |
|
ENGLISH
|
MIỄN DỊCH HỌC - CHƯƠNG BỐN
KHÁNG THỂ - CẤU TRÚC VÀ CHỨC NĂNG
Gene Mayer, Ph.D
Emertius Professor of Pathology, Microbiology and Immunology
University of South Carolina
Biên dịch: Nguyễn Văn Đô, MD., PhD.,
Bộ môn Sinh lý bệnh-Miễn dịch,
Trường Đại học Y Hà Nội,
Hà Nội, Việt Nam
|
|
TURKISH |
|
FRANCAIS |
|
PORTUGUES |
|
SHQIP |
Let us know what you think
FEEDBACK |
|
SEARCH |
|
|

 |
|
Logo image © Jeffrey
Nelson, Rush University, Chicago, Illinois and
The MicrobeLibrary |
| MỤC TIÊU
GIẢNG DẠY
Trình bày đặc điểm chung của kháng thể
Mô tả cấu trúc cơ bản của kháng thể
Trình bày mối liên quan giữa cấu trúc và chức năng của kháng thể
Xác định các vùng hằng định và vùng cực kỳ thay đổi của kháng thể
Xác định các lớp và dưới lớp kháng thể, các nhóm và dưới nhóm
Mô tả cấu trúc và đặc điểm của các lớp kháng thể
 Hình 1. Điện di protein huyết thanh
Hình 1. Điện di protein huyết thanh |
ĐỊNH NGHĨA
Kháng thể (Ig)
Kháng thể (KT) là các phân tử glycoprotein được sản xuất
bởi các tương bào trong một đáp ứng với chất sinh miễn dịch và có chức
năng như kháng thể. Tên của kháng thể xuất phát từ việc chúng di chuyển
cùng với các protein hình cầu, khi huyết thanh chứa kháng thể được đặt
trong một điện trường (Hình 1).
CHỨC NĂNG CHUNG CỦA KHÁNG THỂ
Kết hợp với kháng nguyên
Kháng thể kết hợp đặc hiệu với một hoặc vài kháng nguyên
(KN) gần giống nhau. Thực ra, mỗi kháng thể kết hợp với một quyết định
kháng nguyên đặc hiệu. Kháng thể kết hợp với kháng nguyên là chức năng
đầu tiên của các kháng thể và do đó cơ thể được bảo vệ. Hóa trị của
kháng thể dựa vào số quyết định kháng nguyên mà mỗi phân tử kháng thể có
thể kết hợp. Hóa trị của tất cả các kháng thể có ít nhất là hai và trong
một số trường hợp có nhiều hơn nữa.
Các chức năng hiệu ứng
Thông thường sự kết hợp của 1 KT với 1 KN không có hiệu
ứng sinh học. Dĩ nhiên, các hiệu ứng sinh học quan trọng là kết quả của
“chức năng hiệu ứng" thứ phát của các kháng thể. Kháng thể làm trung
gian của nhiều chức năng hiệu ứng này. Khả năng thực hiện một chức năng
hiệu ứng đặc biệt cần phải có KT kết hợp với KN kích thích sinh ra nó.
Không phải mọi kháng thể làm trung gian cho tất cả các chức năng hiệu
ứng. Các chức năng hiệu ứng này bao gồm:
-
Hoạt hóa bổ thể - Điều này
dẫn đến sự ly giải các tế bào và giải phóng các phân tử có hoạt
tính sinh học (xem chương hai).
-
Bám vào các loại tế bào khác nhau
- Các tế bào thực bào, lympho, tiểu cầu, các tế bào mast, và
bạch cầu ái kiềm có các thụ thể để kháng thể bám vào. Sự kết hợp
đó làm hoạt hóa các tế bào, thực hiện một số chức năng. Một số
kháng thể cũng liên kết với thụ thể trên bề mặt nguyên bào nuôi
của nhau thai, dẫn đến kháng thể được vận chuyển qua nhau thai.
Kết quả là, người mẹ cung cấp các kháng thể miễn dịch cho thai
nhi và trẻ sơ sinh.
|
|
TỪ KHÓA
Kháng thể
Hóa trị
Chuỗi nặng
Chuỗi nhẹ
Vùng thay đổi
Vùng hằng định
Vùng bản lề
Domain
Vùng siêu biến
Vùng khung
Nhóm và dưới nhóm
Fab & Fc, F(ab')2
loại và dưới loại
Lớp và dưới lớp
Opsonin
Chuỗi J
Thành phần tiết
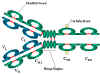 Hình 2A. Cấu trúc cơ bản của kháng thể
Hình 2A. Cấu trúc cơ bản của kháng thể
 Hình 2B. Bấm vào hình trên để xem hình ảnh động về cấu trúc của kháng
thể
Hình 2B. Bấm vào hình trên để xem hình ảnh động về cấu trúc của kháng
thể
Requires Chime Plug-In. Get Chime here. Developed by Eric Martz.
Development supported by the Division of Undergraduate Education of the
National Science Foundation.
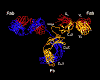 Hình 2C. Mô hình dạng dải của vị trí kết hợp kháng nguyên của kháng thể
(IgG2A).
Hình 2C. Mô hình dạng dải của vị trí kết hợp kháng nguyên của kháng thể
(IgG2A).
Harris, L. J., Larson, S. B., Hasel, K. W., Day, J., Greenwood, A.,
McPherson, A. Nature 1992, 360, 369-372. © 2000 Antibody Resource Page
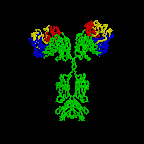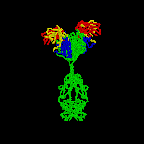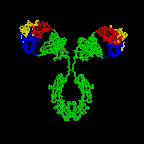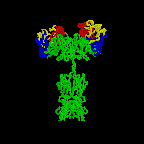 Hình 2D. Kháng thể xoay vòng
Hình 2D. Kháng thể xoay vòng
Jose Saldanha, Humanization by Design © 2000, Antibody Resource Page
|
CẤU TRÚC CƠ BẢN CỦA KHÁNG THỂ
Cấu trúc cơ bản của các kháng thể được minh
họa trong Hình 2. Mặc dù các kháng thể khác nhau có thể khác nhau về cấu
trúc, nhưng tất cả họ đều được cấu tạo từ các đơn vị cơ bản giống nhau.
Chuỗi nặng và
chuỗi nhẹ
Tất cả các kháng thể có một cấu trúc chuỗi bốn là
đơn vị cơ bản của chúng. Chúng được bao gồm hai chuỗi nhẹ giống hệt nhau
(23kD) và hai chuỗi nặng giống hệt nhau (50-70kD).
Cầu nối đisulfua
Cầu nối
disulfua liên chuỗi
Các chuỗi nặng và chuỗi nhẹ, và hai chuỗi nặng được liên kết với
nhau bằng các cầu nối disulfua liên chuỗi và bởi các tương tác không
cộng hóa trị. Số lượng các cầu disulfua liên chuỗi khác nhau tùy
thuộc vào loại kháng thể khác nhau.
Liên kết disulfua nội chuỗi
Trong mỗi chuỗi polypeptid cũng có cầu nối disulfua.
Vùng biến
đổi (V) và vùng hằng định (C)
Khi so sánh trình tự các acid amin của các chuỗi nặng và chuỗi nhẹ
khác nhau, người ta thấy cả hai chuỗi nặng và nhẹ có thể được chia
thành hai khu vực dựa trên sự biến đổi trong trình tự acid amin. Đó
là:
Chuỗi nhẹ - VL (110 acid amin) và
CL (110 cid amin)
Chuỗi nặng - VH (110 acid amin)
và CH (330-440 acid amin)
Vùng bản lề
Đây là khu vực mà các cánh tay của các phân tử kháng thể
hình thành một chữ Y. Nó được gọi là vùng bản lề vì có một sự linh hoạt
trong phân tử tại vị trí này.
Domain
Hình ảnh ba chiều của phân tử kháng thể cho thấy nó không
phải là thẳng như mô tả trong Hình 2A. Thay vào đó, nó được cuộn lại như
hình cầu mà mỗi hình cầu có một cầu nối disulfua nội chuỗi (Hình 2B-D).
Những vùng đó được gọi là domain.
Domain chuỗi nhẹ - VL và CL
Domain chuỗi nặng - VH, CH1 - CH3 (hoặc CH4)
Oligosaccharid
Carbohydrat được gắn vào domain CH2 của hầu hết các kháng thể. Tuy nhiên,
trong một số trường hợp carbohydrat cũng có thể được gắn tại các vị trí
khác.
CẤU TRÚC VÙNG THAY ĐỔI
Vùng siêu biến (HVR) hoặc vùng
kết hợp với kháng nguyên (CDR)
Khi so sánh trình tự các acid amin ở vùng
biến đổi của kháng thể cho thấy hầu hết các vị trí biến đổi tại ba vùng
gọi là vùng siêu biến nằm ở khu vực như minh họa trong Hình 3. Các kháng
thể có tính đặc hiệu khác khác nhau có vùng kết hợp kháng nguyên khác
nhau trong khi các kháng thể có cùng một tính đặc hiệu có vùng kết hợp
kháng nguyên giống hệt nhau (CDR là vị trí kết hợp của kháng thể). Vùng
kết hợp với kháng nguyên của kháng thể bao gồm cả chuỗi H và chuỗi L.
Vùng khung
Các vùng nằm giữa vùng kết hợp với kháng
nguyên trong vùng thay đổi được gọi là các vùng khung (Hình 3). Dựa trên
sự tương đồng và khác biệt trong vùng khung, vùng thay đổi của chuỗi
nặng và nhẹ của kháng thể có thể được chia thành các nhóm và phân nhóm.
Chúng được hình thành từ các sản phẩm của các gen khác nhau.
|
 Hình 3. Cấu trúc vùng thay đổi và hằng định
Hình 3. Cấu trúc vùng thay đổi và hằng định
|
CÁC
MẢNH KHÁNG THỂ KHÁC NHAU: MỐI LIÊN QUAN GIỮA
CẤU TRÚC VÀ CHỨC NĂNGCác mảnh kháng thể
được tạo ra do phân cắt protein là minh chứng quan trọng để giải thích
những mối liên quan giữa cấu trúc và chức năng của kháng thể.
Fab
Papain có thể cắt phân tử kháng thể tại khu vực
bản lề ở phía trước cầu nối disulfua liên chuỗi H-H (Hình 4). Kết
quả là tạo ra hai mảnh giống hệt nhau có chứa các chuỗi nhẹ và các
domain VH và CH1 của chuỗi nặng.
Kết hợp KN - Những mảnh đó được gọi là mảnh
Fab bởi vì chúng có các vị trí kết hợp với KN của KT. Mỗi mảnh
Fab có đơn hóa trị trong khi phân tử nguyên gốc là hóa trị hai.
Vị trí kết hợp kháng nguyên được hình thành bởi VH và VL. Một
kháng thể có khả năng kết hợp một quyết định kháng nguyên đặc
hiệu vì nó có một sự phối hợp đặc biệt của VH và VL. Sự kết hợp
khác nhau của VH và VL ở các kháng thể làm cho chúng có thể kết
hợp các quyết định kháng nguyên khác nhau.
Fc
Sau khi phân cắt kháng thể bằng papain cũng tạo ra
một mảnh có chứa phần còn lại của hai chuỗi nặng, mỗi chuỗi có chứa
một domain CH2 và một CH3. Đoạn này được gọi là Fc bởi vì nó được
kết tinh một cách dễ dàng.
|
 Hình 4. Các mảnh kháng thể: Liên quan giữa cấu trúc và chức năng
Hình 4. Các mảnh kháng thể: Liên quan giữa cấu trúc và chức năng |
Chức năng hiệu ứng - Các chức năng hiệu ứng của
kháng thể được thực hiện bởi phần Fc của phân tử. Các chức năng khác
nhau được thực hiện bởi các domain khác nhau trong mảnh này (hình
5). Thông thường, để thực hiện chức năng hiệu ứng của kháng thể nó
cần phải kết hợp với kháng nguyên, tuy nhiên, có những ngoại lệ cho
quy luật này.
|
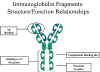 Hình 5.
Hình 5.
ác mảnh kháng thể: Mối quan hệ giữa cấu trúc và chức năng |
F(ab')2
Khi cắt kháng thể bằng pepsin, vị trí được cắt là ở chuỗi nặng, phía
sau cầu disulfua liên chuỗi tạo ra một mảnh có chứa cả hai vị trí
kết hợp kháng nguyên (hình 6). Đoạn này được gọi là F(ab’)2 vì nó có
hóa trị hai. Vùng Fc của phân tử kháng thể được phân cắt bởi pepsin
tạo thành các peptid nhỏ. Mảnh F(ab')2 kết hợp với kháng nguyên,
nhưng nó không còn chức năng hiệu ứng của kháng thể.ag
|
 Hình 6.
Hình 6.
Các mảnh kháng thể: Liên quan giữa cấu trúc và chức năng |
CÁC LỚP KHÁNG THỂ, PHÂN LỚP, NHÓM VÀ PHÂN
NHÓM
Các lớp kháng thể
Các kháng thể có thể được chia thành năm lớp khác nhau,
dựa vào sự khác biệt trình tự acid amin trong vùng hằng định của các
chuỗi nặng. Tất cả các kháng thể trong một lớp nhất định sẽ có vùng hằng
định chuỗi nặng rất giống nhau. Các khác biệt này có thể được phát hiện
bởi các nghiên cứu trình tự hoặc phổ biến hơn bằng huyết thanh học (tức
là sử dụng các kháng thể để tìm những khác biệt này).
- IgG - chuỗi nặng Gamma
- IgM - chuỗi nặng Muy
- IgA - chuỗi nặng Alpha
- IgD - chuỗi nặng Delta
- IgE - chuỗi nặng Epsilon
Dưới lớp kháng thể
Các lớp kháng thể có thể chia thành dưới lớp dựa
trên sự khác biệt nhỏ trong trình tự acid amin trong vùng hằng định
của chuỗi nặng. Tất cả các kháng thể trong một phân lớp sẽ có trình
tự acid amin vùng hằng định chuỗi nặng rất giống nhau. Một lần nữa
những khác biệt này được phát hiện một cách phổ biến nhất bằng
phương pháp huyết thanh học.
- Dưới lớp IgG
- IgG1 – Chuỗi nặng Gamma 1
- IgG2 - Chuỗi nặng Gamma 2
- IgG4 - Chuỗi nặng Gamma 4
- IgG3 - Chuỗi nặng Gamma 3
- Dưới lớp IgA
- IgA1 - Chuỗi nặng Alpha 1
- IgA2 - Chuỗi nặng Alpha 2
|
| |
Các nhóm kháng thể
Kháng thể cũng có thể được phân loại theo
loại chuỗi nhẹ mà kháng thể đó có. Các loại chuỗi nhẹ dựa trên sự khác biệt
ở trình tự acid amin trong vùng hằng định của chuỗi nhẹ. Các khác biệt này
được phát hiện bằng phương pháp huyết thanh học.
Chuỗi nhẹ Kappa
Chuỗi nhẹ Lambda
Dưới nhóm kháng thể
Các chuỗi nhẹ cũng có thể được chia thành các
phân nhóm dựa trên sự khác biệt ở trình tự acid amin trong vùng hằng định
của chuỗi nhẹ.
Phân nhóm Lambda
-
Lambda 1
-
Lambda 2
-
Lambda 3
-
Lambda 4
Danh pháp
Kháng thể được đặt tên dựa trên lớp, hoặc
dưới lớp của chuỗi nặng và nhóm hoặc dưới nhóm của chuỗi nhẹ. Trừ khi nó
được ghi chính xác, bạn nên biết rằng tất cả các phân lớp, nhóm, dưới nhóm
đều có. IgG có tất cả các dưới lớp và dưới nhóm.
Tính không đồng nhất
Kháng thể được coi là một tập hợp các phân tử
thường rất không đồng nhất, vì chúng được hình thành từ các lớp khác nhau và
dưới lớp khác nhau. Mỗi lớp hoặc dưới lớp đều có các nhóm và dưới nhóm của
các chuỗi nhẹ. Ngoài ra, các phân tử kháng thể khác nhau có các đặc tính kết
hợp kháng nguyên khác nhau vì chúng có các vùng VH và VL khác nhau.
|
 Hình
7 Hình
7
Cấu trúc IgG |
CẤU TRÚC VÀ MỘT SỐ ĐẶC ĐIỂM CỦA
CÁC LỚP VÀ DƯỚI LỚP CỦA KHÁNG THỂ
IgG
Cấu trúc
Các cấu trúc của dưới lớp IgG được trình bày trong Hình 7. Tất
cả các IgG ở dạng mono (kháng thể 7S). Các dưới lớp có sự khác
nhau ở số lượng cầu disulfua và độ dài của vùng bản lề.
Đặc điểm
IgG là kháng thể đa năng nhất bởi vì nó có khả năng thực hiện
tất cả các chức năng của kháng thể
-
IgG là kháng thể có
nhiều nhất trong huyết thanh - 75% kháng thể của huyết
thanh là IgG
-
IgG là kháng thể
chủ yếu ở xung quanh mạch máu
-
Chuyển qua nhau
thai - IgG là lớp kháng thể duy nhất đi qua được nhau
thai. Sự vận chuyển này nhờ một thụ thể với vùng Fc của
IgG trên các tế bào nhau thai. Không phải tất cả dưới
lớp IgG đi qua nhau thai tốt như nhau; IgG2 đi qua nhau
thai không tốt.
-
Hoạt hóa bổ thể -
Không phải tất cả các dưới lớp IgG có thể hoạt hóa bổ
thể tốt như nhau; IgG4 không hoạt hóa bổ thể.
-
Gắn lên các tế bào
- Các đại thực bào, tế bào mono, PMNs và một số lympho
có các thụ thể Fc cho vùng Fc của IgG. Không phải tất cả
các dưới lớp của IgG gắn lên tế bào tốt như nhau; IgG2
và IgG4 không gắn vào các thụ thể Fc. Kết quả của sự kết
hợp của các dưới lớp kháng thể với các thụ thể Fc trên
PMNs, tế bào mono và các đại thực bào làm cho các tế bào
có thể tiêu diệt kháng nguyên tốt hơn. Các kháng thể đã
gắn vào kháng nguyên sẽ được các tế bào này bắt và tiêu
diệt. Từ “opsonin” được dùng để miêu tả những chất làm
tăng cường sự thực bào. IgG là một chất opsonin tốt.
Liên kết của IgG vào thụ thể Fc trên các loại tế bào
khác sẽ hoạt hóa các chức năng khác.ll
|
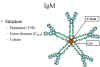 Hình 8
Hình 8
Cấc trúc IgM dạng pentamer trong huyế t thanh
 Hình 9
Hình 9
Cấu trúc IgM bề mặt tế bào
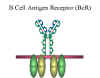 Hình 10
Hình 10
Thụ thể tế bào B (BcR) |
IgM
Cấu trúc
Cấu trúc của IgM được trình bày trong Hình
8. IgM thường tồn tại dưới dạng pentamer (kháng thể 19S), nhưng
nó cũng có thể tồn tại ở dạng monomer. Trong dạng pentamer, tất
cả các chuỗi nặng và chuỗi nhẹ giống hệt nhau. Như vậy, hóa trị
trên lý thuyết là 10. IgM có một domain phụ trên chuỗi muy (CH4)
và nó có một protein đồng hóa trị liên kết thông qua một cầu nối
disulfua được gọi là J. Chuỗi này có chức năng là liên kết các
chuỗi dạng monomer tạo thành dạng pentamer.
Đặc điểm
- Kháng thể IgM có hàm lượng xếp thứ 3
trong huyết thanh.
- IgM là kháng thể đầu tiên được sản
xuất ở bào thai và là kháng thể đầu tiên được sản xuất bởi
dòng tế bào B trinh tiết sau khi được kích thích bởi kháng
nguyên.
- Với cấu trúc pentamer, IgM là một
kháng thể hoạt hóa bổ thể tốt. Do đó, kháng thể IgM rất có
hiệu quả để ly giải các vi sinh vật
- Với đặc điểm cấu trúc như vậy, IgM
cũng là một kháng thể ngưng kết tốt. Vì thế, kháng thể IgM
rất tốt cho kết tụ vi sinh vật để cuối cùng loại bỏ chúng
khỏi cơ thể
- IgM gắn vào một số tế bào thông qua
thụ thể Fc
- Là kháng thể bề mặt tế bào lympho B
IgM bề mặt tế bào tồn tại ở dạng
monomer và không có chuỗi J nhưng nó có thêm 20 acid
amin ở đầu cacboxy để giữ chặt nó vào trong màng tế bào
(Hình 9). IgM bề mặt tế bào có chức năng là thụ thể cho
kháng nguyên trên tế bào B. IgM bề mặt liên kết không
đồng hóa trị với hai loại protein khác trên màng tế bào
B được gọi là Ig-alpha và Ig-beta được thể hiện trong
Hình 10. Những protein này đóng vai trò là phân tử tín
hiệu từ sau phần đuôi trong bào tương của phân tử kháng
thể, vì phần đuôi của kháng thể quá ngắn để truyền một
tín hiệu. Trước khi tín hiệu có thể được truyền bởi các
chuỗi Ig-alpha và Ig-beta cần phải có sự kết hợp gữa
kháng nguyên và kháng thể trên bề mặt tế bào. Trong
trường hợp kháng nguyên không phụ thuộc T, sự kết hợp
giữa các kháng nguyên và kháng thể bề mặt là đủ để hoạt
hóa các tế bào B biệt hóa thành các tế bào tương bào
tiết ra kháng thể. Tuy nhiên, đối với kháng nguyên phụ
thuộc T, cần phải có một tín hiệu thứ hai được cung cấp
bởi các tế bào lympho T hỗ trợ trước khi các tế bào B
được hoạt hóa.
|
 Hình
11 Hình
11
Cấu trúc IgA
 Hình
12 Hình
12
Nguyên bản của IgA hòa tan |
IgA
Cấu trúc
IgA huyết thanh ở dạng monomer nhưng IgA trong
dịch tiết lại có dạng dimer được trình bày trong Hình 11. Khi IgA ở
dạng dimer, có một chuỗi J sẽ liên kết hai monomer.
IgA trong dịch tiết cũng có một protein liên kết với nó được gọi là
các mảnh tiết hoặc mảnh T; sIgA đôi khi được gọi là kháng thể 11s.
Không giống như IgA, phân tử được sản xuất trong tế bào plasma, các
mảnh tiết được sản xuất bởi các tế bào biểu mô và được gắn thêm vào
IgA khi nó được chuyển vào dịch tiết (Hình 12). Các mảnh tiết giúp
IgA vận chuyển được qua niêm mạc và cũng bảo vệ nó khỏi bị thoái hóa
trong dịch tiết.
Đặc điểm
- IgA là kháng thể phổ biến thứ 2 trong huyết
thanh.
- IgA là lớp kháng thể chính có mặt trong
dịch tiết - nước mắt, nước bọt, sữa non, chất nhầy. Kể từ khi nó
được tìm thấy trong dịch tiết, IgA rất quan trọng trong miễn
dịch tại chỗ (màng nhầy).
- Thông thường IgA không cố định bổ thể,
trừ khi vón tụ.
- IgA có thể liên kết với một số tế bào
như bạch cầu đa nhân và một số lympho bào.gur
|
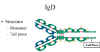 Hình 13
Hình 13
Cấu trúc IgD |
IgD
Cấu trúc
Cấu trúc của IgD được trình bày trong
Hình 13. IgD chỉ tồn tại ở dạng monomer.
Đặc điểm
-
IgD được tìm thấy trong
huyết thanh ở mức độ thấp; vai trò của nó trong huyết thanh chưa
được biết rõ.
-
IgD chủ yếu được tìm thấy
trên bề mặt tế bào B, nơi nó có chức năng như một thụ thể cho
các kháng nguyên. IgD trên bề mặt của tế bào B có thêm các acid
amin tại đầu cacboxy để giữ chặt vào màng. Nó cũng liên kết với
chuỗi Ig-alpha và Ig-beta.
-
IgD không hoạt hóa bổ thể.
|
 Hình 14
Hình 14
Cấu trúc IgE |
IgE
Cấu trúc
Cấu trúc của IgE được trình bày trong
Hình 14. IgE tồn tại ở dạng monomer và có thêm một domain trong vùng
hằng định.
Chức năng
-
IgE là kháng thế có ít nhất
trong huyết thanh vì nó gắn rất chặt với các thụ thể Fc trên
màng bạch cầu ái kiềm và các tế bào mast ngay cả trước khi tương
tác với kháng nguyên.
-
Tham gia các phản ứng dị
ứng - là kết quả của việc gắn vào bạch cầu ái kiềm, IgE có liên
quan đến phản ứng dị ứng. Sự kết hợp của chất gây dị ứng với IgE
trên tế bào dẫn đến giải phóng một loạt các chất hóa học trung
gian gây ra các triệu chứng dị ứng.
-
IgE có vai trò trong các
bệnh do ký sinh trùng. Vì IgE tăng trong các bệnh lý nhiễm ký
sinh trùng, nên định lượng IgE trong huyết thanh là hữu ích để
chẩn đoán nhiễm ký sinh trùng. Bạch cầu ái toan có thụ thể Fc
dành cho IgE và chúng tấn công giun sán đã được gắn IgE nó có
thể giết chết ký sinh trùng.
-
IgE không hoạt hóa bổ thể.
|
 Hình 15
Hình 15
Kháng thể xoay vòng.
© 2000 Antibody Resource Page
Antibody Concepts
|
NHỮNG ỨNG DỤNG LÂM SÀNG CỦA CÁC LỚP KHÁNG THỂ
Adapted from:F.T. Fischbach in "A Manual of Laboratory
Diagnostic Tests," 2nd Ed., J.B. Lippincott Co., Philadelphia, PA
IgG
Tăng trong:
- Nhiễm trùng tạo u hạt mãn tính
- Tất cả các loại nhiễm trùng
- Tăng mẫn cảm
- Bệnh gan
- Suy dinh dưỡng (nặng)
- Rối loạn protein máu
- Bệnh liên kết với bệnh u hạt do quá mẫn cảm,
rối loạn da liễu, và đa u tủy IgG
- Viêm khớp dạng thấp
Giảm trong:
- Bệnh không có kháng thể
- Bất sản lympho
- Giảm IgG, IgA chọn lọc
- Đa u tủy IgA
- Thiếu protein Bence Jones
- Ung thư bạch cầu mạn tính (CLL)
IgM
Tăng (ở người lớn) trong:
- Ung thư lympho Waldenström
- Bệnh do ký sinh trùng
(trypanosomiasis)
- Nấm (Actinomycosis)
- Bệnh Carrión (bartonellosis)
- Bệnh sốt rét
- Bệnh bạch cầu đơn nhân nhiễm
khuẩn
- Lupus ban đỏ
- Viêm khớp dạng thấp
o Rối loạn gammaglogolin máu (một số trường hợp)
Lưu ý: Ở trẻ sơ sinh, lượng IgM cao hơn 20 ng/dl là một
dấu hiệu của sự kích thích miễn dịch ở tử cung bởi virút
rubella, CMV, giang mai, hoặc nhiễm ký sinh trùng (toxoplasma).
Giảm trong:
- Bệnh không có kháng thể
- Rối loạn phát triển lympho
(một số trường hợp)
- Bất sản lympho
- Đa u tủy IgG và IgA
(myeloma)
- Rối loạn gammaglobulin máu
- Bệnh ung thư bạch cầu mãn
tính (CLL)
IgA
Tăng trong:
- Wiskott-Aldrich
syndrome
- Cirrhosis of the
liver (most cases)
- Certain stages of
collagen and other autoimmune disorders such
as rheumatoid arthritis and lupus
erythematosus
- Chronic infections
not based on immunologic deficiencies
- IgA myeloma
- Hội chứng
Wiskott-Aldrich
- Xơ gan của gan (phần
lớn trường hợp)
- giai đoạn nhất định
của collagen và các rối loạn tự miễn khác
như viêm khớp dạng thấp và luput ban đỏ hệ
thống
- nhiễm trùng mãn
tính không dựa trên sự thiếu hụt miễn dịch
- Đa u tủy IgA
Giảm trong:
- Thất điều giãn
mạch
- Các trạng thái
thiếu hụt miễn dịch (ví dụ, suy giảm
miễn dịch, không có kháng thể bẩm sinh
và mắc phải, và thiểu năng kháng thể)
- Hội chứng kém
hấp thu
- Bất sản lympho
- Đa u tủy IgA
- lymphoblastic
bệnh bạch cầu
- Đa u tủy IgG
- Bệnh ung thư
bạch cầu cấp tính
- Bệnh ung thư
bạch cầu mãn tính
IgD
Tăng
trong:
- Nhiễm
trùng mãn tính
- Đa u
tủy IgD
IgE
Tăng trong:
- Bệnh
da dị ứng
- Sốt
mùa
- Hen
phế quản
- Sốc
phản vệ
- Đa
u tủy IgE
Giảm trong:
-
Không kháng thể bẩm
sinh
- Suy
giảm kháng thể do
chuyển hóa hoặc do
tổng hợp kháng thể
|
|

 |
 Trở về phần Miễn dịch của Vi khuẩn học và Miễn dịch học
online
Trở về phần Miễn dịch của Vi khuẩn học và Miễn dịch học
online
This page last changed on
Sunday, August 20, 2017
Page maintained by
Richard Hunt
|

 Hình 3. Cấu trúc vùng thay đổi và hằng định
Hình 3. Cấu trúc vùng thay đổi và hằng định
 Hình 4. Các mảnh kháng thể: Liên quan giữa cấu trúc và chức năng
Hình 4. Các mảnh kháng thể: Liên quan giữa cấu trúc và chức năng Hình 5.
Hình 5.  Hình 6.
Hình 6.  Hình
7
Hình
7 Hình 8
Hình 8 Hình
11
Hình
11 Hình 13
Hình 13 Hình 14
Hình 14 Hình 15
Hình 15


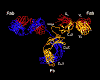
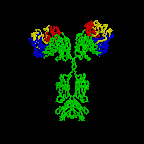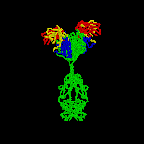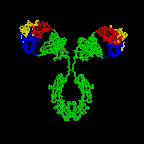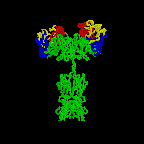 Hình 2D. Kháng thể xoay vòng
Hình 2D. Kháng thể xoay vòng

