|
x |
x |
|
 |
 |
|
INFECTIOUS
DISEASE |
BAKTERIYOLOJİ |
İMMÜNOLOJİ |
MYCOLOGY |
PARASITOLOGY |
VIROLOGY |
|
|
İMMÜNOLOJİ - BÖLÜM ONİKİ
HÜCRESEL İMMÜNİTE
Spesifik immün yanıtta hücre
– hücre etkileşimleri
Dr Gene Mayer
Professor
Department of Pathology, Microbiology and Immunology
University of South Carolina School of Medicine
ve
Dr Jennifer Nyland
Assistant Professor
Department of Pathology, Microbiology and Immunology
University of South Carolina School of Medicine
Çeviri:
Doç. Dr. Erkan Yula
İzmir, Katip Çelebi Üniversitesi, Tıp Fakültesi, Tıbbi Mikrobiyoloji
Anabilim Dalı
|
|
ENGLISH |
|
FRANCAIS |
|
PORTUGUES |
|
Let us know what you think
FEEDBACK |
|
SEARCH |
|
|
|

 |
|
Logo image © Jeffrey
Nelson, Rush University, Chicago, Illinois and
The MicrobeLibrary |
|
|
|
Edited and
illustrated by Dr Richard Hunt
|
|
|
|
ÖĞRENİM HEDEFLERİ
İmmün yanıtta Th hücrelerinin temel rolünü tartışmak
hücre-hücre etkileşimlerini (i) T-bağımlı antijenlere karşı antikor
yanıtta, (ii) sitotoksik T hücrelerin oluşumunda ve (iii) makrofajlarla
NK hücrelerinin aktivasyonunda açıklamak
Sitotoksik T hücreleri ve NK hücreleri tarafından öldürülme
mekanizmalarını tartışmak
T-bağımsız antijenlere karşı yanıtı tartışmak
|
İMMÜN YANITTA Th
HÜCRELERİNİN TEMEL ROLÜ Şekil 1’de gösterildiği üzere, antijen sunan hücre (ASH) tarafından sunulan
spesifik antijeni Th hücreleri tanıdıktan sonra birçok anahtar immün süreci
başlatabilir.
Bunlar:
-
Uygun efektör mekanizmaların seçimi (ör: B hücre
aktivasyonu veya Tc oluşumu)
-
Uygun efektör hücrelerin çoğalmasının
uyarılması ve
-
Diğer hücrelerin (ör: granülositler, makrofajlar, NK hücreleri)
fonksiyonel aktivitelerinin arttırılması
Th hücrelerinin dört alt popülasyonu bulunmaktadır: Th0, Th1, Th2 ve Th17
hücreleri. Naif Th0 hücreleri sekonderlenfoid dokularda antijenle
karşılaştığında ürettikleri sitokine göre farklılık gösteren inflamatuar Th1
hücrelerine, yardımcı Th2 hücrelerine veya patojenik T17 hücrelerine
farklılaşabilirler (Şekil 2). Th0 hücrelerinin Th1, Th2 veya T17 hücre haline
gelmesi antijen tarafından tetiklenen çevredeki sitokinlere bağlı olarak
değişmektedir. Örneğin, bazı antijenler Th2 hücrelerinin oluşmasını sağlayan
IL-4 üretimini uyarırken diğer antijenler Th1 hücrelerinin oluşmasını sağlayan
IL-12 üretimini uyarır. Şekil 3’te Th1 ve Th2 hücreleri için gösterildiği üzere,
Th1, Th2 ve Th17 hücreleri farklı hücreleri ve immün yanıt tipini etkiler.
Th1 hücreleri tarafından üretilen sitokinler makrofajları aktive eder ve
sitotoksik lenfositlerin (CTL) oluşumunda yer alırlar ve bu hücre-aracılı immün
yanıtla sonuçlanır. Buna karşın, Th2 hücreleri tarafından üretilen sitokinler B
hücrelerinin aktive olmasına yardım eder, bu antikor üretimiyle sonuçlanır.
Son yıllarda yapılan bir çalışmada, Th17 hücreleri (IL-17 üretmeleriyle
belirlenmiş) IL-1, IL-6 ve IL-23’e yanıt olarak farklılaşır (insanlarda).TGF-β
farelerde Th17 farklılaşması için önemlidir ancak insanlarda değildir. IL-17
multiple skleroz, inflamatuar bağırsak hastalığı ve romatoid artriti kapsayan
bazı otoimmün hastalıkların şiddetini arttırır. Aynı şekilde önemli olarak her
bir alt popülasyon diğeri üzerinde inibitör etki gösterebilir. Th1 hücreleri
tarafından üretilen IFN-γ, Th2 hücrelerinin çoğalmasını ve Th17 hücreleinin
farklılaşmasını inhibe eder ve Th2 hücreleri tarafından üretilen IL-10, Th1
hücrelerinin IFN-γ üretmesini inhibe eder. Ayrıca, gösterilmemesine rağmen IL-4,
Th1 hücrelerinin üretimini ve Th17 hücrelerinin farklılaşmasını inhibe eder. Bu
yüzden, immün yanıt, karşılaşılan patojen için gerekli olan yanıtını tehditin
tipine göre değişiklik göstermektedir örneğin hücre içi patojenler için hücre
aracılı yanıt ve hücre dışı patojenler için antikor yanıtı gibi.
|
|
ANAHTAR KELİMELER
Th1 hücreleri, Th2 hücreleri, Hapten-taşıyıcı model, CD28, B7, CD40,
CD40 ligand, CD5, B1 hücreleri, B2 hücreleri, CTL, Fas ligand, Perforin,
granzimler, kaspazlar, IFN-γ, aktivasyon
|
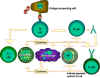 Şekil 1
Şekil 1
Th hücreleri hücre aracılı immünitenin merkezindedir. Antijen sunan hücreler
antijeni yadımcı T hücrelerine (Th) sunar. Th hücreleri hedef epitop olarak
seçilen spesifik epitopları tanır. Uygun efektör mekanizmalar belirlenir.
Örneğin, Th hücreleri B hücrelerinin anitkor üretmesine yardımcı olur ve
aynı zamanda diğer hücreleri de aktive eder. Th hücreleri tarafından
üretilen aktivasyon sinyalleri sitokinlerdir (lenfokinler) ancak benzer
sitokinler makrofajlar ve bu proseste yer alan diğer hücreler tarafından da
üretilirler.
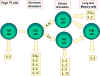 Şekil 2
Şekil 2
Fare Th hücrelerinin farklılaşması. Fare Th hücreleri farklı lenfokinleri
sentezleyen alt gruplara farklılaşır. Bu aynı zamanda insanlarda da
gerçekleşir.
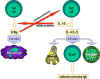 Şekil 3
Şekil 3
Efektör mekanizmaların Th1 ve Th2 hücreleri tarafından seçilimi. Ek olarak,
lenfokin üretiminine göre Lenfokin üretimlerinin hassasiyetiyle çeşitli
efektör yolakların belirlenmesine ek olarak Th1 hücreleri Th2 hücrelerini
durdurabilir veya tam tersi olabilir
|
|
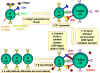 Şekil 4
Şekil 4
B ve Th hücrelerinin etkileşiminde rol alan moleküller. Antijen  B
hücreleri tarafından işlenir. Kostimülatörler eksprese edilir. İşlenmiş
olan antijen peptit B
hücreleri tarafından işlenir. Kostimülatörler eksprese edilir. İşlenmiş
olan antijen peptit  MHC
sınıf II antijenleriyle etkileşerek sunulur. T hücre MHC antijeniyle
birlikte olan peptiti ve kostimülatörleri tanır. T hücre, CD40 ligandını
eksprese eder. CD40 ligandı B hücresinin üzerindeki CD40 antijenine
bağlanır ve B hücreleri bölünür ve farklılaşır. B hücreleri tarafından
antikorlar üretilir. MHC
sınıf II antijenleriyle etkileşerek sunulur. T hücre MHC antijeniyle
birlikte olan peptiti ve kostimülatörleri tanır. T hücre, CD40 ligandını
eksprese eder. CD40 ligandı B hücresinin üzerindeki CD40 antijenine
bağlanır ve B hücreleri bölünür ve farklılaşır. B hücreleri tarafından
antikorlar üretilir.
 Şekil 5
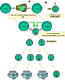
Şekil 5
Cooperation of cells in the immune responseİmmün yanıtta
hücrelerin işbirliği
Antigen-presenting cells (e.g. dendritic cells) present processed
antigen to virgin T cells, thereby priming them. Antijen sunan hücreler
(ör: dendritik hücreler) işlenmiş olan antijeni naif T hücrelerine sunar
ve onları hazırlar. B cells also process the antigen and present it to
the T cells. B hücreleri aynı zamanda antijeni işler ve bunları T
hücrelerine sunar. They then receive signals from the T cells that cause
them to divide and differentiate. T hücreleri kendilerinin bölünmesine
ve farklılaşmasına neden olacak sinyaller alırlar. Some B cells form
antibody-forming cells while a few form B memory cellsBazı B hücreleri
anitkor oluşturan hücrelere dönüşürken bazıları bellek B hücrelerini
oluşturur.
|
EKZOJEN T-BAĞIMLI ANTİJENLERİNE
KARŞI ANTİKOR YANITTAKİ HÜCRE-HÜCRE ETKİLEŞİMLERİ
Hapten-Taşıyıcı Model
Tarihsel olarak en önemli buluşlardan bir tanesi kompleks
bir proteine karşı antikor üretimi için hem T hem de B hücrelerine ihtiyaç
duyulduğudur. Bu prosesi anlamamıza yardımcı olan en önemli katkı anti-hapten
antikorlarının oluşumuna ilişkin olarak yapılmış çalışmalarla sağlanmıştır.
Hapten-taşıyıcı konjugatlarla yapılan çalışmalar şunları ortaya koymuştur:
-
Th2 hücreleri taşıyıcı determinantları tanır ve B
hücreleri haptenik determinantları tanır.
-
Hapten-spesifik B hücreleri ve taşıyıcı-spesifik Th
hücreleri arasındaki etkileşimler self MHC sınırılıdır.
-
B hücreleri hem antijen tanınmasında hem de antijen
sunumunda rol oynayabilirler.
B hücreleri immün yanıtta tek bir pozisyonda yer alır çünkü yüzeylerinde
immünoglobulin ve sınıf II MHC moleküllerini eksprese ederler. Bu yüzden de
immünoglobulin reseptörlerininki gibi aynı spesifiteye sahip antikor
üretebilirler; Ayrıca, antijen sunan hücre olarak da rol oynarlar.
Hapten-taşıyıcı konjugat modeli bakımından mekanizma şu şekilde
düşünülmektedir: Hapten immünoglobulin reseptörü tarafından tanınır,
hapten-taşıyıcı B hücresinin içine taşınır, işlenir ve taşıyıcı proteinlerin
peptit fragmentleri yardımcı T hücresine sunulur. T hücresinin aktivasyonu,
çözünebilir anti-hapten antikorlarını üretmesi için B hücrelerinin aktif
hale gelmesini sağlayan sitokin üretimiyle sonuçlanır. Şekil 4, B hücre-T
hücre etkileşimlerini özetlemektedir.
Th2 hücre-B hücre etkileşimi modelinde B hücrelerine taşınan
çoklu sinyallerin bulunduğuna dikkat edilmelidir. Sinyalin peptit-MHC
molekülünün TCR tarafından tanınmasıyla oluştuğu T hücre aktivasyonu
olaylarındaki prosesler B hücreleri için de geçerlidir. Bir antijenin
immünoglobulin reseptörüne bağlanması B hücresine bir sinyal gönderir ancak
bu yetersizdir. Kositmülatör moleküller tarafından gönderilen ikinci
sinyallere ihtiyaç duyulmaktadır; Bunların en önemlisi ikinci sinyalin
gönderilmesini başlatmak için B hücre üzerindeki CD40 molekülüne bağlanan T
hücre üzerindeki CD40L’dir.
Primer antikor cevabında hücre-hücre
etkileşimleri
B hücreleri primer antikor yanıtında en iyi antijen sunan
hücre değildir; dendritik hücreler veya makrofajlar daha etkilidir. Bununla
beraber bazı minör modifikasyonlarla birlikte yukarıda bahsedilmiş olan
hücre-hücre etkileşimlerinden hapten-taşıyıcı modeli aynı zamanda primer
antikor yanıttaki etkileşimlere de uygundur (Şekil 5). Primer yanıtta, ilk
olarak Th2 hücresi dendiritik hücreler veya makrofajlar tarafından sunulan
antijenle karşılaşır.. “Hazırlanmış” olan Th2 hücresi daha sonra antijenle
karşılaşmış ve antijenik peptitleri sınıf II MHC molekülleriyle birlikte
sunmuş olan B hücreleriyle etkileşime girer. B hücreleri hala daha
aktivasyon için iki sinyale ihtiyaç duyar – bir tanesi antijenin yüzey
immünoglobulinine bağlanmasıdır ve diğeri de Th2/B hücre-hücre etkileşimi
esnasında CD40/CD40 ligand birleşmesidir. Ayrıca, Th2 hücreleri tarafından
üretilen sitokinler B hücrelerinin çoğalmasına ve antikor salgılayan plazma
hücrelerine dönüşmesine yardımcı olur.
Sekonder antikor cevabında hücre-hücre
etkileşimleri
Primer yanıtın sounucunda birçok bellek T ve B hücresi
üretilir. BellekB hücrelerinin yüksek afiniteli immünoglobulin reseptörleri
(afinite olgunlaşmasına bağlı olarak) bulunur ki, bunlar B hücrelerinin
makrofajların veya dendritik hücrelerin gerek duyduğundan çok daha az
konsantrasyondaki antijene bağlanmasını ve bu antijeni sunmasını sağlar.
Ayrıca, bellek T hücreleri naif T hücrelerinden çok daha kolay aktive
olurlar. Bu yüzden B/Th hücre etkileşimleri sekonder antikor yanıtı
oluşturmak için yeterlidir. BellekTh hücrelerinin dentrik hücreler veya
makofajlar tarafından sunulan antijenle “hazırlanmasına” gerek yoktur (oluşabilmesine
rağmen).
Sitokinler ve sınıf değişimi
Aktive edilmiş Th2 hücreleri tarafından üretilen sitokinler
sadece B hücrelerinin çoğalmasını ve farklılaşmasını uyarmaz, aynı zamanda
üretilecek olan antikor sınıfının da regüle edilmesine yardımcı olur. Farklı
sitokinler farklı fonksiyonlara sahip antikorların farklı
sınıflandırılmasını uyarır. Bu şekilde antikor cevabı, karşılaşılan patojene
uygun hale getirilmiş olur (Ör: IgE antikorları parazitik enfeksiyonlar
içindir). Tablo 1’de çeşitli sitokinlerin üretilen antikorun sınıfı
üzerindeki etkilerini gösterilmektedir.
|
Sitokin
|
IgG1
|
IgG2a
|
IgG2b
|
IgG3
|
IgA
|
IgE
|
IgM
|
|
IL-4
|
Uyarır
|
İnhibe eder
|
|
İnhibe eder
|
|
Uyarır
|
İnhibe eder
|
|
IL-5
|
|
|
|
|
Augment
production
|
|
|
|
IFN-gamma
|
İnhibe eder
|
Uyarır
|
|
Uyarır
|
|
İnhibe eder
|
İnhibe eder
|
|
TGF-beta
|
|
|
Uyarır
|
İnhibe eder
|
Uyarır
|
|
İnhibe eder
|
|
Fare T hücre sitokinleriyle izotip
regülasyonu
Berlirli sitokinler belirli antikor izotiplerinin üretimini ya uyarır (yeşil)
ya da inhibe eder (pembe). İnhibisyon çoğunlukla farklı izotipe dönüşüm
inhibisyonu sonucudur.
|
|
Tablo 1 |
|
| |
EKZOJEN T-BAĞIMSIZ
ANTİJENLERE KARŞI ANTİKOR YANITTA HÜCRE-HÜCRE ETKİLEŞİMLERİ
T-bağımsız antijenlere karşı antikor yanıt
hücre-hücre arası etkileşimlere gerek duymaz. Bu antijenlerin polimerik doğası,
B hücreleri üzerindeki reseptörlerine antijenin çapraz bağlanmasını sağlar ve B
hücrelerinin aktivasyonuyla sonuçlanır. Herhangi bir sekonder yanıt, afinite
olgunlaşması veya sınıf değişimi oluşmaz. T-bağımsız antijenlere karşı gelişen
yanıtlar CD5+ B hücreleri (aynı zamanda B1 hücreleri de denir) adı verilen CD5-
(aynı zamanda B2 hücreleri denir) olan konvansiyonel B hücrelerinden farklı olan
B hücre alt grubunun aktivasyonuna ile olmaktadır.
CD5+ (B1) hücreleri
CD5+ hücreleri ontogenezde görülen ilk
B hücreleridir. Yüzey IgM eksprese ederler ancak çok az IgD eksperese eder
veya hiç IgD eksprese etmeyebilirler ve ilk olarak IgM antikorlarını en az
somatik olarak mutasyon geçirmiş germ hattı hücrelerinden üretirler. Bu
hücreler tarafından üretilen antikorlar düşük afinitelidir ve genellikle
polireaktiftirler (birçok antijene bağlanırlar). Serumdaki IgM’nin en çoğu
CD5+ B hücrelerden oluşur. CD5+ B hücreleri hafıza hücrelerini oluşturmaz.
Bu hücrelerin önemli bir özelliği kemik iliğinden yenisi ile değişmek
zorunda olan konvansiyonel B hücrelerinin aksine kendilerini
yenileyebilmeleridir. CD5+ B hücreler periferal polisakkaridler olan birçok
bakteriyel patojene karşı temel savunmayı oluştururlar. Bu hücrelerin
immünitedeki önemleri T hücre defekti olan kişilerde birçok bakteriyel
patojene direncin olmasıyla gösterilmiştir.
|
 Şekil 6
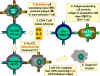
Şekil 6
CTL hücreleri antijene yanıt
olarak farklılaşmak zorundadır. Fonksiyonel sitotoksik T lenfositlerine
farklılaşmak için pre-CD8+ CTL’lerin iki farklı sinyal alması gerekir.
İlki, MHC-I eksprese eden hücreler tarafından sunulan antijeni
tanımaları gerekir ve ikincisi sitokinlerle uyarılmaları gerekir. IL-2,
interferon-gama ve diğerleri CD4+ yardımcı T hücreleri tarafından sınıf
II MHC eksprese eden antijen sunan hücrelerle etkileşimleri sonucu
üretilirler. Bu iki sinyalin sonucunda pre-CTL aynı antijeni taşıyan
hedef hücreleri lize edebilen aktif CTL’ye dönüşür.
Adapted from Abbas, et. al. Cellular and Molecular Immunology. 3rd Ed.,
p. 292.
 Şekil 7
Şekil 7
CTL’ler tarafından hedef hücrelerin Fas- ve TNF- aracılı olarak
öldürülmes
|
IV.
HÜCRE ARACILI İMMÜNİTEDE HÜCRE-HÜCRE
ETKİLEŞİMLERİ – SİTOSOLDEKİ ENDOJEN ANİTJENLERE YANITTA TC HÜCRELERİN OLUŞUMU Sitotoksik T lenfositler timustan çıktıklarında tam olarak olgun değildirler.
Antijeni tanıyan fonksiyonel bir TCR’leri vardır ancak hedef hücreyi lize
edemezler. Tamamen fonksiyonel efektör Tc hücrelerine dönüşmeleri gerekmektedir.
Sitotoksik hücreler “pre-CTL” formundan iki sinyalle farklılaşırlar:
-
Uyarıcı hücre üzerinde, sınıf I MHC’de spesifik antijen
-
Th1 hücreleri tarafından üretilen sitokinler, özellikle IL-2 ve IFN-gama. Bu
Şekil 6’da gösterilmiştir.
CTL-aracılı lizisin özellikleri
-
CTL ile öldürme antijen spesifiktir. CTL tarafından öldürülmesi için hedef
hücrenin pre-CTL farklılaşmasını başlatan aynı sınıf I MHC-ilişkili antijeni
taşıması gerekir.
-
CTL ile öldürme hücre temasını gerektirir. CTL’ler hücre yüzeyindeki MHC
molekülüyle ilişkili hedef antijeni tanıdıklarında öldürmeye başlarlar. Hedef
MHC-antijeni taşımayan komşu hücreler etkilenmezler.
-
CTL’ler hedef hücreyi lize ettiklerinde zarar görmezler. Herbir CTL sırayla
birçok hedef hücreyi öldürebilme yeteneğindedir.
CTL-aracılı öldürme mekanizması
CTL’ler hedef hücreleri öldürmek için birçok mekanizma kullanırlar, bunların
bazıları direkt hücre-hücre etkileşimine ihtiyaç duyar ve diğerleri belirli
sitokinlerin üretimiyle gerçekleşir. Bütün bu mekanizmalarda hedef hücrenin
ölümü apoptozla gerçekleşir.
-
Fas- ve TNF-aracılı öldürme (Şekil 7)
Oluşturulan CTL’ler yüzeylerinde Fas ligandı eksprese eder etmez, hedef hücreler
üzerindeki Fas reseptörlerine bağlanır. Buna ek olarak, CTL’ler tarafından
salgılanan TNF-α hedef hücre üzerindeki TNF reseptörlerine bağlanabilir. Fas ve
TNF reseptörleri çok yakın reseptör ailelerindendir, reseptörleriyle trimer
oluşturmak için ligandlarıyla karşı karşıya gelirler. Bu reseptörler aynı
zamanda reseptörün sitoplazmik kısmında ölü domainleri de içerir, bunlar
trimerizasyondan sonra hedef hücrede apoptozu uyarmak için kaspazları aktive
edebilirler.
-
Granül-aracılı öldürme (Şekil 8)
Tamamen farklılaşmış olan CTL’lerin perforin ve granzimleri içeren birçok
granülü vardır. Hedef hücrelerle iletişime geçmesi üzerine perforin salınır ve
be hedef hücre membranında kanallar oluşurmak üzere polimerize eder. Serin
proteazlar olan granzimler bu kanallar vasıtasıyla hedef hücreye girer ve hedef
hücrede apoptoza sebep olacak olan kaspazları ve nükleazları aktive ederler.
|
| |
Şekil 8
Hedef hücrenin CTL ile parçalanma mekanizmaları
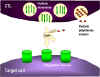 1. CTL perforin monomerlerini degranüle eder ve çevreye serbest bırakır.
Perforini poliperforin kanalları oluşturmak için polimerize eden enzimler de
salınır ve bunlar Ca++ ile birlikte hedef hücrenin membranında kanal
oluşumunu katalizlerler
1. CTL perforin monomerlerini degranüle eder ve çevreye serbest bırakır.
Perforini poliperforin kanalları oluşturmak için polimerize eden enzimler de
salınır ve bunlar Ca++ ile birlikte hedef hücrenin membranında kanal
oluşumunu katalizlerler
 2. CTL aynı zamanda perforin kanalarından geçip hedef hücreye zarar
veren parçalayıcı enzimleri ve toksinleri de salgılayabilir.
2. CTL aynı zamanda perforin kanalarından geçip hedef hücreye zarar
veren parçalayıcı enzimleri ve toksinleri de salgılayabilir.
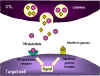 3. TNF alfa ve TNF beta gibi sitokinler CTL veya yakındaki bir
makrofajdan salınırlar. İnterferon gamma da CTL’lerden veya diğer yakın
lenfoid hücrelerden salınabilir. Bunlar hedef hücre üzerindeki reseptöre
bağlanarak apoptozu başlatırlar.
3. TNF alfa ve TNF beta gibi sitokinler CTL veya yakındaki bir
makrofajdan salınırlar. İnterferon gamma da CTL’lerden veya diğer yakın
lenfoid hücrelerden salınabilir. Bunlar hedef hücre üzerindeki reseptöre
bağlanarak apoptozu başlatırlar.
|
|
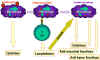 Şekil 9
Şekil 9
Makrofajlar immün sistemde T ve B hücre immünitesi
başlamadan önce temel rol oynarlar. Makrofajlar antijenleri işler ve
daha sonradan daha fazla sitokin üretimini içeren birçok fonksiyonu
yerine getirmesi için makrofajları aktive eden lenfokinleri salan T
hücrelerine sunarlar.
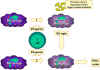 Şekil 10 Makrofaj aktivasyonu birçok sitokinin ve diğer
faktörlerin etkilşimi sonucu oluşur.
Şekil 10 Makrofaj aktivasyonu birçok sitokinin ve diğer
faktörlerin etkilşimi sonucu oluşur.
Yolak 1’de, TNF-alfa, interferon gama ve sitokin üretimini başlatan
bakteriyel bileşenlerle etkileşimi sonucu aktive olan makrofajlardan
salınır. Bu tip bir aktivasyon başlatıcıya örnek bakteriyel bir bileşen
lipopolisakkarittir. 1. Yolaktan TNF-alfa 2. yolaktaki interferonla
aktive olmuş makrofajın nitrik oksit üretmesine neden olur.
|
HÜCRESEL
İMMÜNİTEDE HÜCRE-HÜCRE ETKİLEŞİMLERİ – VEZİKÜLLERDEKİ ENDOJEN
ANTİJENLERE KARŞI YANITTA MAKROFAJLARIN AKTİVASYONU
Makrofajlar immün sistemde merkezi rol oynarlar.
Şekil 9’da gösterildiği üzere, makrofajlar şunların içinde yer alır:
-
Doğal immün sistemin bir kısmı olan ilk
savunmada
-
Th hücrelerine antijen sunumunda
-
Birçok efektör fonksiyonda (ör: sitokin üretimi,
bakterisidal ve tümörisidal aktiviteler).
Hatta makrofajlar sadece immünitede önemli rol
oynamazlar aynı zamanda dokuların reorganizasyonunda da önemlidirler.
Ancak, potent aktivitelerinden dolayı makrofajlar dokulara zarar da
verebilir. Tablo 2’de makrofajların immünitedeki ve inflamasyondaki
birçok fonksiyonu özetlenmiştir.
Enflamasyon– Ateş
Şunların üretimi:
IL-6, TNF alfa, IL-1 – pirojen olarak rol alır.
|
Doku zararı
Hidrolaseshidrolazlar,
hidrojen peroksit üretimi
Kompleman C3a
TNF alfa üretimi
|
İmmünite
Aktive olacak olan
lenfositlerin seçimi:
IL-12, Th1 aktivasyonu ile sonuçlanır.
IL-10, Th2 aktivasyonuyla sonuçlanır.
Lenfositlerin aktivasyonu:
IL-1 üretimi
Antijenin işlenmesi ve sunumu
|
Antimikrobiyal fonksiyon
Oksijen-bağımlı olarak
üretilen:
hidrojen peroksit
süperoksit
hidroksil radikal
hipoklorik asit
Oksijen-bağımsız olarak
üretilen:
asit hidrolazlar
katyonik proteinler
lizozimler
|
Dokuların reorganizasyonu
Birçok faktörün
salgılanması:
Parçalayıcı enzimler (elastaz, hiyaluronidaz, kollajenaz)
Fibroblast uyarıcı faktörler
anjiyogenezin uyarılması
|
Anti-tümör aktivitesi
ToxicfactorsToksik faktörler
HydrogenperoxideHidojen peroksit
Complement C3aKompleman C3a
ProteasesProteaz
ArginaseArjinaz
Nitric oxideNitrik oksit
TNF alphaTNF alfa
|
|
Tablo 2 |
Bu makrofaj fonksiyonlarının birçoğu sadece aktif makrofajlar tarafından
yapılabilir. Makrofaj aktivasyonu, dinlenme halindeki makrofajlar
tarafından gerçekleştirilemeyen bazı fonksiyonları aktif makrofajın
yerine getirmesini sağlayan birçok gen ürünün ekspresyonundaki
kantitatif değişiklikler olarak tanımlanabilir.
Makrofaj aktivasyonu Th1 hücrelerinin önemli bir görevidir. Th1
hücreleri makrofaj gibi bir APC ile aktive edildiğinde, makrofajları
aktive etmek için gerekli olan iki sinyalden birisi olan IFN-γ salarlar.
Bakterilerin lipopolisakkariti (LPS) veya bakteriyel ürünlere maruz
kalan makrofajlardan salınan TNF-α ikinci sinyali gönderir (Şekil 10).
Makrofajların yer aldığı efektör mekanizmalar şunları içermektedir:
-
Apoptozu uyarabilen TNF-α
-
Nitrik oksit ve diğer reaktif azot ara
ürünleri
-
Reaktif Oksijen ara ürünleri
-
Katyonik proteinler ve hidrolitik
enzimler
Th1 hücreleri tarafından makrofajların aktive edilmesi farklı
patojenlere karşı korunmada çok önemlidir. Örneğin, Pneumocystis carinii
bir ekstraselüler patojen olup normal bireylerde aktif makrofajlarla
kontrol edilirler; Ancak AIDS hastalarında en yaygın ölüm sebeplerinden
olması Th1 hücre eksiklikleri olmasından kaynaklanmaktadır. Benzer
şekilde Mycobacterium tuberculosis veziküllerde bulunan bir patojen olup
aktive edilmedikleri sürece makrofajlar tarafından etkili bir şekilde
öldürülemezler; bu yüzden de bu enfeksiyon AIDS hastalarında bir
problemdir.
|
| |
HÜCRESEL İMMÜNİTEDE HÜCRE-HÜCRE ETKİLEŞİMLERİ – NK HÜCRELERİNİN
AKTİVASYONU
Aktif Th1 hücreleri tarafından üretilen sitokinler, özellikle IL-2 ve
IFN-γ, aynı zamanda lenfokinle aktive olmuş öldürücü hücrelere (LAK
hücreleri) dönüşmesi için NK hücrelerini aktive eder. LAK hücreleri,
virüsle enfekte olduğunda veya tümör hücrelerini non-MHC-sınırlı bir
şekilde öldürebilir. Bunun yanında, hedef hücrelerin NK ve LAK
hücrelerinde öldürülmeye duyarlılıkları MHC sınıf I moleküllerinin
ekspresyonuyla ters orantılır (doğal immünite bölümüne bakınız). NK ve
LAK hücrelerinin hedef hücreleri öldürmek amacıyla kullandıkları efektör
mekanizmalar CTL’lerin kullandığıyla benzerdir (örn: perforin ve
granzimler). NK ve LAK hücreleri aynı zamanda antikorla kaplı hedef
hücreleri ADCC ile öldürebilmektedir.
|
|
|
|
|

 |
 Mikrobiyoloji ve İmmünoloji On-line, İMMÜNOLOJİ Bölümüne Dönünüz
Mikrobiyoloji ve İmmünoloji On-line, İMMÜNOLOJİ Bölümüne Dönünüz
This page last changed on
Thursday, March 31, 2016
Page maintained by
Richard Hunt
|

 Şekil 6
Şekil 6










