|
x |
x |
|
 |
 |
|
INFECTIOUS
DISEASE |
BAKTERIYOLOJİ |
İMMÜNOLOJİ |
MYCOLOGY |
PARASITOLOGY |
VIROLOGY |
|
|
İMMÜNOLOJİ- BÖLÜM ONÜÇ
SİTOKİNLER VE İMMÜNOREGÜLASYON
Dr Gene Mayer
Professor
Department of Pathology, Microbiology and Immunology
University of South Carolina School of Medicine
Çeviri:
Doç. Dr. Erkan Yula
İzmir, Katip Çelebi Üniversitesi, Tıp Fakültesi, Tıbbi Mikrobiyoloji
Anabilim Dalı
|
|
TURKISH |
|
FRANCAIS |
|
PORTUGUES |
Let us know what you think
FEEDBACK |
|
SEARCH |
|
|

 |
|
Logo image © Jeffrey
Nelson, Rush University, Chicago, Illinois and
The MicrobeLibrary |
|
|
|
Edited and illustrated by Dr Richard Hunt
|
|
ÖĞRENİM HEDEFLERİ
(i) Doğal immunite, (ii) kazanılmış immunite ve (iii) hematopoez
mediatörlerinin majör sitokinlerini vurgulamak.
İmun cevap düzenlenmesinin tartışılması
ANAHTAR SÖZCÜKLER
Monokinler, Lenfokinler, İnterlökinler, Kemokinler, TNF-α, IL-1, IL-10,
IL-12, İnterferonlar, IFN-γ, IL-2, IL-4, IL-5, TGF-β, GM-CSF, M-CSF,
G-CSF, Treg’ler
 Şekil 1A
Şekil 1A
Çeşitli sitokinlerin ortak alt üniteleri ile ilgili reseptörler
 Şekil 1B
Şekil 1B
İnterferon reseptör ailesi |
GENEL BAKIŞ
Sitokinler, hücreler arasında mediatör olarak davranan çeşitli antikor
olmayan proteinlerin oluşturduğu bir gruptur. Bunlar, başlangıçta mediatör
olarak davranan ve bağışıklık süreçleri regüle eden immün sistem hücrelerinin
ürünleri olarak tanımlanmışsa da bu gün artık birçok sitokinin immün sistem
dışındaki hücreler tarafından da üretildiği ve immün sistem dışı hücreleri de
etkileyebileceği bilinmektedir. Sitokinlerin, günümüzde çeşitli bozuklukların
tedavisi için, biyolojik cevabı modifiye edici olarak klinik kullanımı
bulunmaktadır. Sitokin terimi büyük bir protein grubunu tanımlamak için
kullanılan genel bir terimdir ancak belirli türde sitokinleri tanımlamak için
yaygın kullanılan diğer terimler de vardır. Bunlar aşağıdakileri içerir:
- Monokinler, tek çekirdekli fagositik hücreler tarafından üretilen
sitokinler
- Lenfokinler, Aktive lenfositlerden, özellikle Th hücreleri tarafından
üretilen sitokinler
- İnterlökinler, lökositler arasında mediatör olarak hareket sitokinler
- Kemokinler, öncelikle lökosit göçünden sorumlu küçük sitokinler
Sitokinler, sitokin ağı denilen daha büyük birbiriyle ilişkili proteinler
sisteminin ve sinyal iletiminin bir parçası olarak işlev görür. Bunlar, farklı
hücrelerin hücre tarafından alınan diğer sinyallere bağlı olarak aynı sitokine
farklı yanıt verebildiği karmaşık etkileşimlerdir. Sitokin sinyalizasyonu
oldukça değişkendir ve hem koruyucu hem de hasar verici tepkilere neden olabilir.
Bir sitokin, genellikle diğer sitokinlerin sentezini etkiler. Bir kaskad
başlatabilirler, arttırabilirler ya da diğer sitokinlerin üretimini bastırabilir.
Ayrıca, genellikle diğer sitokinlerin davranışlarını etkileyebilirler. Bu
etkiler antagonistik, aditif ya da sinerjistik olabilir.
Sitokinler genellikle öncül proteinler olarak depolanamazlar. Aksine onların
sentezi, gen transkripsiyonu tarafından başlatılır ve mRNA'ları kısa ömürlüdür.
Bağışıklık yanıtta ihtiyaç duyulduğunda üretilirler. Sitokinleri kodlayan genler,
birbirinden çok az farklı ama biyolojik olarak önemli biyoaktiviteye sahip
proteinler elde etmek için alternatif kırpılma ile varyantlar üretebilir.
Pek çok özgün sitokin hem doğal hem de kazanılmış bağışıklık yanıta dahil olan
çok sayıda hücre türleri tarafından üretilir. Özgün sitokinler birçok hücre
tiplerine etki eder (başka deyişle, pleotropiktirler) birçok durumda benzer
fonksiyonları vardır (örnmeğin ihtiyaçtan fazladırlar). . Fazlalık sitokin
reseptörlerinin niteliğine nedeniyledir.
Sitokinler reseptörleri, ortak yapısal özelliklerine göre aileler halinde
gruplandırılabilen heterodimerler dir (bazen heterotrimerler); bir alt birimi
belirli bir ailenin tüm üyeleri için ortaktır. Bazı örnekler, Şekil 1 'de
gösterilmiştir.
- Tip 1 sitokin reseptörleri (IL-2R ailesi), sitokin reseptörlerinin en
büyük ailesidir. Bu aile ortak bileşenleri göre üç alt-gruba ayrılmıştır:
IL2Rγ ortak β ve gp130 (Şekil 1A). Bu reseptörlerin intrinsik protein
tirozin kinaz aktivitesi yoktur. Ligand (sitokin) bağlanması reseptör
dimerizasyonuna ve hücre içi sinyal başlatılmasına yol açar.
- Tip 2 sitokin reseptörlerinin (IFNR ailesi) alt ünitelerin ekstraselüler
parçalarındaki sisteinleri korunmuştur. Hücre-dışı domainler aynı zamanda,
bu sitokin reseptör ailesinin ardışık immünoglobülin benzeri bölgeleri
özelliğine sahiptir. Bu reseptör alt-üniteleri de (Şekil 1 B 'de * ile
belirtilmiştir) ayrıca tirozin kinaz aktivitesine sahiptir.
Kemokin reseptörleri tüm GTP bağlayıcı proteinler ile bağlantılı yedi
transmembran segmentine sahiptir. Onlar seçici olarak belirli lenfosit
popülasyonlarında eksprese edilirler ve bağlandıkları kemokin ailesine göre
isimlendirilirler; CXCR ligandı gibi CXC kemokinlere bağlanırken CCR (CC
reseptörü) ligandı gibi CC kemokinlere bağlanır (kemokinlerin adlandırma kuralı
aşağıda tartışılacaktır).
Tüm aile üyelerinin sitokin bağlanma ve sinyal transdüsyonu fonksiyonlarında
alt birimleri ortak olduğu için, bir sitokin reseptörü genellikle aynı aileden
başka sitokine de yanıt verebilir. . Böylece, örneğin izole bir IL-2 eksikliği,
diğer sitokinler (IL-15, IL-7, IL-9 vs) onun işlevini de yerine getireceğinden,
olumsuz bir etkiye neden olmaz. Benzer şekilde, bir sitokin reseptörü alt-ünitesindeki
bir mutasyon genellikle çok az bir etkiye sahiptir. Öte yandan, ortak alt
birimdeki bir mutasyonun önemli etkileri vardır. Örneğin IL-2R gama alt-ünitesi
genindeki bir mutasyon bir tam ya da tama yakın T ve B hücre bozuklukları ile
karakterize insan X'e bağlı ağır kombine immün yetmezliği (XSCID)’ne neden olur.
Sitokinler hedef hücreler üzerindeki spesifik reseptörlerine yüksek afinite
ile bağlanır ve hücreler sitokine yanıta göre:
- Sitokin salgılanan aynı hücre (otokrin)
- Yakındaki bir hücre (parakrin)
- Dolaşım aracılığıyla uzak bir hücre (endokrin)’dir. Sitokinlere hücresel
yanıt genellikle yavaştır (saatler) çünkü yeni mRNA ve protein sentezini
gerektirir.
|
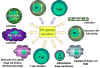 Şekil 2
Şekil 2
İnterferon gamanın immun sistem üzerinde immunregülatör rolleri. IFN
alfa ve IFN betadan antiproliferatif ve anti-ral aktivitelerinin daha
zayıf olduğuna dikat ediniz. Üçü arasında makrofaj aktivasyonu ve MHC
sınıf II ekspresyonu indüksiyonun en güçlü yapan IFN gamadır.
|
SİTOKİN KATEGORİLERİ
Sitokinler fonksiyonlarına veya kaynağına göre farklı kategoriler halinde
gruplandırılabilir ancak çok farklı hücreler tarafında üretilebilmeleri ve
birçok farklı hücreyi etkileyebilmeleri nedeniyle sınıflandırma
girişimlerinde sınırlamalar yaşanacağı akılda tutulmalıdır.
Doğal bağışıklığın mediatörleri
(doğal bağışık yanıt)
Doğal bağışıklık sisteminde önemli rol oynayan sitokinler şunlardır:
TNF-α, IL-1, IL-10, IL-12, tip I interferonlar (IFN-α ve IFN-β), IFN-γ,
ve kemokinler.
TNF-α
Tümör nekroz faktör alfa mikroplara, özellikle Gram negatif bakterin
lipopolisakkarid (LPS) 'lerine karşı yanıtta aktifleşmiş makrofajlar
tarafından üretilirler. Akut inflamasyonda önemli bir aracıdır.
Endotel hücrelerinin adezyon moleküllerini üretmek üzere uyararak ve
sitokinler için kemotaktik olan kemokinleri üreterek enfeksiyon
bölgelerine nötrofil ve makrofajların yapışmasına aracılık eder. TNF-α,
aynı zamanda, ateş oluşumu için hipotalamusa etki eder ve akut faz
protein üretimini kolaylaştırır.
IL-1
İnterlökin-1, aktive makrofajlar tarafından üretilen diğer bir
enflamatuar sitokindir. Etkileri, TNF-α’ya benzer ve aynı zamanda T
hücrelerinin aktive edilmesine yardımcı olur.
IL-10
İnterlökin 10, aktive edilmiş makrofajlar ve Th2 hücreleri
tarafından üretilir. Bu ağırlıklı olarak inhibitör bir sitokindir.
IFN-γ’nın Th1 hücreleri tarafından üretimini inhibe eder, böylece
bağışık yanıtı Th2 tipe kaydırır. Aynı zamanda, aktive edilmiş
makrofajlarda sitokin üretimini, sınıf II MHC ekspresyonunu ve
makrofaj üzerindeki ko-stimulatör molekülleri inhibe eder, bu da
immün yanıtta azalma ile sonuçlanır.
IL-12
İnterleukin 12 aktive edilmiş makrofajlar ve dendritik hücreler
tarafından üretilir. IFN-γ üretimini ve Th hücrelerin Th1 hücrelere
farklılaşmasını uyarmaktadır.. Buna ek olarak, Tc ve NK hücrelerinin
sitolitik fonksiyonlarını artırır.
Tip I interferonlar
Tip I interferonlar (IFN-α ve IFN-β), birçok hücre türü tarafından
üretilir ve hücrelerde viral replikasyonu inhibe etmede görev
yaparlar. Ayrıca, hücrelerde CTL’ler ile öldürülmeye karşı onları
daha hassas hale getiren sınıf I MHC moleküllerinin ifadesini
arttırır. Tip I interferonlar ayrıca NK hücreleri aktive etmektedir.
INF-γ
İnterferon gama, daha düşük ölçüde Tc ve NK hücreleri tarafından da
üretilebilse de, asıl olarak Th1 hücreler tarafından üretilen önemli
bir sitokindir. Şekil 2'de de gösterildiği gibi, hem doğal hem de
adaptif bağışıklık sistemde çok sayıda fonksiyona sahiptir.
Kemokinler
Kemokinler, birçok türden lökositler ve diğer hücre tipleri
tarafından üretilen kemotaktik sitokinlerdir. Bunlar, enfeksiyon
bölgelerine lökositleri yönlendiren ve hangi hücrenin epitelden
geçip nereye gideceğini belirleyerek lenfosit trafiğinde rol oynayan
büyük bir molekül ailesini temsil eder. Korunmuş sistein
aralıklarına dayalı olarak dört kemokin ailesi vardır. Bir CXC
yapısına (arasında farklı bir amino asit ile iki sistein) sahip α-kemokinler
ve CC yapısına (iki komşu sistein) sahip β-kemokinler bunlara iki
φrnektir. Baπύmsύz kemokinler(aynύ aile iηinde) genellikle birden
fazla reseptφre baπlanύr.
|
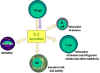 Şekil 3
Şekil 3
İnterlökin-2’nin immuno-regülatör davranışları
 Şekil 4
Şekil 4
T hücre proliferasyonu ve sitokinler. T hücreler sessiz durumdayken
interlökin 2, 4 ve 7 gibi sitokinleri üretmez . Ya da yüksek miktarda
reseptör eksprese etmez. IL-2 reseptörleri yoktur. T hücre aktivasyonu
yüksek afiniteli IL-2 reseptörlerinin oluşumu, IL-2 ve IL-4 sentez ve
sekresyonunun uyarılması ile sonuçlanır. Bunlar reseptörlerine bağlanır
ve hücreler prolifere olur. İnterlökinlerle uyarılma azaldığında (örneğin
antijen uyarımı azaldığında) reseptörler bozunur ve proliferasyon fazı
sonlanır. Not: sitokinlerle stimulasyon parakrin ya da otokrin olabilir.
|
Kazanılmış immünitenin
mediatörleri
Kazanılmış bağışıklık sistemde önemli rol oynayan sitokinler:
IL-2, IL-4, IL-5, TGF-β, IL-10 ve IFN-γ’dır.
IL-2
IL-2, daha düşük düzeyde Tc hücreleri tarafından yapılabilse de Th
hücreleri tarafından üretilir. T hücreleri için ana büyüme faktörüdür.
Ayrıca Şekil 3 de gösterildiği gibi, B hücrelerinin büyümesini teşvik
ededebilir, NK hücreleri ve monositleri aktive edebilir. IL-2 T
hücreleri üzerinde otokrin etkilidir. T hücrelerinin aktivasyonu IL-2R
ekspresyonu ve IL-2 üretimi ile sonuçlanır. IL-2, IL-R'ye bağlanır ve
hücre bölünmesini teşvik eder. T hücrelerin antijen tarafından
uyarılması bittiğinde, IL-2R sonunda azalır ve çoğalma fazı sona erer
Şekil 4.
IL-4
İnterlökin 4 makrofajlar ve Th2 hücreleri tarafından üretilir. Naif Th
hücrelerinin Th2 hücrelerinin dönüşümünü ve antikor yanıtın oluşması ile
sonuçlanan farklılaşmış Th2 hücre büyümesini teşvik eder. Ayrıca, Ig
sınıfının IgE izotipine anahtar çevirimini stimule eder.
IL-5
İnterlökin 5 Th2 hücreleri tarafından üretilir ve B hücrelerinin ve
eozinofillerin büyümesini ve farklılaşmasını güçlendirmede rol oynar.
Ayrıca, olgun eosinofilleri aktive eder.
TGF-β
Transforme edici büyüme faktörü beta, T hücreleri ve diğer hücre türü
tarafından üretilir. Esas olarak inhibitör bir sitokindir. T
hücrelerinin çoğalmasını ve makrofaj aktivasyonunu inhibe eder. Aynı
zamanda, pro-enflamatuar sitokinlerin etkilerini, PMN ve endotelyal
hücreleri üzerine etki ederek bloke edebilir.
Hematopoez
stimulatörleri
Bazı sitokinler hematopoetik hücrelerin farklılaşmasını uyarır. Bunlar,
kemik iliği öncüllerinin farklılaşmasını teşvik eden GM-CSF, öncül
hücrelerin büyümesini ve monositler ve makrofajlara farklılaşmasını teşvik
eden M-CSF ve PMN’lerin üretimini teşvik eden G-CSF’yi kapsar.
Interlökin 17
IL-17, yaklaşık 150 amino asit uzunluğunda bir proenflamatuar sitokindir.
IL-17 ailesi, dizi homolojisini paylaşan ancak doku ekspresyonuyla
farklılaşan altı üyeyi kapsar. IL-17, Th17 hücreler tarafından üretilir ve
aşırı ekspresyonu multipl skleroz, romatoit artrit ve inflamatuar bağırsak
hastalığı dahil olmak üzere otoimmün hastalıklarla ilişkilendirilmiştir.
|
|
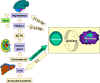 Şekil 5a
Şekil 5a
Sitokin ağı. Lenfositler ve makrofajlar ile hipotalamus, adrenaller ve
karaciğer arası iletişim.
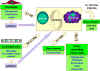 Şekil 5b
Şekil 5b
Sitokin ağı. Lenfositler ve makrofajlar ile diğer hücreler ve dokular
arası iletişim. |
SİTOKİN AĞLARI Çoğu
araştırmanın odak noktası sitokinlerin üretimi ve bağışıklık sistemi
hücreleri üzerine etkileri olmasına rağmen, çoğunun pek çok başka
hücreleri ve organ sistemlerini etkilediği hatırda tutulmalıdır. Aslında
sitokin ağı oldukça karmaşıktır ve birbirleri arasında örtüşen diziler
ve ilişkili bağlantılar gösterirler. Bu ağ içinde, bir sitokin kendinin,
diğer sitokinlerin veya sitokin reseptörlerinin (hem kendinin hem de
diğer sitokinlerin reseptörlerinin) sentezini arttırabilir ya da suprese
edebilir ve başka sitokinler ile antagonize edilebilir veya sinerji
içinde olabilir.
Sitokin ağı içindeki bazı etkileşimlerin gösterildiği diyagram Şekil 5
a, b ve c'de sunulmaktadır.
|
|
|
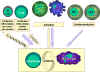 Şekil 5c
Şekil 5c
Sitokin ağı. Lenfositler, makrofajlar ve bağışıklık sisteminin diğer
bileşenleri arasında iletişim |
|
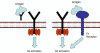 Şekil 6
Şekil 6
Antikorla regülasyon. Çözünür antikorlar antijen bağlamada hücre yüzey
Ig ile yarışır(solda) ya da Fc reseptörlerine bağlanarak inhibitör
sinyal oluşumuna yol açar (sağda)
|
İMMÜNOREGÜLASYON
Bir immün cevabının büyüklüğü, lenfositlerin antijen sunucu aktivasyonu
ile cevabı önleyen ya da azaltan negatif regülatör etkiler arasındaki
dengeyle belirlenir. Düzenleyici mekanizmalar, bir bağışıklık tepkisinin
tanıma, aktivasyon veya efektör aşamasında rol oynayabilir. Daha önce
tartışılan düzenleme örnek olarak şunları içerir:
- Ko-stimülasyon yokluğunda antijen tanıma anerjiyle sonuçlanır
- B7-CTLA-4 bağlanmasıyla antijenin tanınması T hücresi
aktivasyonunun down-regülasyonu ile sonuçlanır
- Bağışıklık hücreleri üzerinde stimulatör ve inhibitör etkili
sitokinler
- İdiyotipik/anti-idiyotipik etkileşimler bağışıklık yanıtının
stimülasyon ya da inhibisyonuna neden olur
- Antijenle karşılaşma yolu ve dozu bir durumda korunmaya diğer
bir durumda ise toleransa neden olan farklı Th yanıtlarını
tetikleyebilir.
Bunlara ek olarak bağışiklık yanıtın regüle edilebileceği başka
yollar da mevcuttur.
Antikorla regülasyon
(Şekil 6)
Solübl antikorlar B hücreleri üzerindeki antijen
reseptörleriyle yarışarak B hücresi aktivasyonunu önleyebilir ya
da bloke edebilir. Buna ek olarak, antijen-antikor kompleksleri
B hücreleri üzerindeki Fc reseptörlerine bağlanabilir ve B
hücrelerine önleyici bir sinyal gönderebilir. Bu durumda
düzenleme tanıma düzeyine gerçekleşir. Ayrıca, antijen-antikor
kompleksleri B hücrelerine önleyici bir sinyal göndererek, B
hücreleri üzerindeki Fc reseptörlerine bağlanabilir. Buradaysa
düzenleme aktivasyon seviyesinde gerçekleşir.
Antikor ayrıca ASH için antijen kaynağını koruyarak
aktivasyonu düzenleyebilir (arttırıcı yönde). Bu durumda,
antikor komleman sistemi bağlayan ve aktive eden bir immun
kompleks oluşturmak üzere antijeni bağlar. Kompleman aktivasyonu
ASH üzerindeki kompleman reseptörüne bağlanmayı sağlar.
Sitokinlerle regülasyon
Sitokinler hem pozitif hem de negatif regülatörlerdir. Bunlar,
immun cevabın birçok aşamasında rol alır, ancak aktivitesi
efektör hücreleri üzerindeki reseptör ekspresyonu kadar aynı
mikroçevrede sunulan diğer sitokinlere de bağlıdır. Sitokinler
meydana gelen immün yanıtın tipini ve büyüklüğünü düzenler.
Regülatör T hücreleriyle
düzenleme (Treg’ler)
Regülatör T hücreleri (Treg’ler) yakın zamanda tanımlanmış
immun cevabı düzenleyici hücre popülasyonlarıdır. Onlar ilk T
hücre aktivasyona engel olmak yerine, devam eden yanıtı inhibe
ederek kronik ve muhtemelen zararlı yanıtları önlerler. Th1, Th2
veya TH17 hücrelerinin özelliklerini taşımazlar ancak hem Th1
hem de Th2 yanıtını baskılayabilir.
Doğal Treg oluşumu
Timus Treg olarak işlev gören CD4 +/ CD25 +/ Foxp3 +
hücreleri meydana getirir. Bu Treg’ler hücresel temasa
bağımlı bir yolla immun yanıtı baskılar ancak bu supresyon
mekanizması henüz kanıtlanmamıştır.
İndüklenen Treg’ler
Periferde bazı T hücreleri Treg’lere dönüşmek üzere
antijenlerle, IL-10 ve TGF-β2’den biri ile uyarılır. IL-10
ile indüklenen Treg’ler CD4+/CD25+/Foxp3 –‘tir ve Tr1 olarak
anılırlar. Bu hücreler IL-10 salınımıyla immun yanıtı
baskılarlar. TGF-β ile indüklenen Treg’ler
CD4+/CD25+/Foxp3+’tir ve indüklenen Treg’ler olarak
anılırlar. These cells suppress by secretion of TGF-β. Bu
hücreler TGF-β salınımıyla baskılanırlar.
CD8 + Treg'ler
Bazı CD8 + hücreler, Treg hücresine dönüşmek üzere antijen
ve IL-10 ile indüklenebilir. Bu hücreler, CD8 / Foxp3 +’tir
ve hücresel temasa bağımlı bir mekanizma ya da sitokin
salgılanmasıyla immünsistemi bastırırlar. Bu hücreler, in
vitro olarak gösterilmiştir ama in vivo olarak mevcut olup
olmadığı bilinmemektedir.
İmünoregülasyonu
etkileyen genetik faktörler
MHC-bağlantılı genler enfeksiyon yanıtının kontrolüne
yardımcı olurlar. Bazı HLA haplotipleri, yanıt oluşturan veya
oluşturmayan bireylerin duyarlı veya dirençli olmasıyla
ilişkilidir.
MHC dışı genler de ayrıca immunoregülasyona katılır. Makrofaj
aktivitesi ile ilişkili olarak fagolizozoma nitrit (NO2-)
taşınması ile ilgili bir taşıyıcı proteini, doğal
direnç-ilişkili makrofaj proteini-1 (NRAMP1)’i, kodlayan gen
buna bir örnektir. Bu gendeki polimorfizmler makrofajların
aktivitesini değiştirebilir.
Yukarıda ele alındığı gibi sitokin, kemokin ve bunların
reseptörleri immunregülasyona katılmaktadır. Başta reseptörler
olmak üzere bunları kodlayan genlerdeki polimorfizmlerin,
enfeksiyona duyarlılık ya da otoimmün hastalık oluşumuyla
ilişkili olduğu gösterilmiştir.
|
| |
|
Tablo 1 - SİTOKİNLERİN
ÖZELLİKLERİ |
|
Sitokin |
Kaynaklandığı Hücre |
Hedef Hücre |
Başlıca etkileri |
|
IL-1 |
Monositler
Makrofajlar
Fibroblastlar
Epiteliyal hücreler
Endoteliyal hücreler
Astrositler |
T hücreler; B hücreler
Endoteliyal hücreler
Hipotalamus
Karaciğer
|
Kostimulatör molekül
Aktivasyon (inflamasyon)
Ateş
Akut faz reaktanları
|
|
IL-2 |
T hücreleri
NK hücreleri |
T hücreler
B hücreler
Monositler
|
Büyüme
Büyüme
Aktivasyon
|
|
IL-3 |
T hücreleri |
Kemikiliği öncülleri |
Büyüme ve farklılaşma |
|
IL-4 |
T hücreleri |
Naif T hücreler
T hücreler
B hücreler
|
TH 2 hücrelere dönüşüm
Büyüme
Aktivasyon ve büyüme; Ig E’ye izotip çevrimi
|
|
IL-5 |
T hücreleri |
B hücreler
Eozinofiller
|
Büyüme ve aktivasyon |
|
IL-6 |
T hücreleri
Makrofajlar
Fibroblastlar |
T hücreler
B hücreler
Matür B hücreler
Karaciğer
|
Kostimulatör molekül
Büyüme(insanda)
Akut faz reaktanları
|
|
IL-8
family
|
Makrofajlar
Epiteliyal hücreler
Plateletler |
Nötrofiller |
Aktivasyon ve kemotaksis |
|
IL-10 |
T hücreleri (TH2) |
Makrofajlar
T hücreler
|
ASH aktivitesinin inhibisyonu
Sitokin üretiminin inhibisyonu
|
|
IL-12 |
Makrofajlar
NK hücreleri |
Naif T hücreler |
TH 1 hücreye dönüşüm |
|
IFN-gamma |
T hücreleri
NK hücreleri |
Monositler
Endoteliyal hücreler
Özellikle makrofajlar olmak üzere çoğu dokudaki hücreler
|
Aktivasyon
Aktivasyon
MHC sınıf I ve II artışı
|
|
TGF-beta |
T hücreleri
Makrofajlar |
T hücreler
Makrofajlar
|
İnhibisyon aktivasyon ve büyüme
Aktivasyon inhibisyonu
|
|
GM-CSF |
T hücreleri
Makrofajlar
Endoteliyal hücreler
Fibroblastlar |
Kemikiliği öncülleri |
Büyüme ve farklılaşma |
|
TNF-alpha |
Makrofajlar
T
hücreleri |
IL-1 ile benzer |
IL-1 ile benzer |
|
IL = interleukin
GM-CSF
= granulocyte-macrophage colony stimulating factor
IFN = interferon TNF =
tumor necrosis factor
TGF = transforming
growth factor
|
|
|

 |
 Mikrobiyoloji ve İmmünoloji On-line, İMMÜNOLOJİ Bölümüne Dönünüz
Mikrobiyoloji ve İmmünoloji On-line, İMMÜNOLOJİ Bölümüne Dönünüz
This page last changed on
Thursday, March 31, 2016
Page maintained by
Richard Hunt
|

 Şekil 2
Şekil 2 Şekil 3
Şekil 3 Şekil 5c
Şekil 5c





